Материал: Идентификация генов изоцитратлиазы в прорастающих семенах арабидопсиса
Ген кодирующий изоцитратлиазу у психрофитной бактерии Colwellia maris был клонирован и секвенирован. Длина гена icl составила 1584 пар оснований, а длина первичной аминокислотной последовательности белка - 528 аминокислотных остатков. Молекулярная масса белка составила 58 кДа[28].
Другими исследователями была расшифрована кДНК из Strongyloides stercoralis. Сиквенс нуклеотидной последовательности кДНК показал, что она кодирует ИЦЛ. Концептуально полученная аминокислотная последовательность с открытой рамкой считывания кодирует белок размером 450 аминокислтных остатков с молекулярной массой субъединицы 50кДа.
Показано, что в мышечных клетках, а также клетках кишечика C. elegans в избытке содержится белок с молекулярной массой 106 кДа[21], который обладает ИЦЛ и МС каталитическими активностями. Данный белок назван бифункциональным белком глиоксилатного цикла. Его кДНК состоит из 3274н. п. N-концевой домен белка состоит из 443 аминокислотных остататков и имеет значительную степень гомологии с ИЦЛ грибов, бактерий и растений. Изоцитратлиаза из кукурузы Zea mays L. - тетрамерный белок, состоящий из идентичных субъединиц с молекулярной массой 64 kDa каждая[30].
Также показано, что
изоцитратлиаза M. tuberculosis
имеет гомотетрамерное строение. Каждая субъединица состоит из 14 α-спиралей
и 14 ß-структур.
Все субъединицы устойчиво связаны взаимодействием спиралей. Восемь α-спиралей
и восемь ß-структур,
составляющий самый большой домен и основу структуры, формирует α/ß-баррель.
Активный центр ИЦЛ типично для подобных структур формируется C-концевыми
остатками ß-структур. Плоская
молекула глиоксилата в активном центре координационно связывается с ионом Mg2+,
а также образует водородные связи с аминокислотными остатками Ser
91, Gly 92, Trp
93, Arg 228.
Молекула сукцината с другой частью активного центра фермента и формирует
водородные связи с Asn
92, Glu 295, Arg
228, Gly 192,
(первая карбоксильная группа) и Thr
347, Asn 313, Ser
315, Ser 317, His
193, (вторая карбоксильная группа).
Глава 2. Экспериментальная
часть
.1 Цели и задачи
Целью работы являлась идентификация генов изоцитратлиазы в прорастающих семенах арабидопсиса.
Для достижения цели были поставлены следующие задачи:
. Изучить динамику активности изоцитратлиазы в семенах арабидопсиса.
. Выделить суммарную клеточную РНК из прорастающих семян арабидопсиса.
. Методом обратной транскрипции получить кДНК из РНК объекта исследования.
. Провести ПЦР анализ
кДНК из семян арабидопсиса для идентификации генов ИЦЛ.
.2 Объекты и методы
исследования
.2.1 Объект исследования
В качестве основных объектов
исследования в работе использовали 4-дневные семена Arabidopsis
thaliana L., выращенные
гидропонным способом при 25° и интенсивности света 25 Ватт/м2.
2.2.2 Методы исследования
Определение активности изоцитратлиазы
Измерение активности изоцитратлиазы проводилось спектрофотометрическим методом при длине волны 324 нм на СФ-46 в кюветах с толщиной слоя 1 см в течение 5 минут при 25оС. Коэффициент экстинкции (ε при 324) составил 1,7 мМ-1 см-1. Спектрофотометрирование проводили в среде колориметрирования с добавлением 20 мкл гомогената.
Активность изоцитратлиазы измеряли спектрофотометрически по увеличению оптической плотности при 324 нм. Среда колориметрирования содержала 50 мМ Tris-HCl (pH 7,5); 1 мМ изоцитрат калия; 5 мМ MgCl2; 4 мМ фенилгидразин солянокислый. Данный метод основан на образовании комплекса фенилгидразина с глиоксилатом, поглощающим при 324 нм (рис.3).
За единицу ферментативной активности принимали количество фермента, которое превращает 1 мкмоль субстрата за одну минуту при 25оС и оптимальном значении рН.
Общее количество белка определяли по методу Лоури [27]. Оптическую плотность растворов определяли на спектрофотометре СФ-46 (ЛОМО, Россия) при 750 нм.
Суммарную клеточную РНК выделяли методом фенол-хлороформной экстракции [8] со следующими модификациями. Для ингибирования РНКаз на стадии получения клеточного лизата использовали 42,6% гуанидин тиоцианат. Очистку РНК проводили при помощи осаждения хлоридом лития. Качественный анализ препаратов РНК проводили путём неденатурирующего электрофореза в 1% (в/о) геле агарозы при напряжённости электрического поля 7 В/см. Окрашивание геля производилось 0,1% водным раствором бромистого этидия. Визуализация результатов проводилась с использованием трансиллюминатора с длиной волны 312 нм. Результаты фиксировались цифровой видеокамерой Samsung и обрабатывались с помощью пакета программ Gel Explorer 1.0.
Обратную транскрипцию проводили с использованием ревертазы RevertAid M-MuLV (Fermentas, Литва) согласно рекомендациям фирмы-производителя. Для проведения обратной транскрипции использовали 1 мкг суммарной клеточной РНК. В качестве затравочного использовался олиго-(dT)20 праймер. Для предотвращения деградации матриц РНК в реакционную смесь вносилось 20 ед. ингибитора РНКаз IRNasine.
Для идентификации генов
изоцитратлиазы использовали специфические праймеры, разработанные с применением
программного обеспечения FastPCR
(Финляндия). Последовательности праймеров для гена icl
1: прямой 5'-atcgcacacccacttacctc-3'
и обратный 5'-ttcccctagagcgtttctga-3'
(Tm=57°С).
Последовательности генспецифических праймеров для icl
2: прямой 5'-atcgaggacgagtgg-3'
и обратный 5'-gtcccagtcccagac-3'
(Tm=58°С).
Полимеразную цепную реакцию [23] проводили в термоциклёрах Biometra
(Biometra, Германия) и «Терцик»
(ДНК-Технология, Россия). Исследование результатов полимеразной цепной реакции
проводили при помощи электрофореза в 1% агарозном геле в присутствии 0,1%
этидиум бромида. Размер продуктов определяли путём сравнения с маркерами ДНК
известной длины (СибЭнзим, Россия).
.3 Результаты и их обсуждение
.3.1 Динамика активности изоцитратлиазы
Измерение активности
изоцитратлиазы в семенах арабидопсиса в течение 10 дней показало, что она
индуцируется с первых дней прорастания и достигает максимального значения уже
на четвертые сутки. Возрастание активности ИЦЛ свидетельствует об
интенсификации глиоксилатного цикла.

Рис. 3. Динамика активности
изоцитратлиазы из семян арабидопсиса.
Активное функционирование
глиоксилатного цикла приводит к уменьшению содержания жирных кислот в семенах и
увеличению количества сахаров и их производных. Первоначально идет активное
запасание сахаров, которое сменяется их потреблением в период интенсивного
прорастания. По мере снижения концентрации жирных кислот, происходит уменьшение
активности ИЦЛ.
.3.2 Идентификация генов icl 1 и icl 2
В результате применения
оптимизированной методики выделения с использованием фенол-хлороформной
экстракции была проведена экстракция суммарной клеточной РНК из семян
арабидопсиса. В ходе выделения в качестве хаотропного агента был использован
гуанидин-изотиоцианат. Применение данного соединения позволило получить
высокоочищенные препараты недеградированной РНК из растительных клеток, что
было установлено путём проведения аналитического электрофореза в 1% агарозном
геле (рис. 4). На приведённой электрофореграмме результатов типичного выделения
видно, что количество 28S
рРНК преобладает над 18S
рРНК, что свидетельствует об отсутствии деградации препарата под действием
РНКаз. Кроме того, в полученных препаратах отсутствовали примеси геномной ДНК,
что является важным условием успешного проведения дальнейших манипуляций с
выделенной РНК и позволяет получать достоверные и воспроизводимые результаты
при измерении концентрации растворов РНК и проведении полимеразной цепной
реакции.
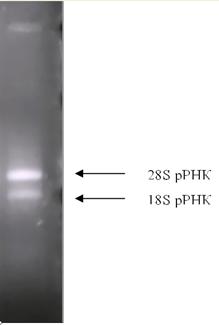
Рис. 4. Электрофорез суммарной
клеточной РНК из семян арабидопсиса, в 1% агарозном геле в присутствии
бромистого этидия.
Для синтеза первой цепи комплементарной ДНК использовалась рекомбинантная обратная транскриптаза вируса Moloney лейкоза мышей M-MuLv. Данный фермент состоит только из одной субъединицы и проявляет 5’→3’ праймер-зависимую полимеразную активность, эффективную только в отношении матриц РНК [15]. В качестве затравочного праймера использовался олиго-(dT)20 праймер.
Использование данного праймера
позволяет избирательно перевести в форму ДНК только молекулы информационной
РНК, представляющих собой транскрипты работающих генов. Применение в реакционной
смеси ингибитора РНКаз IRNasine
[6] позволило избежать деградации матриц РНК во время протекания реакции и
получить набор комплиментарных ДНК (рис. 5). Полученные в ходе обратной
транскрипции продукты использовались далее для проведения полимеразной цепной
реакции.


Рис. 5. Продукты обратной
транскрипции суммарной клеточной РНК семян арабидопсиса с использованием
ревертазы M-Mulv
и олиго-(dT)20
праймера.
Обратная транскрипция выделенной
РНК и последующий ПЦР-анализ кДНК с праймерами для icl1
и icl2 генов
изоцитратлиазы показали наличие двух полос на гель-электрофорезе (рис. 6), что
свидетельствует об экспрессии этих генов. Анализ банка данных GeneBank
показал, что в геноме арабидопсиса изоцитратлиаза кодируется двумя генами,
расположенными в разных хромосомах.


Рис. 6. Результаты ПЦР на
матрице кДНК с использованием праймеров для генов icl1
и icl2.
Полученные результаты показывают, что в геноме арабидопсиса, на стадии прорастания семян экспрессируются одновременно два гена изоцитратлиазы.
Экспрессия двух генов в семенах арабидопсиса связана с тем, что в период прорастания клетки зародыша нуждаются в большом количестве энергии и материала для биосинтетических процессов. На начальных этапах прорастания семена осуществляют гетеротрофный тип питания, используя в качестве субстратов запасные вещества. В том числе, осуществляется процесс превращения запасных жиров в углеводы через глиоксилатный цикл, являющийся звеном глюконеогенеза.
При прорастании семян арабидопсиса происходит интенсификация процессов утилизации запасных веществ, в том числе липидов, что, вероятно, связано с индукцией глиоксилатного цикла. Так появление активности изоцитратлиазы в первый день прорастания и постепенное ее увеличение до максимума на 4 день свидетельствует об активной утилизации липидов.
Изучение, включавшее выделение суммарной клеточной популяции РНК и проведение обратной транскрипции, получение комплементарной ДНК и ОТ-ПЦР анализ, показало, что в ходе прорастания семян арабидопсиса экспрессируются оба гена изоцитратлиазы - icl1 и icl2.
Таким образом глиоксилатный
цикл может иметь более универсальное распространение в организмах чем считалось
ранее. При этом данный метаболический путь не функционирует на протяжении всего
онтогенеза, а индуцируется на определенных стадиях и выполняет ключевую роль в
мобилизации запасного пула жирных кислот.
Выводы
.Изучена динамика активности ИЦЛ при прорастании семян арабидопсиса и показано, что исследуемый фермент имеет максимальное значение активности на 4 день прорастания. Вероятно, в данный период осуществляется активная утилизация запасных липидов через глюконеогенез.
2. Применение олиго-dT праймера в качестве затравки при проведении реакции обратной транскрипции, дало возможность получить набор кДНК к матричной РНК из семян арабидопсиса, пригодных для дальнейших анализов.
3. Методом ОТ-ПЦР, с
использованием специфических праймеров к генам изоцитратлиазы, установлено, что
в семенах активно транскрибируются два гена - icl1
и icl2. Вероятно, в
процессе развития организма происходит экспрессия генов ИЦЛ, обеспечивающей
протекание глиоксилатного цикла в растительной клетке, при конверсии липидов в
углеводы.
Литература
1. Гааль Э. Электрофорез в разделении биологических макромолекул / Э. Гааль, Г. Медьеши, Л. Верецкеи. // М., 2012. - 446с.
. Епринцев А.Т. Глиоксилатный цикл: универсальный механизм адаптации?/ А.Т Епринцев., В.Н Попов., М.Ю. Шевченко //М.: ИКЦ «Академкнига», 2007.- 228 с.: ил.
. Попов В.Н. Сравнительный анализ ключевого фермента глиоксилатного цикла, изоцитратлиазы, из организмов разных систематических групп / В.Н.Попов, Е.А. Москалёв, М.Ю.Шевченко, А.Т. Епринцев // Журнал эволюционной биохимии и физиологии. - 2009. - №6.- С.317-329.
. Филлипович Ю.Б. Основы биохимии. - М.: Высш. шк. 1993.- 496 с.
6. Blackburn P. Ribonuclease inhibitor from human placenta: interaction with derivatives of ribonuclease A / P. Blackburn, B.L. Jailkhani // J Biol Chem. - 2009. - vol. 254. - pp. 12488-93.
. Carpenter W.D. Distributhion and properties of isocitritase in plants/ W.D. Carpenter H. Beevers//Plant Physiol.-2009.-Vol.34,№4.-P.403-409.
. Chomczynski P. Single-step method of RNA isolation by acid guanidinium thiocyanate-phenol-chloroform extraction extraction /P. Chomczynski, N. Sacchi // Anal. Biochem. - 2007. - vol. 162. - pp. 156-159.
. Cioni M. Comparative biochemistry of glyoxylate cycle / M.Cioni, G.Pinzauti, P. Vanni // Comp.Biochem. and Physiol.-1981.- V.70, B, N 1.-P.1-26.
. Cioni M., Comparative biochemistry of isolation by acid guanidinium glyoxylate cycle / M. Cioni, P.Vanni // Comp.Biochem. and Biophis. - 2012, Vol. 70, P. 2621-2629.
. Davis W.L.Cytochemical localization of malate synthase in amphibian fat body adipocytes:possible glyoxylate cycle in a vertebrate / W.L.Davis, R..G.Jones, D.B. Goodman // J.Histochem.Cytochem.-2006.-Vol.34,№5.-P.689-692.
. Davis W.L. Evidence for the glyoxylate cycle in human liver / W.L.Davis, D.B. Goodman // Source Anatomical Record.-1992.-V.234,№4.-P.461-468.
. Firenzuoli A.M. Enzymes of glyoxylate cycle in conifers / A.M.Firenzuoli, P.Vanni, E.Mastronuzzi, A. Zanobini, V.Baccari // Plant Physiol.- 1968.-Vol.43, №7.-Р.1125-1128.
. Gemmrich A.R.Isocitrat lyase in germinating spores of the fern Anemia Phillitia / A.R Gemmrich // Phytochemistry.-2009.-Vol.18,№6.-P.1143-1146.
. High-efficiency cloning of full-length cDNA; construction and screening of cDNA expression libraries for mammalian cells / H. Okayama [et al.] // Methods Enzymol. - 1987. - vol. 154. - pp. 3-28.
. Holmes R.P. The absence of glyoxylate cycle enzymes in rodent and embrione chick liver // Biochim. Biophys. Acta. - 1993. - Vol.233.- P.123-138.
. Jameel S.H., Caenorhabditis elegans: purification of isocitrate lyase and the isolation and cell-free translation of poly (A+) RNA./ S.H. Jameel, B.McFadden //Exp. Parasitol. -1985.- Vol.59.- P.337-346.
. Jones J.D. The glyoxylate cycle: does it function in the dormant or active bear?/ J.D. Jones, P.Burnett, P. Zollman // Comp. Biochem. Phisiol. B.- 1999.- Vol. 124.- P.177-179.
. Kamel M.Y.Biochemical studies of tick embryogenesis. Purification and partial characterization of isocitrate lyase from eggs of the tick.Hyalomma dromedarii / M.Y.Kamel, A.S.Fahmy // Comp.Biochem.Physiol.B/-1982.-Vol.72.-P.107-115.
. Kornberg H.L.Synthesis of cell Constituents from C2-units by a modigied tricarboxylic acid cycle / H.L.Kornberg, H.A.Krebs // Nature.-2007.-Vol.179.-P.988-991.
. Liu F. Bifunctional glyoxylate cycle protein of Gaenorhabditis elegans: a developmentally regulated protein of intestine and muscle. / F. Liu, J.D.Thatcher, J.M. Barral // Dev.Biol.-2012/-Vol.169.-P.399-414.