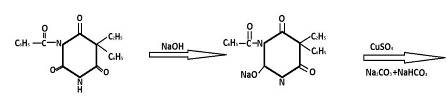
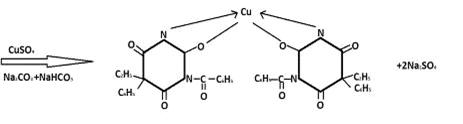
Курсовая работа (т): Хроматографические методы анализа производных барбитуровой кислоты
- метод внешнего стандарта. При применении метода концентрацию испытуемого вещества определяют путём сравнения сигнала (пика), полученного на хроматограммах испытуемого раствора, и сигнала (пика), полученного на хроматограммах раствора стандартного образца.
- метод внутреннего стандарта, который основан на введении в анализируемую смесь определенного количества стандартного вещества (внутренний стандарт);
- метод стандартных добавок.Основан на введении в анализируемую смесь известного количества определяемого вещества и сравнения сигналов, полученных для испытуемого раствора со стандартной добавкой и без добавки определяемого вещества [7].
Порядок проведения качественного и количественного хроматографического анализа закреплен ГФ XIII в статьях:
- ОФС.1.2.1.2.0002.15 «Хроматография на бумаге»;
- ОФС.1.2.1.2.0003.15 «Тонкослойная хроматография»;
- ОФС.1.2.1.2.0004.15 «Газовая хроматография»;
- ОФС.1.2.1.2.0005.15 «Высокоэффективная жидкостная хроматография»;
- ОФС.1.2.1.2.0006.15 «Сверхкритическая флюидная хроматография» [7].
Кратко охарактеризуем сущность этих методов.
Хроматография на бумаге - это хроматографический процесс, протекающий на листе фильтровальной бумаги при перемещении по ее капиллярам и поверхности подвижной фазы.
Тонкослойной хроматографией или хроматографией в тонком слое сорбента называется хроматографический процесс, протекающий при движении подвижной фазы в тонком слое сорбента, нанесенном на инертную твердую подложку (пластинку) из соответствующего материала - стекла, металла или полимера. Тонкослойная хроматография (ТСХ) может использоваться для анализа как однокомпонентных, так и многокомпонентных лекарственных средств. В последнем случае подбираются условия хроматографирования, обеспечивающие разделение компонентов смеси.
Газовая хроматография представляет собой метод разделения летучих соединений, основанный на различии в распределении компонентов анализируемой смеси в системе несмешивающихся и движущихся относительно друг друга фаз, где в качестве подвижной фазы выступает газ (газ-носитель), а в качестве неподвижной фазы - твердый сорбент или жидкость, нанесенная на твердый носитель или внутренние стенки колонки.
Высокоэффективная жидкостная хроматография (жидкостная хроматография высокого давления) является методом колоночной хроматографии, в котором подвижной фазой служит жидкость, движущаяся через хроматографическую колонку, заполненную неподвижной фазой (сорбентом). Колонки для высокоэффективной жидкостной хроматографии характеризуются высоким гидравлическим сопротивлением на входе.
Сверхкритическая флюидная хроматография представляет собой хроматографический процесс, в котором в качестве подвижной фазы используется флюид. Cверхкритический флюид (флюид) - это вещество, находящееся при значениях температуры и давления выше критических. В этом состоянии (сверхкритическом флюидном) свойства вещества являются промежуточными между свойствами газа и жидкости [7].
Говоря о значимости хроматографических методов, специалисты отмечают, что хроматография применяется во всех цивилизованных странах мира в жизненно важных сферах деятельности человека - от исследований в космосе. За вклад хроматографических методов в научные исследования - контроль загрязнений окружающей среды, пищевых продуктов и лекарств - хроматографию отнесли к двадцати выдающимся открытиям двадцатого века. Отдельно отмечается, что метод ВЭЖХ способствовал прогрессу в биохимии, биологии, медицине, фармацевтике [30,31,34].
В литературе также подчеркивается, что метод жидкостной хроматографии применим для разделения значительно более широкого круга веществ, чем газовая хроматография, поскольку большая часть веществ не обладает летучестью, а многие вещества неустойчивы при высоких температурах. В жидкостной хроматографии разделение обычно происходит при комнатной температуре [33].
К числу наиболее востребованных методов в фармацевтическом анализе также относят метод тонкослойной хроматографии (ТСХ) - важный аналитический, физико-химический и микропрепаративный метод, который отличается простотой, высокой экономичностью и универсальностью. Тонкослойная (планарная) хроматография - представляет собой оперативный метод хроматографии для анализа всех классов химических соединений, приобрела значение в качестве экспресс-метода анализа и широко используется в медицине и фармации [5,17].
.2 Хроматографический анализ производных барбитуровой кислоты
В настоящее время в качестве методов хроматографического анализа производных барбитуровой кислоты наибольшее применение находят:
. Тонкослойная хроматография (ТСХ).
. Газожидкостная хроматография (ГЖХ).
. Высокоэффективная жидкостная хроматография (ВЭЖХ) [5,21,26,28].
На стартовую линию хроматографической пластинки «Силуфол» или «Сорбфил» наносят с помощью капилляров в виде точек стандартные (1 мг/мл) хлороформные растворы барбитуратов (барбитал, бармамил, фенобарбитал, этаминал, бензонал, бензобамил) и хлороформное извлечение. Пластинку хроматографируют в системе хлороформ - н-бутанол - 25% раствор аммиака в объемном соотношении 7:4:0,5. Длина пробега фронта растворителей 10 см.
Хроматография в тонком слое сорбента в частной системе растворителей проводится в присутствии «стандартов», в качестве которых используют спиртовые растворы барбитала. Идентифицируют барбитураты на хроматографической пластинке по месторасположению, окраске и значению Rf анализируемого вещества и «стандарта».
Приготовление стандартного раствора барбитуратов: точную навеску барбитурата (50 мг) помещают в мерную колбу на 1000 мл и растворяют ее в 100 мл фосфатного буфера (pH 7,4) при осторожном перемешивании, затем объем жидкости доводят до метки дистиллированной водой. Концентрация барбитурата составляет 50 мкг/мл [1].
Хроматографирование ведут на пластинках с закрепленным слоем силикагеля в системах растворителей:
) хлороформ-ацетон (9:1) - для разделения N - замещенных и 5 5-замещенных производных, система является общей в скрининге лекарственных веществ кислого и нейтрального характера.
) толуол - ацетон - этанол - 25% раствор аммиака (45:45:7,5:2,5) (применяется в экспресс- анализе интоксикаций)
) хлороформ - н-бутанол - 25% раствор аммиака (70:40:5) - в качестве частной системы для разделения 5,5 -замещенных барбитуратов.
Детектирование веществ на хроматограмме проводится двумя реагентами: дифенилкарбазоном (ДФК) и HgSО4. При этом в местах расположения барбитуратов возникают красно- или сине-фиолетовые пятна. Идентификация проводится по величине Rf (отношение длины пробега вещества к длине пробега растворителя). Хроматографирование ведут параллельно метчикам (А), в качестве которых используют хлороформные растворы барбитуратов с известной концентрацией [28].
Применение метчиков наряду с расчетом Rf обусловлено невоспроизводимостью Rf из-за трудности соблюдения стандартных условий при хроматографировании. Чувствительность реакции барбитуратов с ДФК и HgSО4 достигает 0,5 мкг, однако, она неспецифична, поэтому дальнейшее подтверждение присутствия барбитурата производится микрокристаллическими реакциями, исследованием в УФ-области спектра после элюирования вещества с пластинки подходящим растворителем (боратный буфер с рН=10).
Газовая хроматография в сочетании с масс-спектрометрией используется для обнаружения нанограммовых количеств барбитуратов и позволяет вести анализ на фоне эндогенных соединений, выделенных из исследуемого объекта. Для выделения барбитуратов из объекта после гидролиза используют жидкость-жидкостную или твердофазную экстракцию. Концентрирование извлечений проводят упариванием при температуре 40-60°С. Идентифицируют барбитураты по времени удерживания - для барбитала - 5,18 мин [21].
ГЖХ-определение производных барбитуровой кислоты проводят на жидких фазах типа SE-30 или OV-17. Используют ступенчатый температурный режим колонки 180°С; 200°С - для барбитала, барбамила, нембутала; 230°С - для фенобарбитала или другие варианты программирования. Температура испарителя - 250 С. Для подготовки пробы в образец вводят серную кислоту в дозе 0,25 моль, такой же объем очищенного хлороформа. Смесь центрифугируют при 8000 об./мин. На анализ отбирают 1-5 мкл хлороформного извлечения.
При применении ГЖХ-анализа для обнаружения барбитала используют индекс удерживания 1490, фенобарбитала - 1974.
ВЭЖХ при обнаружении барбитуратов применяется в токсикологическом анализе. Барбитураты извлекают из биологических объектов при рН=1-2 хлороформом, смесью хлороформ - изопропанол 9:1 или диэтиловым эфиром. Предварительно рекомендуется при анализе мочи провести кислотный гидролиз для разрушения метаболитов - глюкуронидов [12].
Для обнаружения с помощью ВЭЖХ рекомендованы следующие условия: хроматограф «Милихром», хроматографическая колонка (62x2 мм), заполненная обращенно-фазовым сорбентом «Сепарон» С,8 (5 мкм), подвижная фаза - смесь 0,05 М водного раствора гидрофосфата аммония и метанола (60:40), скорость элюирования равна 100 мкл) мин. Сухой остаток растворяют в 100 мкл подвижной фазы и вводят в хроматограф 4 мкл.
Для обнаружения барбитуратов в исследуемой пробе
сравнивают время (объем) удерживания и коэффициент емкости определяемого
вещества с образцом сравнения в тех же условиях; сравнивают УФ-спектры
поглощения с образцом сравнения, а также сопоставляют УФ-спектры исследуемого
компонента и образца сравнения при 2 и более длинах волн и оценивают их
спектральные отношения (табл. 4) [12].
Таблица 4 Хроматографические характеристики производных барбитуровой кислоты, полученные с помощью «Милихром А-02»
|
Барбитурат |
Объем VR, мкл |
Спектральные отношения (S/S210) |
||||||
|
|
|
220 |
230 |
240 |
250 |
260 |
280 |
300 |
|
Барбитал |
933 |
0,615 |
0,088 |
0,027 |
0,010 |
0,007 |
0,000 |
0,001 |
|
Фенобарбитал |
1394 |
0,506 |
0,194 |
0,113 |
0,062 |
0,039 |
0,003 |
0,000 |
Сухой остаток, полученный при изолировании по методу В.А.Карташова и содержащий вещества кислотного характера, растворяют в небольшом объеме хлороформа и количественно наносят на стартовую линию хроматографической пластинки. По краям стартовой линии наносят хлороформные растворы «стандартов» (дифенин и тиопентал).
Условия анализа. Система растворителей: ацетон - н-гексан - диэтиламин (10:10:1). После высушивания пластинку обрабатывают раствором сульфата ртути. Вещества кислотного характера проявляются в виде полосы, а «стандарты» - в виде пятен белого цвета [16].
По полученным данным вещество относят к одной из трех хроматографических
групп (табл. 5).
Таблица 5 Хроматографические группы веществ кислотного характера (производные барбитуровой кислоты)
|
1 группа |
2 группа |
3 группа |
|
Фенобарбитал |
Барбамил Барбитал Этаминал-натрий |
Тиопентал |
.3 Анализ таблеток фенобарбитала, 100 мг (ОАО «Татхимпрепараты»)
.3.1 Реакции идентификации
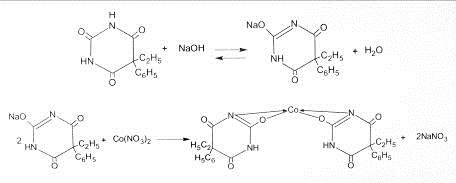
0,1 г растертых таблеток взбалтывают с 2 мл спирта 96 %, прибавляют 1
каплю 20% раствора кальция хлорида, 2 капли 5 % раствора кобальта нитрата и 2
капли 20 % раствора натрия гидроксида; появляется сине-фиолетовое окрашивание
[29].
2.3.2 Количественное определение
Около 0,2 г (точная навеска) субстанции растворяют в 5 мл предварительно нейтрализованного по тимолфталеину спирта 96%, прибавляют 5 мл воды и титруют 0,1 М раствором натрия гидроксида до появления синего окрашивания (индикатор - 0,5 мл 0,1 % раствора тимолфталеина) [29].
Параллельно проводят контрольный опыт.
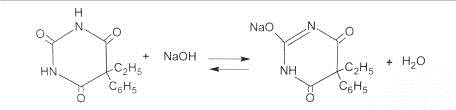
мл 0,1 М раствора натрия гидроксида соответствует 23,22 мг фенобарбитала C12H12N2O3.
.3.3 Хроматографический анализ
Определение проводят методом тонкослойной хроматографии (ТСХ) [1].
Испытуемый раствор. 0,1 г субстанции растворяют в 5 мл спирта 96 %.
Раствор сравнения А. 0,5 мл испытуемого раствора разбавляют спиртом 96 % до 100 мл.
Раствор сравнения Б. 25 мл раствора сравнения А разбавляют спиртом 96 % до 50 мл.
Раствор для проверки пригодности хроматографической
системы.
15 мл раствора сравнения Б разбавляют спиртом 96 % до 25 мл.
Подвижная фаза. Готовят смесь: аммиака раствор концентрированный 25 % - спирт 96 % - хлороформ (5:15:80). Дают смеси отстояться до разделения слоев и в качестве элюента используют нижний слой [29].
Раствор используют свежеприготовленным.
На линию старта пластинки Силикагель 60 F254, предварительно промытой метанолом и высушенной при температуре от 80 до 85 °C в течение 7 мин, наносят по 10 мкл испытуемого раствора (200 мкг), раствора сравнения А (1 мкг), раствора сравнения Б (0,5 мкг) и раствора для проверки пригодности хроматографической системы (0,3 мкг). Пластинку с нанесенными пробами сушат в токе теплого воздуха в течение 5 мин, помещают в камеру с подвижной фазой и хроматографируют восходящим способом. Когда фронт подвижной фазы пройдет около 80-90 % длины пластинки от линии старта, ее вынимают из камеры и немедленно просматривают в УФ-свете при длине волны 254 нм. После этого пластинку опрыскивают дифенилкарбазон-ртутным реактивом, сушат в токе теплого воздуха в течение 5 мин и опрыскивают свежеприготовленным 0,66 % спиртовым раствором калия гидроксида. Пластинку нагревают при температуре от 100 до 105 °C в течение 5 мин и немедленно просматривают.
Любое дополнительное пятно на хроматограмме испытуемого раствора при просмотре в УФ-свете и после проявления не должно превышать по величине и интенсивности поглощения или окраски пятна на хроматограмме раствора сравнения А (не более 0,5 %).
Предел обнаружения: 1 мкг анализируемого соединения.
Суммарное содержание примесей - не более 0,75 %.
Вывод: лекарственная форма «Таблетки фенобарбитала 0,1» удовлетворяют
требованиям фармакопейной статьи «Фенобарбитал. ФС 2.1.0041.15» [29].
2.4 Анализ таблеток бензонала 100 мг (ОАО «Татхимпрепараты»)
.4.1 Реакции идентификации
В связи с отсутствием изменений в ГФ XIII и ГФ XII в силе остается статья 92 «Бензонал» ГФ X [8].
. 0,1 г препарата растворяют в 2 мл спирта при нагревании на водяной
бане, прибавляют 1 каплю раствора хлорида кальция, 2 капли раствора нитрата
кобальта и 1 каплю раствора едкого натра; появляется сине-фиолетовое
окрашивание.
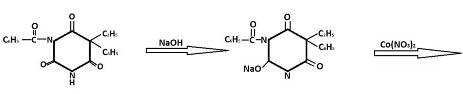
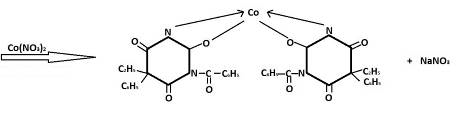
. К 0,2 г препарата прибавляют 10 капель 1% раствора едкого натра, 0,2 мл
раствора гидрокарбоната и карбоната калия, 0,1 мл раствора сульфата меди и
тщательно перемешивают; появляется серо-голубое окрашивание [8].