Курсовая работа (т): Хроматографические методы анализа производных барбитуровой кислоты
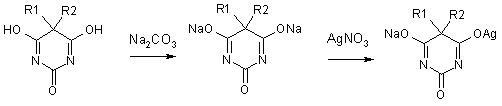
Однозамещенная серебряная соль при добавлении избытка
нитрата серебра превращается в нерастворимую двузамещенную серебряную соль:
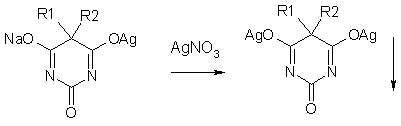
Гексенал и бензонал, содержащие заместители в положении 1, образуют только однозамещенные соли серебра [16].
. Мурексидная проба. Раствор исследуемого вещества в
этиловом спирте помещают в фарфоровую чашку, спирт осторожно испаряют, к
остатку добавляют 0,1 мл раствора хлорида аммония, содержащего следы соли Мора,
и 0, 1 мл 30% раствора перекиси водорода. Реакционную смесь перемешивают и
чашку нагревают на спиртовке. Через 5 минут по краям сухого остатка появляется
розовое или красное окрашивание. Окрашивание становится интенсивнее при
нанесении на остаток капли 25% раствора аммиака.
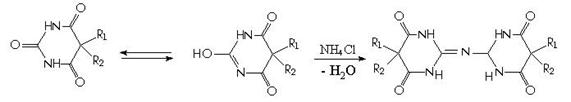
Чувствительность реакции различна для каждого из барбитуратов. В среднем она составляет 3-5 мг вещества в пробе.
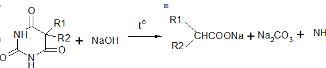
. Сплавление со щелочью. Все барбитураты при сплавлении со щелочами
выделяют аммиак. При сплавлении с NaOH молекулы барбитуратов разрушаются, образуя соли соответствующих
дизамещенных производных ацетатной кислоты, аммиак NH3 и натрия карбонат Na2CO3 .
Для натриевых солей используется реакция осаждения кислотной формы
барбитуратов.

Выпавший осадок барбитурата отфильтровывают, промывают водой, сушат и определяют его температуру плавления [8].
. Реакция выделения кислотной формы барбитуратов. На предметное стекло
наслаивают несколько капель хлороформного раствора исследуемого вещества,
удаляя хлороформ при комнатной температуре. Следующую каплю наносят после
испарения предыдущей. Сухой остаток растворяют в капле концентрированной серной
кислоты. Через 3-5 минут рядом с этой каплей помещают одну каплю
дистиллированной воды, после чего их осторожно соединяют при помощи капилляра
[12]. Через 10-20 минут наблюдают появление кристаллического осадка,
характерного для каждого отдельного барбитурата (рис. 1-4).
Кристаллы кислотной формы
Кристаллы кислотной формы барбитала фенобарбитала

Кристаллы кислотной
Кристаллы кислотной формы барбамила. формы бутобарбитала
5. УФ-спектрофотометрия основана на способности барбитуратов к
лактам-лактимной таутомерии [12].
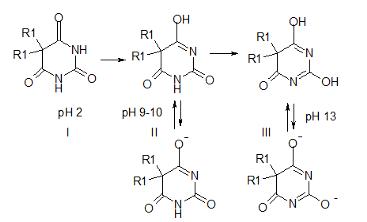
Отсутствие поглощения растворов при рН=2 и появление максимума при рН=10
и λ = 239-240 нм подтверждает
присутствие барбитуратов (рис. 5) [16].
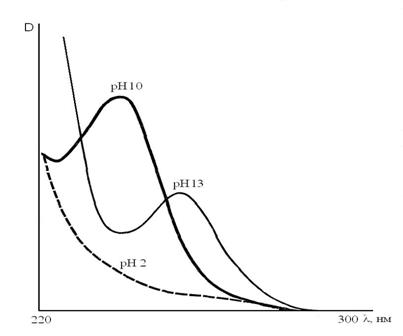
Спектры поглощения производных барбитуровой кислоты в зависимости от pH раствора
. ИК-спектры производных барбитуровой кислоты имеют характеристические
частот при λ = 1712-1720 см-1 (С = О - валентные колебания) и при λ = 1210-1245 см-1 (- С = О -
деформационные колебания), при λ = 1680 -1693 см-1 (-NH - деформационные колебания) [12].
1.4.2 Частные реакции на производные барбитуровой кислоты
1. Реакция нитрования (на фенильный радикал -C6H5) (фенобарбитал и бензонал). При нагревании препарата,
содержащего в молекуле бензольный цикл, с концентрированной сульфатной кислотой
H2SO4 и раствором натрий нитрата NaNO3 (или смесью конц. HNO3 и H2SO4) происходит нитрование в
мета-положение с образованием нитропроизводного желтого цвета [8].
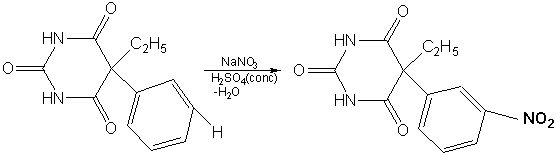
Гексенал образует без повторного нагревания на границе двух слоев буровато-красное кольцо с зеленоватой флюоресценцией.
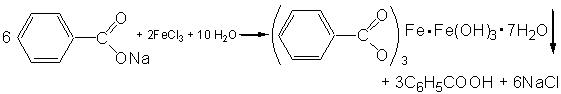
. Реакция на бензоат-ион после щелочного гидролиза
препарата (бензонал) - реакция с хлоридом железа (III). Предварительно препарат
взбалтывают с раствором гидроксида натрия и фильтруют. Образующийся при
гидролизе бензонала бензоат-ион переходит в фильтрат. Он образует с ионом
железа (III) розовато-желтый осадок [8].
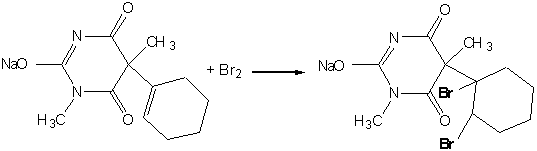
. Реакция на двойную связь (гексенал) - обесцвечивание
раствора калий перманганата KMnO4
или бромной воды Br2.
. Реакция на атом серы (тиопентал-натрий).
.1. При кипячении препарата с раствором щелочи в
присутствии ацетата свинца образуется осадок сульфида свинца и ощущается запах
аммиака. При последующем подкислении разведенной соляной кислотой выделяется
сероводород [8,16].
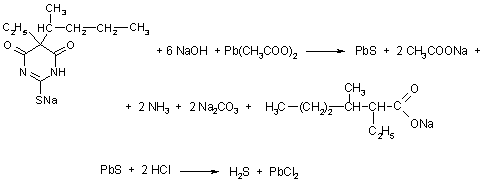
.2. При минерализации препарата смесью для спекания (смесь Na2CO3 и NaNO3) сера переходит в анионы SO42-, которые выявляют раствором BaCl2:
SO42-
+ Ba2+ → BaSO4↓
белый осадок
. Кристаллические реакции. Реакция с хлорцинкйодом [12]. На остаток
исследуемого вещества на предметном стекле (после удаления хлороформа) наносят
каплю раствора хлорцинкйода. Через 10-15 минут под микроскопом наблюдают
образование кристаллических осадков. Если осадок долго не образуется, к каплям
на предметных стеклах добавляют 1-2 кристалла йода и препараты снова через
10-15 минут рассматривают под микроскопом (рис. 6).

Кристаллы продукта взаимодействия барбитала с раствором хлорцинкйода
Барбитал с хлорцинкйодом образует прямоугольные пластинки темно-красного, зеленого, фиолетового, серо-розового цветов [15].
.5 Методы количественного анализа лекарственных средств, производных барбитуровой кислоты
. Алкалиметрия в неводной среде. Метод применяется для количественного определения барбитала, фенобарбитала, бензонала [1,7].
Навеску препарата растворяют в смеси диметилформамида (ДМФА) и бензола С6Н6 (1:3), предварительно нейтрализованной по тимоловому синему в ДМФА (протофильный растворитель, усиливает кислотные свойства барбитуратов) и титруют раствором метилата натрия CH3ONa или раствором гидроксида натрия NaOH в смеси метанола CH3OH и бензола C6H6 до появления синего окрашивания [12].
Метод базируется на способности барбитуратов к таутомерным превращениям и образованием имидольной или аци-формы, имеющей кислотный характер, по схеме:
fэ = 1
.1. Схема реакции при использовании в качестве
титранта раствора метилата натрия:
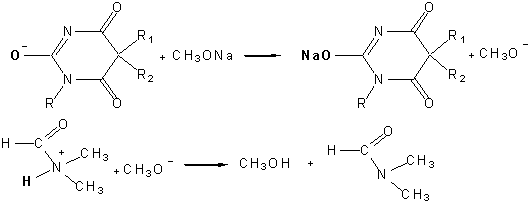
.2. Схема реакции при использовании в качестве
титранта раствора гидроксида натрия в смеси метанола и бензола:
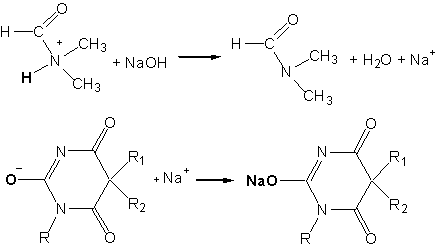
. Алкалиметрия в водно-спиртовой среде. Метод пригоден
для количественного определения любого барбитурата, имеющего кислотный характер
[12]. В качестве титранта используют раствор натрий гидроксида NaOH, а индикатора - тимолфталеин [6,7].
Навеску препарата растворяют в нейтрализованном по тимолфталеину в спирте
С2Н5ОН (для улучшения растворимости барбитуратов и предупреждения гидролиза
образовавшейся натриевой соли).
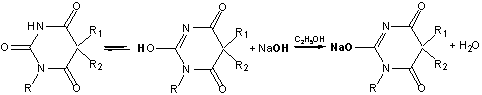
. Аргентометрический метод. Способ прямого титрования.
Основан на количественном взаимодействии производных пиримидин-2,4,6-триона
(барбитуратов) с серебра нитратом, с образованием растворимых однозамещённых
серебряных солей. Во внутриаптечном контроле определение обычно проводят в
среде натрия карбоната или тетрабората, индикация осуществляется по появлению
устойчивой мути - осадка двузамещённой серебряной соли (титрование без
индикатора) [9]. Навеску субстанции (кислотной или солевой формы) растворяют в
5 % растворе безводного натрий карбоната Na2CO3 и титруют
раствором аргентум нитрата AgNO3
без индикатора по появления неисчезающей мути (двухзамещенная Ag-соль), что указывает на конец
титрования. fэ = 1/2.
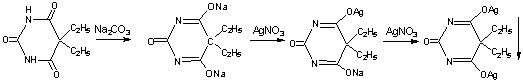
При определении в присутствии индикатора калия хромата (среда слабощелочная) сначала осаждается двузамещённая серебряная соль, затем избыточная капля титранта реагирует с индикатором, образуя осадок кирпично-красного цвета [8].
4. Меркуриметрия обратная [9]. Титрант - водный
раствор Hg(NO3)2. В результате реакции образуется осадок барбитурата ртути (II), его отфильтровывают, а в фильтрате
комплексонометрически оттитровывают избыток нитрата ртути (II). fэ = 1.
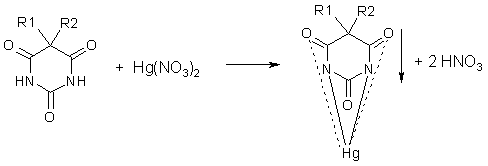
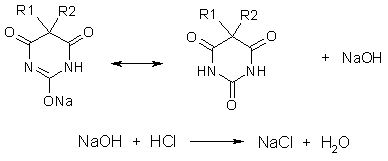
. Ацидиметрия в водной среде. Метод пригоден для количественного определения натриевых солей барбитуратов, имеющих основный характер (барбитал-натрий, барбамил, гексенал) [12]. В качестве титранта используют раствор HCl, а индикатора - метиловый оранжевый или метиловый красный. Na-соли барбитуратов способны гидролизовать в водных растворах, образуя щелочную среду и поэтому их можно оттитровать кислотами в присутствии метилового оранжевого или метилового красного. fэ = 1.

При этом титруется кислотой и свободная щелочь NaOH, возникающая при гидролизе
препарата:
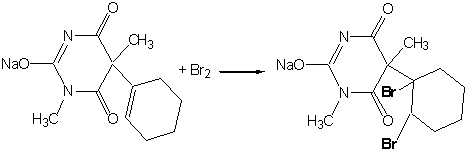
. Броматометрия, обратное титрование, с
йодометрическим окончанием [22]. Метод используется для количественного
определения барбитуратов с ненасыщенной связью, например, гексенала. Метод
основан на бромировании субстанции по месту двойной связи. fэ = 1/2.
KBrO3 + 5KBr +
6HCl → 3Br2 + 6KCl + 3H2O
+ 2KI = I2 + 2KBr+ 2Na2S2O3 = 2NaI + Na2S4O6
Параллельно проводят контрольный опыт.
. Гравиметрия. Гравиметрический метод обычно применяют
для количественного определения Na-солей барбитуратов (например, тиопентал-натрий),
а также при анализе лекарственных смесей. Суть метода состоит в том, что к
водному раствору препарата прибавляют разбавленную хлоридную кислоту HCl [2].
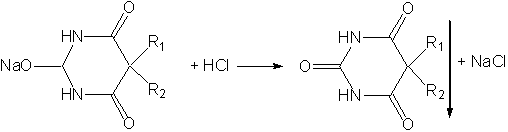
Полученную кислотную форму экстрагируют хлороформом (5 раз небольшими порциями). Все хлороформные извлечения соединяют, хлороформ отгоняют, а остаток сушат при 70°С до постоянной массы и взвешивают [12].
.6 Хранение и применение лекарственных средств, производных барбитуровой кислоты
Лекарственные средства, производные барбитуровой кислоты хранят в соответствии с требованиями постановления Правительства № 1148 «О порядке хранения наркотических и психотропных веществ» хранят в хорошо укупоренной таре, в сухом защищенном от света месте. В хорошо укупоренной таре. Гигроскопичные препараты - в сухом, прохладном, защищенном от света месте [15].
Фенобарбитал и бензонал - в банках темного стекла, в защищенном от света месте.
Гексенал и тиопентал-натрий - в стеклянных флаконах по 0,5-1,0 г, которые герметически закрыты резиновыми пробками, обтянуты алюминиевыми колпачками; в сухом, прохладном, защищенном от света месте. В качестве стабилизатора к гексеналу прибавляют 0,05-0,25 % NaOH, к тиопентал-натрию - 5-6 % натрий карбоната Na2CO3.
Водные растворы Na-солей барбитуратов легко гидролизуются, поэтому их готовят на физиологическом растворе в асептических условиях непосредственно перед употреблением (ex tempore).
Лекарственные средства изучаемой группы применяют как седативные и снотворные средства:
- длительного действия - барбитал, фенобарбитал, барбитал-натрий;
- средней продолжительности - барбамил;
- кратковременнго действия - гексенал, тиопентал-натрий;
В качестве противоэпилептических (противосудорожных) средств используют фенобарбитал и бензонал, при этом последний снотворного действия не имеет [19].
Гексенал и тиопентал-натрий используются для вводного, интравенозного
наркоза. При длительном применении и повышенных дозах барбитуратов может быть
отравление,
поэтому их применение должно контролироваться врачом.
ГЛАВА 2. АНАЛИЗ ЛЕКАРСТВЕННЫХ ФОРМ, СОДЕРЖАЩИХ ПРОИЗВОДНЫЕ БАРБИТУРОВОЙ КИСЛОТЫ
.1 Общая характеристика хроматографических методов анализа
В фармацевтической химии широкое распространение получили методы анализа, сочетающие в себе разделение и количественное определение веществ. В качестве одной из основных групп такого анализа можно выделить хроматографические методы.
Существует ряд определений сущности методов хроматографии. Рассмотрим основные из них.
Согласно определению международной комиссией ИЮПАК в 1993 г. хроматография представляет собой физический метод разделения, в котором разделяемые компоненты распределены между двумя фазами, одна из которых является неподвижной (стационарная или неподвижная фаза), в то время как другая (подвижная фаза) движется в определенном направлении [20]. Следует подчеркнуть, что это определение сводит хроматографию только к физическому методу разделения, а это сужает область ее применения.
Существует точка зрения, что термин «хроматография» имеет три смысла:
- наука о межмолекулярных взаимодействиях и переносе молекул или частиц в системе несмешивающихся и движущихся относительно друг друга фаз;
- процесс дифференцированного многократного перераспределения веществ или частиц между несмешивающимися и движущихся относительно друг друга фазами, приводящий к обособлению концентрационных зон индивидуальных компонентов исходных смесей этих веществ или частиц;
- метод разделения смесей веществ или частиц, основанный на различии в скоростях их перемещения в системе несмешивающихся и движущихся относительно друг друга фаз [24].
Хроматографический метод представляет собой метод разделения веществ, в основе которого лежит разница в коэффициентах распределения этих веществ между неподвижной и подвижной фазами [3].
В настоящее время, по оценкам специалистов хроматография представляет собой:
- самый распространенный и совершенный метод разделения лекарственных смесей;
- уникальный метод качественного и количественного анализа сложных многокомпонентных смесей [11,22,27].
В соответствии с ОФС.1.2.1.2.0001.15 «Хроматография» Государственной фармакопеи Российской Федерации XIII издания хроматографией называется метод разделения смесей веществ, основанный на их многократном перераспределении между двумя контактирующими фазами, одна из которых неподвижна, а другая имеет постоянное направление движения. По механизму, лежащему в основе разделения, различают адсорбционную, распределительную, ионообменную и другие виды хроматографии [7].
Говоря о количественном анализе, необходимо отметить, что в ГФ XIII издания закреплено применение в фармацевтическом анализе четырех основных методов расчета концентрации анализируемого вещества по хроматографическим данным, в том числе:
- метод нормирования (метод внутренней нормализации). Применение данного метода основано на предположении, что на хроматограмме зарегистрированы все вещества, входящие в состав анализируемой смеси, и что доля площади (высоты) каждого пика от суммы площадей (высот) всех пиков соответствует содержанию вещества в массовых процентах;