Курсовая работа (т): Хроматографические методы анализа производных барбитуровой кислоты
Хроматографические методы анализа производных барбитуровой кислоты
«БЕЛГОРОДСКИЙ ГОСУДАРСТВЕННЫЙ НАЦИОНАЛЬНЫЙ ИССЛЕДОВАТЕЛЬСКИЙ УНИВЕРСИТЕТ» (НИУ «БелГУ»)
МЕДИЦИНСКИЙ ИНСТИТУТ
Кафедра фармацевтической химии и
фармакогнозии
Курсовая работа
Хроматографические методы анализа
производных барбитуровой кислоты
Белгород 2017
ОГЛАВЛЕНИЕ
ВВЕДЕНИЕ
ГЛАВА 1. ОБЩАЯ ХАРАКТЕРИСТИКА ЛЕКАРСТВЕННЫХ СРЕДСТВ, ПРОИЗВОДНЫХ БАРБИТУРОВОЙ КИСЛОТЫ
.1 Химическое строение и стереометрия
.2 Способы получения лекарственных средств, производных барбитуровой кислоты
.3 Физические свойства лекарственных средств, производных барбитуровой кислоты
.4 Методы качественного анализа лекарственных средств, производных барбитуровой кислоты
.4.1 Общие реакции идентификации
.4.2 Частные реакции на производные барбитуровой кислоты
.5 Методы количественного анализа лекарственных средств, производных барбитуровой кислоты
.6 Хранение и применение лекарственных средств, производных барбитуровой кислоты
ГЛАВА 2. АНАЛИЗ ЛЕКАРСТВЕННЫХ ФОРМ, СОДЕРЖАЩИХ ПРОИЗВОДНЫЕ БАРБИТУРОВОЙ КИСЛОТЫ
.1 Общая характеристика хроматографических методов анализа
.2 Хроматографический анализ производных барбитуровой кислоты
.3 Анализ таблеток фенобарбитала, 100 мг (ОАО «Татхимпрепараты»)
.3.1 Реакции идентификации
.3.2 Количественное определение
.3.3 Хроматографический анализ
.4 Анализ таблеток бензонала 100 мг (ОАО «Татхимпрепараты»)
.4.1 Реакции идентификации
.4.2 Количественное определение
.4.3 Хроматографический анализ
.5 Анализ порошка тиопентала натрия, 500 мг (ОАО «Синтез»)
.5.1 Реакции идентификации
.5.2 Количественное определение
ВЫВОДЫ
СПИСОК ЛИТЕРАТУРЫ
ВВЕДЕНИЕ
барбитуровый кислота хроматографический лекарственный
В настоящее время на фармацевтическом рынке широко распространены комбинированные лекарственные средства барбитуратов с другими веществами, такими как кофеин, ацетилсалициловая кислота, эфедрин, теофиллин, кодеин, диазепам. В незаконном обороте наркотиков нередки случаи использования барбитуратов в смеси с героином, кокаином, амфетаминами, а также алкоголем. Производные барбитуровой кислоты, являясь агонистами рецепторов гамма-аминомасляной кислоты, оказывают различные виды действия на ЦНС - от легкого седативного до общей анестезии. Прием их может вызвать эйфорию, подобную морфиновой, но они практически не обладают болеутоляющим свойством [15].
Определение производных барбитуровой кислоты актуально как при анализе качества лекарственных средств, так и при токсикологическом анализе, так как их используют не только как седативно-снотворные, но и как наркотические средства.
Физико-химические методы анализа наиболее часто используются для решения диагностических и идентификационных задач при исследовании подлинности лекарств, в частности наркотических средств. Качественный хроматографический анализ, то есть идентификация вещества по его хроматограмме, занимает весомое место при анализе лекарственных средств. Хроматография - один из наиболее перспективных в настоящее время методов разделения и анализа веществ, используемый в различных отраслях аналитической химии. Основы метода были заложены М.С. Цветом для разделения сложной смеси растительных пигментов из листьев зеленых растений. Бурное развитие методов хроматографического анализа началось во второй половине XX века [32]. С 1961 года хроматография используется для анализа лекарственных средств. В ряде случаев метод тонкослойной хроматографии (ТСХ) является наиболее точным по сравнению с предшествующими методами, так как его реализация позволяет надежно дифференцировать и идентифицировать сложные смеси веществ, содержащих смеси барбитуровой кислоты.
Цель работы - изучение основных хроматографических методов анализа лекарственных форм, содержащих производные барбитуровой кислоты на основе литературных источников.
Для достижения поставленной цели необходимо решить следующие задачи:
- изучить строение и физико-химические свойства лекарственных средств, производных барбитуровой кислоты;
- охарактеризовать методы качественного и количественного анализа лекарственных средств, производных барбитуровой кислоты, исходя из их строения;
- рассмотреть основные хроматографические методы, используемые при анализе барбитуратов;
- провести анализ лекарственных форм, содержащих лекарственных
средств, производных барбитуровой кислоты.
ГЛАВА 1. ОБЩАЯ ХАРАКТЕРИСТИКА ЛЕКАРСТВЕННЫХ СРЕДСТВ, ПРОИЗВОДНЫХ БАРБИТУРОВОЙ КИСЛОТЫ
.1 Химическое строение и стереометрия
Производные барбитуровой кислоты представляют собой синтетические
препараты, содержащие в основе гексагидропиримидиновый цикл с тремя
оксогруппами =С=О в положении 2,4,6 -:
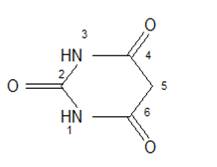
Производные барбитуровой кислоты способны проявлять лактим-лактамную
таутомерию (за счет водородов имидных групп) [12].
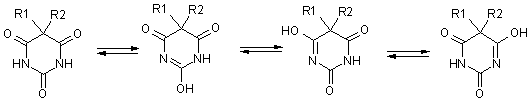
Первая группа - барбитураты - имеют лактамную форму, вторая - соли
барбитуратов - лактимную форму. Общие формулы этих групп могут быть
представлены следующим образом [4,12]:

барбитураты натриевые соли барбитуратов
Лактимная или аци-форма обусловливает кислый характер производных
барбитуровой кислоты. В присутствии гидроксид-ионов они диссоциируют как
кислоты и образуют соли с металлами:
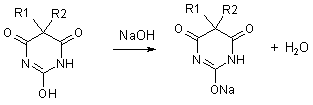
Основные производные барбитуровой кислоты, применяемые в качестве
лекарственных средств, различаются по характеру радикалов R, R1, R2.
Характеристика радикалов приведена в таблице 1 [8,12,29].
Таблица 1 Характеристика радикалов, входящих в химическую структуру производных барбитуровой кислоты
|
Лекарственное средство |
Радикалы |
||
|
|
R1 |
R2 |
R |
|
Барбитал |
-C2H5 |
-C2H5 |
- |
|
Фенобарбитал |
-C2H5 |
-C6H5 |
- |
|
Бензобарбитал (бензонал) |
-C2H5 |
-C6H5 |
|
|
Барбитал-натрий |
-C2H5 |
-C2H5 |
- |
|
Гексобарбитал-натрий (гексенал) |
-CH3 |
|
-CH3 |
|
Тиопентал-натрий |
-C2H5 |
-СН-СН2-СН2-СН3 | СН3 |
- |
Снотворное действие барбитуратов впервые было обнаружено в начале ХХ века Е. Фишером и Ф. Мерингом. В 1904 г. Е. Фишер получил барбитал (веронал), а потом были синтезированы многие барбитураты и установлена связь между структурой и действием на организм [16].
. Снотворное действие проявляют производные барбитуровой кислоты, которые в положении 5,5 содержат алкильные, арильные либо другие радикалы.
. Сила и время действия барбитуратов увеличивается при увеличении длины углеводородного скелета в алкильном заместителе в положении 5,5 до пяти-шести атомов углерода. Дальнейшее увеличение длины карбонового (углеродного) скелета приводит к возникновению возбуждающего действия.
. Разветвление карбонового скелета, наличие ненасыщенных связей, спиртового гидроксила -ОН, атома галогена (особенно Br) усиливает фармакологический эффект.
. Повышение действия барбитуратов, как правило, сопровождается сокращением длительности снотворного эффекта.
Наличие одного фенильного C6H5- радикала в положении 5 усиливает действие, не изменяя длительности действия, а введение второго фенильного радикала снижает снотворный эффект [12].
. Введение алкильного радикала в одну из имидных групп (положение 1, 3) сокращает время действия препаратов.
. Замена гидрогена в положении 1 остатком ароматической кислоты (например, бензойной) придает препарату противоэлептическое действие (препарат бензонал).
. При одновременном замещении атомов Н имидных групп в положении 1 и 3 возникает способность вещества вызывать судороги.
. Производные тиобарбитуровой кислоты (в положении 2 содержит атом серы) проявляют более сильное и кратковременное действие по сравнению с оксигенсодержащими аналогами [16].
1.2 Способы получения лекарственных средств, производных барбитуровой кислоты
Барбитураты могут быть получены из 1,3-дикарбонильного соединения по двум схемам:
схема:
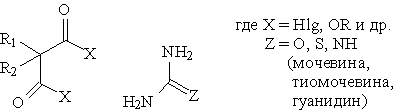
Обычно исходными веществами являются соответствующий диалкилмалоновый
эфир и мочевина [16]:
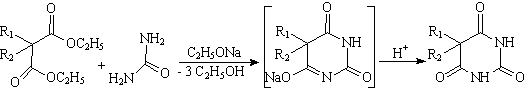
Конденсация (N-ацилирование аминогрупп мочевины) идет в среде
абсолютированного этанола в присутствии этилата натрия при кипячении массы в
аппарате с обратным холодильником. Этилат натрия повышает нуклеофильность
мочевины:
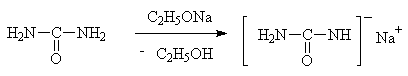
Процесс ведут в сухой аппаратуре, для предотвращения разложения этилата натрия и гидролиза исходного эфира. Выход достигает 85-90% от теории.
Первая схема синтеза барбитуратов применяется в производстве барбитала, барбамила, этаминала-натрия. Она экономически выгодна вследствие простоты производства и применения дешевой мочевины [12].
Схема синтеза барбитала выглядит следующим образом:
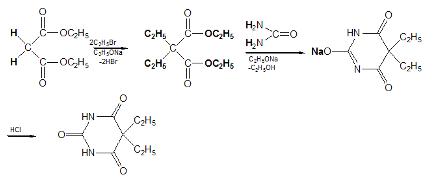
Первая схема применяется и для синтеза производных тиобарбитуровой кислоты, например, тиопентала-натрия конденсацией этил-(втор.пентил)-малонового эфира с тиомочевиной [12].
схема получения барбитуратов:
Обычно субстратами являются соответствующий диалкилциануксусный эфир -
ЦУЭ (этилового эфира циануксусной кислоты) и дициандиамид (цианогуанидин),
однако возможны и другие комбинации. Схема более сложная, так как требуется
дополнительная обработка продуктов конденсации для превращения их в барбитураты
[23].
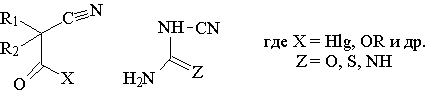
Конденсацию соответствующих производных циануксусного эфира с
дициандиамидом ведут в присутствии этилата (или метилата) натрия в среде
метанола:
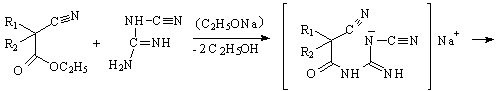
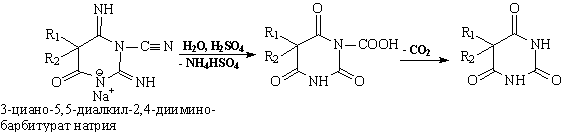
Конденсация начинается с ацилирования наиболее нуклеофильной аминогруппы дициандамида. Затем к тройной связи нитрила присоединяется нуклеофил. Образующуюся соль 5,5-диалкил-3-циано-2,4-дииминобарбитуровой кислоты кипятят с водным раствором серной кислоты. При этом нитрильная и иминогруппы гидролизуются, а образовавшаяся карбоксигруппа декарбоксилируется [16].
Конденсация по второй схеме идет в более мягких условиях (температура
может быть в пределах 8-12оС). Это объясняется более высокой нуклеофильностью
аминогруппы дициандиамида по сравнению с мочевиной и большей легкостью
протекания стадии циклизации в данном случае вследствие более высокой
кислотности фрагмента
![]()
по сравнению с фрагментом
![]()
и, соответственно, более высокой концентрации аниона:
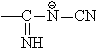
Другой особенностью является проведение конденсации не в этаноле, а в метаноле, в котором дициандиамид растворяется лучше [23].
Вторая схема более сложна, менее экономична, чем первая; используются более токсичные виды сырья (метанол, органические цианистые соединения), высокий расход кислоты на стадии гидролиза. Однако производные циануксусного эфира более доступны, чем малонового эфира. Вторая схема получения барбитуратов применяется в производстве циклобарбитала, гексенала, фенобарбитала.
.3 Физические свойства лекарственных средств, производных барбитуровой кислоты
Русские, латинские и химические названия, а также строение и физические
свойства лекарственных средств, производных барбитуровой кислоты представлены в
таблице 2 [8,12,29].
Таблица 2 Строение и физические свойства лекарственных средств, производных барбитуровой кислоты
|
Лекарственное средство |
Химическая структура |
Описание |
|
|
Барбитал Barbitalum |
|
Белый кристаллический порошок, без запаха, горького вкуса. tплав =189-191°С Малорастворим в воде и спирте, легко растворим в щелочах |
|
|
Фенобрбитал Phenobarbitalum |
|
Белый кристаллический порошок без запаха, горького вкуса. tплав =174-178 °С. Очень мало растворим в холодной воде, трудно растворим в кипящей воде, легко растворим в спирте и щелочах |
|
|
Бензобарбитал (бензонал) Benzonalum |
|
Белый кристаллический порошок, горького вкуса. tплав =134-137 °С. Очень мало растворим в воде, трудно растворим в спирте, легко растворим в хлороформе, растворим в эфире |
|
|
Барбитал-натрий Barbitalum-Natrium |
|
Белый кристаллический порошок без запаха, горького вкуса. Водный раствор имеет щелочную реакцию. Легко растворим в воде, мало растворим в спирте, практически нерастворим в эфире |
|
Гексобарбитал-натрий (гексенал) Hexobarbitalum-
Natrium (Hexenalum) 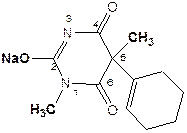

|
натрия 1,5-диметил-5-(циклогекс-1¢-енил)-барбитурат натрияБелая пенообразная масса, на воздухе от CO2 разлагается. Гигроскопичен. Очень легко растворим в воде и спирте; практически нерастворим в эфире и хлороформе |
|
|
|
Тиопентал-натрий Thiopentalum-Natrium |
|
1.4 Методы качественного анализа лекарственных средств, производных барбитуровой кислоты
.4.1 Общие реакции идентификации
1. Производные барбитуровой кислоты образуют нерастворимые соли с ионами тяжелых металлов - серебра, ртути (II), меди (II), кобальта (II). Эта реакция происходит только с ионизированной формой препарата, поэтому кислотную форму предварительно необходимо перевести в ионную [8]. Однако при этом нельзя допускать избытка щелочи, так как он при последующем выполнении реакции приведет к образованию гидроксидов металлов [12].
.1. С ионом кобальта в присутствии солей кальция образуются комплексные соединения, окрашенные в сине-фиолетовый цвет (в присутствии хлорида кальция) [8].
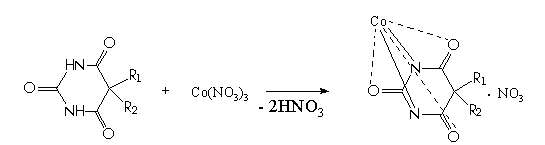
.2. Цветная реакция с раствором сульфата меди (II) (на
примере барбитала):
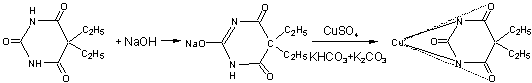
Схема взаимодействия производных барбитуровой кислоты
и ионов меди (II) выглядит следующим образом:
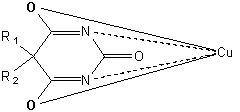
Данная реакция позволяет отличать друг от друга
производные барбитуровой кислоты (табл. 3) [12].
Таблица 3 Наблюдаемый результат реакции с сульфатом меди
|
Лекарственное средство |
Результат реакции |
|
Барбитал |
Синее окрашивание в осадок красно-сиреневого цвета |
|
Фенобарбитал |
Осадок бледно-сиреневого света, не изменяющийся при стоянии |
|
Бензобарбитал (бензонал) |
Серо-голубое окрашивание, переходящее в сиреневое |
|
Барбитал-натрий |
Синее окрашивание, затем выпадает осадок красно-сиреневого цвета |
|
Гексобарбитал-натрий (гексенал) |
Голубое окрашивание, переходящее в ярко-синее, затем выпадает белый осадок |
|
Тиопентал-натрий |
Желто-зеленое окрашивание с взвешенным осадком |
.3. Реакция с ионами серебра. При взаимодействии с
ионами серебра происходит образование однозамещенных (растворимых в воде) и
двузамещенных (нерастворимых в воде) солей серебра [8, 12]. В присутствии
карбоната натрия барбитураты образуют вначале натриевую соль, затем
однозамещенную серебряную:
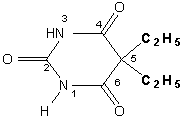 5,5-диэтилбарбитуровая кислота или
5,5-диэтил-1Н,3Н,5Н-пиримидин-2,4,6-трион
5,5-диэтилбарбитуровая кислота или
5,5-диэтил-1Н,3Н,5Н-пиримидин-2,4,6-трион
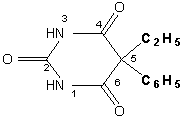 5-этил-5-фенилбарбитуровая кислота или
5-этил-5-фенил-1Н,3Н,5Н-пиримидин-2,4,6-трион
5-этил-5-фенилбарбитуровая кислота или
5-этил-5-фенил-1Н,3Н,5Н-пиримидин-2,4,6-трион
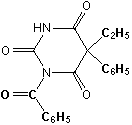 1-бензоил-5-этил-5-фенилбарбитуровая кислота
1-бензоил-5-этил-5-фенилбарбитуровая кислота
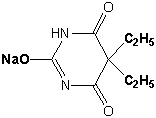 натрия 5,5-диэтилбарбитурат
натрия 5,5-диэтилбарбитурат
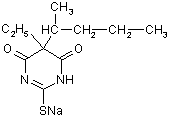 смесь 5-этил-5-(2¢-амил)-2-тиобарбитурата
натрия с безводным карбонатом натрия
смесь 5-этил-5-(2¢-амил)-2-тиобарбитурата
натрия с безводным карбонатом натрия