Материал: Хроматин и его специфическая регуляция экспрессии генов
Важную роль в познании механизма действия энхансеров сыграли работы по изучению механизма переключения экспрессии β-глобиновых генов. У человека этот кластер состоит из пяти родственных генов, один из которых (ε) экспрессируется на ранней эмбриональной стадии, два других (°у и Ау) экспрессируются на поздней эмбриональной стадии и, наконец, гены σ и β экспрессируются в клетках взрослого организма. Расположение генов в домене (начиная от области контроля локуса) соответствует порядку их активации по ходу развития эмбриона. Наиболее интересным представляется тот факт, что экспрессия всех этих генов контролируется одной и той же группой энхансеров, расположенных в области контроля локуса (LCR). Было высказано предположение, что активация транскрипции того или иного из β-глобиновых генов напрямую зависит от установления прямого физического контакта между промотором этого гена и LCR. Понятно, что вероятность установления такого контакта обратно пропорциональна расстоянию между геном и LCR. Иными словами, просто в силу своей близости к LCR эмбриональный ген ε должен транскрибироваться предпочтительно по сравнению с другими β-глобиновыми генами. Эффективная транскрипция последних будет возможна лишь после принудительного выключения гена ε с помощью некоего отличного от LCR контрольного механизма. Сформулированная гипотеза, которую можно назвать «пространственно-статистической» моделью активации транскрипции β-глобиновых генов, позволила сделать несколько предположений, и они были проверены экспериментально. Прежде всего, процесс активации индивидуальных глобиновых генов должен носить статистический характер. Следовательно, в популяции эмбриональных эритроидных клеток, экспрессирующих преимущественно глобиновый ген ε, должно присутствовать определенное количество клеток, экспрессирующих другие глобиновые гены. При этом в некий фиксированный момент времени на каждой из хромосом может экспрессироваться только один из глобиновых генов (ген, промотор которого находится в комплексе с LCR). Это предсказание оказалось вполне справедливым лишь в случае домена β-глобиновых генов мыши. В эмбриональных эритроидных клетках человека гены «взрослых» глобинов вообще не экспрессировались. Другое предсказание, которое можно сделать на основании «пространственно-статистической» модели функционирования LCR, состоит в том, что любое изменение позиции гена (перестановка генов, внедрение дополнительных копий генов и изменение протяженности межгенных спейсеров) в домене, находящемся под контролем LCR, должно существенным образом влиять на характер экспрессии всех генов в домене (в том числе и на время активации транскрипции различных генов по ходу развития организма). В случае домена β-глобиновых генов человека это предсказание было подтверждено результатами экспериментов с трансгенными мышами, в геном которых были внедрены перестроенные копии данного домена. Наиболее показательными можно считать результаты эксперимента, в котором были изменены относительные позиции генов ε (эмбриональный ген) и β (ген, экспрессирующийся в эритроидных клетках взрослого организма). После инверсии всего кластера β-глобиновых генов относительно LCR ген β оказывается расположенным ближе всего к LCR, тогда как ген е, напротив, оказывается наиболее удаленным от LCR. При такой конфигурации домена в эмбриональных эритроидных клетках трансгенных мышей экспрессируется ген β, а эмбриональный ген ε остается неактивным. Этот результат позволяет утверждать, что конкуренция за LCR является важным элементом механизма регуляции экспрессии β-глобиновых генов. Понятно, однако, что переключение экспрессии глобиновых генов в эмбриогенезе не может быть объяснено только конкуренцией промоторов индивидуальных генов за доступ к LCR. Должны существовать дополнительные регуляторные системы, инактивирующие эмбриональные гены и активирующие гены взрослого организма. Здесь, скорее всего, работает механизм создания активных субдоменов при участии связанного с транскрипцией ацетилирования гистонов. Как уже говорилось, уровень ацетилирования гистонов в границах домена β-глобиновых генов существенно различается (рис.6 ). Наиболее высокий уровень ацетилирования характерен для области контроля локуса и для той группы глобиновых генов (эмбриональные, либо взрослые), которые транскрибируются в данном типе клеток.
Наряду с энхансерами, в геноме эукариот
присутствуют сайленсеры, которые подавляют активность находящегося под их
контролем промотора. Принцип действия сайленсеров, по-видимому, мало отличается
от принципа действия энхансеров. Как и энхансеры, сайленсеры представляют собой
площадки связывания транскрипционных факторов. Именно последние определяют
направление действия регуляторного элемента (активация транскрипции либо ее
подавление). Одни и те же регуляторные элементы могут быть энхансерами в одном
типе клеток и сайленсерами в другом типе клеток. Классическим примером является
LCR-домена β-глобиновых
генов, который активирует экспрессию находящихся под его контролем генов в
эритроидных клетках и подавляет экспрессию тех же генов в неэритроидных
клетках.
Заключение
Хроматин уже давно перестал быть аморфной массой и предстал перед глазами исследователей в виде достаточно упорядоченной структуры, построенной по иерархическому принципу.
Для активной фракции хроматина характерна менее компактная упаковка, чем для основной массы хроматина, о чем свидетельствует, в частности предпочтительная чувствительность активного хроматина к нуклеазам. Активный хроматин отличается от неактивного как на уровне организации нуклеосомной фибриллы в структуры высших порядков, так и на уровне организации индивидуальных нуклеосом. Для активного хроматина характерны высокий уровень ацетилирования гистонов в целом.
Важную роль в регуляции инициации транскрипции у эукариот играет процесс освобождения промотора от нуклеосом.
Энхансеры существенны как для создания активного хроматинового домена, так и для поддержания стабильности инициаторного комплекса РНК-полимеразы II.
Энхансеры участвуют в образовании единого инициаторного комплекса с промотором. При этом разделяющая энхансер и промотор хроматиновая фибрилла выпетливается.
Один и тот же регуляторный элемент может быть энхансером и сайленсером в зависимости от набора связанных с этим элементом белковых факторов.
Список литературы
1.Хроматин: упакованный геном / С. В. Разин, А. А. Быстрицкий. - М. : БИНОМ. Лаборатория знаний, 2012.- 176 с.: ил., [16] с. цв. вкл.
. Экспрессия генов / Патрушев Л.И. - М.: Наука, 2000.
хроматин нуклеосомы белок
Приложение 1
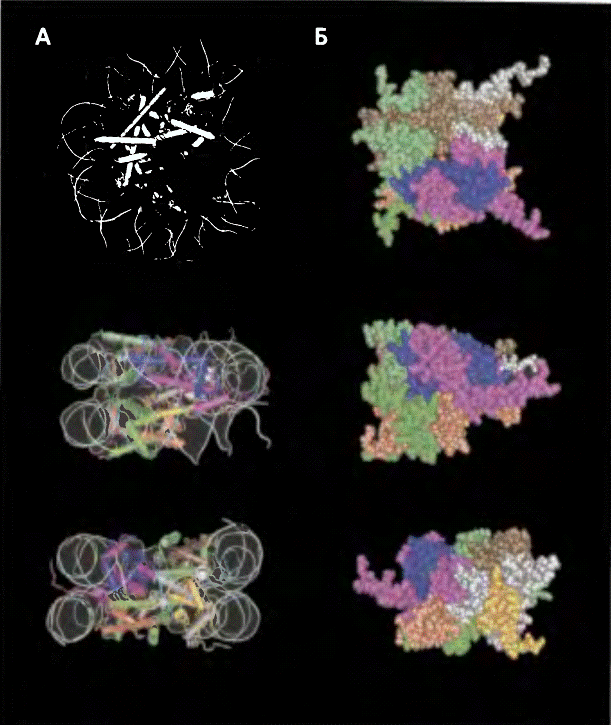
Рис. 3 Модель октамера гистонов
На рисунке представлена молекулярная модель
нуклеосомы (А) и октамера гистонов (Б) в трех разных ракурсах.Разные молекулы
гистонов обозначены следующими цветами: Н2А - красный и коричневый, Н2В -
изумрудный и зеленый. НЗ - розовый и серый. Н4 - синий и оранжевый. «Хвосты»
молекул гистонов показаны не полностью.
Приложение 2
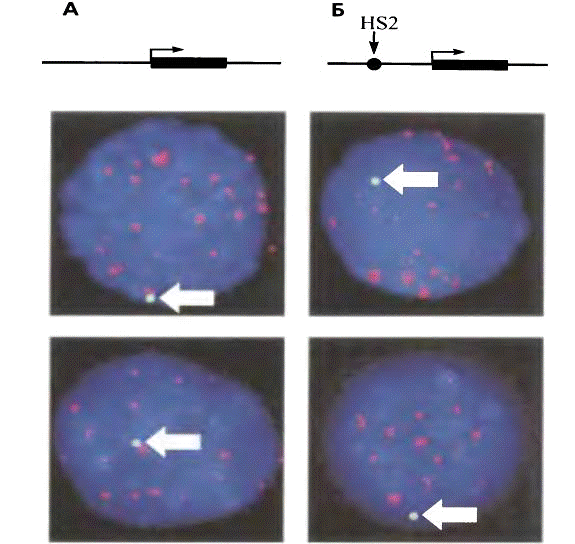
Рис 12. Активность локуса и его внутриядерная
локализация
На рис. показаны результаты визуализации интегрированной в геном трансгенной конструкции в ядрах эритроидных клеток. Для гибридизации с трансгеном использовался зонд, меченный зеленым красителем; красным красителем помечен зонд, позволяющий визуализировать все центромеры (этот зонд гибридизуется с центромерами всех хромосом). Синяя флуоресценция - краситель DAPI, неспецифически окрашивающий тотальную ДНК. Позиции трансгенов отмечены белыми стрелками. Конструкция, в состав которой входит только ген β-глобина (А), локализуется преимущественно возле центромер. Так как центромеры содержат гетерохроматин, то и трансген оказывается гетерохроматинизирован и репрессирован. Включение же в конструкцию энхансера HS2 из области контроля локуса β-глобинового домена (Б) приводит к тому, что такой трансген локализуется преимущественно в эухроматических областях ядра. Никакой гетерохроматинизации не происходит и трансген активно экспрессируется.
Важно, что во всех рассмотренных клетках трансгенные конструкции интегрированы в одно и то же место генома. Таким образом, разница в локализации обусловлена только свойствами самой конструкции (т. е. присутствием либо отсутствием в ее составе мощного энхансера).