Материал: Хроматин и его специфическая регуляция экспрессии генов
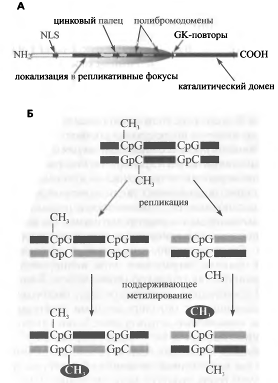
Рис. 8. Метилирование ДНК
За поддержание метилирования ДНК отвечает фермент ДНК-метилтрансфераза 1 - Dnmtl. Слева приведена схема структуры Dnmtl, где отмечены различные функциональные домены белка. Серым выделена часть фермента, препятствующая осуществлению метилирования de novo. Схематически изображен (Б) результат работы Dnmtl: после репликации ДНК новосинтезированные молекулы содержат неметилированные и полуметилированные CpG-ди- нуклеотиды. Dnmtl превращает полуметилированные CpG в полностью метилированные, не затрагивая неметилированные.Некоторые из этих белков, например МеСР2, содержат репрес- сорный домен и прямо подавляют транскрипцию. Кроме того, МеСР2 способен привлекать Sin3-комплекс, содержащий гистон- дезацетилазы HDAC1 и HDAC2. Соответственно, метилирование
Специальным случаем инактивации протяженных
геномных областей, осуществляющейся при участии метилирования ДНК, является
импринтинг, т. е. избирательное выключение только одного из двух родительских
аллелей. Классическим примером импринтированного локуса является локус генов IGF2/H19
мыши. Ген Н19 активен только на материнских хромосомах, а ген IGF2
- только на отцовских хромосомах. В установлении и поддержании импринтинга
важную роль играют особые регуляторные последовательности, получившие название
«центры выбора импринтинга» (ICR
- Imprinting
choice regions).
Это небольшие фрагменты ДНК, которые по-разному метилируются в материнских и
отцовских хромосомах (DMR
- differentially
methylated
regions).
.4 Регуляция транскрипции
В эукариотических клетках разные группы генов транскрибируются различными РНК-полимеразами. РНК-полимераза I транскрибирует гены предшественника основных рибосомных РНК. РНК-полимераза III транскрибирует гены, коротких - 5S рибосомных и транспортных - РНК. Гены, кодирующие абсолютное большинство клеточных белков, транскрибируются РНК-полимеразой II. Поэтому мы будем говорить в этом разделе только о регуляции работы генов, транскрибируемых РНК-полимеразой II.
Основная особенность систем регуляции транскрипции в эукариотической клетке связана с тем, что мишенью для регуляторных сигналов является ДНК, организованная в хроматин. Это значительно расширяет возможности избирательной активации генов. Регуляция транскрипции осуществляется на двух основных уровнях: активация хроматинового домена и активация собственно промотора, условием которой часто является удаление либо перемещение расположенных на промоторе нуклеосом. Здесь обсуждается цепь событий, приводящая к активации индивидуальных промоторов.Промотор является ключевым элементом системы регуляции транскрипции у прокариот, в клетках которых существуют конститутивные и индуцибельные промоторы. В последнем случае активация промотора осуществляется с помощью регуляторных белков. Значение промотора сохраняется и в эукариотических клетках. Важным отличием эукариотических промоторов, однако, является то, что в определении их позиций значительную роль играют эпигенетические факторы.
В составе большинства эукариотических промоторов присутствуют ТАТА-бокс и инициаторная последовательность . ТАТА-бокс, находящийся обычно на расстоянии 25-30 п. н. от старта транскрипции, у эукариот имеет менее консервативный характер, чем у прокариот. Роль ТАТА-бокса может играть почти любая АТ-богатая последовательность. Последовательность inr представляет собой так называемый пиримидиновый бокс (YYANWYY1) и находится непосредственно у точки старта транскрипции. Существует много компьютерных программ, позволяющих предсказывать позиции эукариотических промоторов. К сожалению, найденные с помощью этих программ промоторы далеко не всегда работают в живых клетках. Основная проблема с предсказанием позиций эукариотических промоторов заключается в том, что эти предсказания делаются на основе анализа последовательности ДНК без учета эпигенетических факторов. Между тем позиции активных промоторов в значительной мере определяются на уровне организации ДНК в хроматиновую фибриллу. Инициаторный комплекс РНК-полимеразы II является слишком большим для того, чтобы его можно было собрать на межнуклеосомном спейсере. Для сборки этого комплекса промотор должен быть тем или иным образом освобожден от нуклеосом. Это может быть обеспечено рядом механизмов. Во многих случаях достаточно привлечения к промоторной области фактора (факторов) ремоделирования хроматина. Этот процесс может осуществляться при участии тканеспецифичных транскрипционных факторов. Важную роль играет также локальное ацетилирование гистонов, в том числе гистона H2A.Z в промоторных областях. Согласно последним данным, гистон H2A.Z присутствует как в активных, так и в неактивных промоторах, и именно его ацетилирование существенно для активации промотора. Показано, что для поддержания свободного от нуклеосом участка в промоторной области он должен быть фланкирован двумя нуклеосомами, содержащими гистон H2A.Z. Следует особо отметить, что гистон H2A.Z включается в нуклеосомы по независимому от репликации пути. Это обеспечивает возможность избирательной активации промоторов сайт-специфичным включением этого гистона в нуклеосомы в ходе клеточной дифференцировки или реакций на те или иные внешние сигналы. Существуют и другие механизмы создания свободных от нуклеосом участков (участков гиперчувствительности к ДНКазе I).
Свободный от нуклеосом промотор служит местом сборки преинициаторного транскрипционного комплекса, включающего РНК-полимеразу II и шесть консервативных неспецифических (general) факторов транскрипции (обычно их называют общими транскрипционными факторами): TFI1A, TFIIB, TFIID, TFIIE, TFIIF, TFIIH. Лишь один из этих общих транскрипционных факторов (TFIID) способен узнавать промотор. В состав этого фактора транскрипции, состоящего из нескольких субъединиц, входит белок, способный связываться с ТАТА боксом (TATA-binding protein, ТВР) и ряд вспомогательных белков. В экспериментах in vitro с использованием сильного аденовирусного промотора, содержащего классический ТАТА-бокс, ТВР способен замещать полноценный TFIID, обеспечивая базальный уровень транскрипции. В этой системе не требуется также TFIIA. Белки TAF способны узнавать отличные от ТАТА-бокса домены промотора и абсолютно необходимы для инициации транскрипции на широком классе промоторов, не содержащих ТАТА-бокса. Кроме того, они являются мишенями для взаимодействия с тканеспецифичными транскрипционными факторами, в силу чего являются необходимыми для избирательной инициации транскрипции с определенных групп промоторов.
В несколько упрощенном виде современная модель сборки преинициаторного комплекса при участии общих факторов транскрипции выглядит так: TFIID узнает минимальный промотор и, связываясь с ним, обозначает место сборки транскрипционного комплекса. TFIIA и TFIIB стабилизируют взаимодействие ТВР с ДНК, контактируя одновременно с ДНК и ТВР. TFIIF обеспечивает посадку РНК-полимеразы II на формирующийся комплекс. Далее к комплексу присоединяются TFIIE и TFIIH. Последний представляет собой АТФ-зависимую ДНК-хеликазу, которая обеспечивает локальное плавление ДНК в точке начала транскрипции.
Для сборки транскрипционного комплекса in vivo на большинстве промоторов, помимо общих транскрипционных факторов требуется целый ряд дополнительных белков. Регуляторные белки, способствующие активации промотора, как правило, называют транскрипционными факторами. Уже говорилось выше, что эти факторы могут взаимодействовать с TAF-белками, участвуя в определении места посадки на ДНК фактора TFIID. Известно очень много транскрипционных факторов. Некоторые из них являются универсальными, например фактор Spl. Большинство характеризуется определенной специфичностью в отношении типа ткани. Например, в эритроидных клетках существенную роль в инициации транскрипции глобиновых генов играют транскрипционные факторы GATA-1 и NF-E2.
Наряду с промоторами важную роль в регуляции
транскрипции эукариотических генов играют энхансеры и сайленсеры, которые,
соответственно, стимулируют и подавляют активность промоторов. Так случилось,
что первыми были охарактеризованы энхансеры различных вирусов (вируса SV40,
цитомегаловируса и т. д.). Эти энхансеры не проявляют тканевой специфичности.
Они могут работать, находясь на значительном удалении от промотора и будучи
расположены в различных ориентациях. В геноме эукариотической клетки многие
энхансеры являются тканеспецифичными и могут работать только в тандеме с
промотором определенного класса. Механизм работы энхансеров/сайленсеров пока
еще не раскрыт и остается предметом дискуссий. Известно, что большинство
энхансеров содержит участки связывания для различных транскрипционных факторов.
Так, энхансер вируса SV-40
содержит несколько участков связывания транскрипционного фактора Spl.
Энхансеры α- и β-глобиновых
генов содержат участки связывания транскрипционных факторов GATA-1
и NF-E2.
В геноме дрожжей существуют так называемые UAS
(upstream
activating
sequences), которые играют
важную роль в процессе сборки инициаторного комплекса РНК-полимеразы II.
Последовательности UAS
расположены на небольшом (менее 1 т. п. н.) расстоянии от промоторов.
Считается, что комплекс связанных с UAS
транскрипционных факторов прямо взаимодействует с TAF-белками,
способствуя удержанию TFIID
на промоторе. При этом небольшой фрагмент ДНК, разделяющий UAS
и промотор, образует петлю. На этой петле могут находиться две или три
нуклеосомные глобулы. Энхансеры высших эукариот могут располагаться на
существенно большем расстоянии от контролируемых ими генов (иногда это
расстояние превышает 100 т. п. н.). Подобно UAS
дрожжей, энхансеры высших эукариот являются местами сборки тех или иных активаторных
комплексов. Именно по причине взаимодействия с комплексом транскрипционных
факторов активные энхансеры оказываются расположены в свободных от нуклеосом
участках (участках гиперчувствительности к ДНКазе I). Основной вопрос, который
возникает при попытке объяснить механизм действия эукариотических энхансеров,
состоит в том, как активаторный сигнал передается на значительные расстояния. В
современной литературе обсуждается несколько моделей, объясняющих передачу
активаторного сигнала от энхансера к промоторам (рис. 9). Все эти модели можно
разделить на две большие группы: модели, основанные на процессивном
распространении активирующего сигнала (tracking),
и модели, основанные на непосредственном взаимодействии энхансера и промотора с
выпетливанием разделяющего их фрагмента (looping).
Ясно, однако, что такой механизм не может действовать на очень больших
расстояниях. Действительно, между удаленными энхансерами и регулируемыми ими
генами часто располагаются гены, которые данным энхансером не активируются. Ацетилирование
же гистонов не обладает избирательностью и должно привести к активации всех
генов, расположенных в гиперацетилированном домене. Модель, предполагающая
прямое взаимодействие энхансера и промотора (с выпетливанием разделяющего их
фрагмента ДНК), эту проблему легко решает. В настоящее время получены
убедительные доказательства того, что удаленные энхансеры (а точнее говоря,
связанные с энхансерами регуляторные белки) прямо взаимодействуют с
промоторами, образуя сложный активаторный комплекс с транскрипционными
факторами, локализованными на промоторе. В англоязычной литературе этот
активаторный комплекс называют chromatin
hub. Сам факт
взаимодействия удаленных регуляторных элементов с контролируемыми ими
промоторами подтвердился в экспериментах по изучению трехмерной организации ДНК
в ядре. Используемый при этом экспериментальный подход, получивший название ЗС
(«три цэ» - chromosome
conformation
capture), заключается в
том, что из сшитых формальдегидом ядер удаляют гистоны, после чего ДНК
обрабатывается рестриктазами и лигируется по липким концам. Понятно, что
вероятность лигирования свободно диффундирующих в растворе фрагментов ДНК
крайне мала. В то же время вероятность лигирования фрагментов, связанных друг с
другом посредством белков, будет значительно выше.
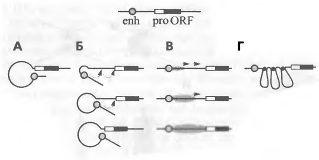
Рис 9. Модель действия энхансера
На рисунке показаны основные обсуждаемые в настоящее время модели взаимодействия энхансера (enh) и промотора (pro). А - прямое взаимодействие при выпетливании района между энхансером и промотором; Б - опосредованное, или сканирующее, выпетливание (в отличие от предыдущего варианта, при котором взаимодействие промотора и энхансера происходит «сразу»); В - распространение некоего активирующего сигнала; Г - приближение энхансера к промотору каким-то дополнительным механизмом (например, белками, укладывающими хроматин между энхансером и промотором в компактную структуру).
Соответствующие различия могут быть зарегистрированы с использованием количественной или полуколичественной полимеразной цепной реакции (рис. 10). С помощью этого экспериментального подхода было продемонстрировано прямое взаимодействие LCR-домена β-глобиновых генов мыши с промоторами глобиновых генов. Было также показано, что структура активирующих комплексов изменяется при переходе домена из потенциально активной в активную форму (рис. 11). Аналогичные наблюдения были сделаны и при изучении ряда других геномных локусов. Выявлены также случаи участия в образовании сложного активаторного комплекса (chromatin hub) регуляторных элементов, расположенных на разных хромосомах. Такие межхромосомные взаимодействия могут играть важную роль в координации экспрессии связанных в функциональном отношении генов, которые располагаются на разных хромосомах.
Следует отметить, что модель образования прямого
активаторного комплекса с участием промоторов и удаленных энхансеров не
исключает возможности последующего ограниченного распространения активирующего
сигнала, т. е. создания активного хроматинового домена, характеризующегося повышенным
уровнем ацетилирования гистонов.
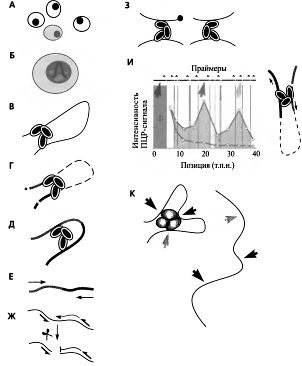
Рис. 10. Принцип метода ЗС
В основе метода лежит лигирование рестриктных
фрагментов, зафиксированных ДНК-белковыми сшивками, при низкой концентрации
ДНК. Клетки (А) обрабатывают формальдегидом, что приводит к образованию
белок-белковых и ДНК-бел- ковых сшивок (Б). Затем клетки лизируют, осаждают
хроматиновую фракцию и детергентом отмывают несвязанные белки. Полученные
ДНК-белковые препараты (В) обрабатывают рестриктазами (Г)- Полученный препарат
сильно разбавляют. Благодаря разбавлению фрагменты ДНК оказываются
изолированными друг от друга, кроме тех, которые остались объединены белковыми
сшивками. Очевидно, что это Moiyr
быть только участки ДНК, которые изначально in
vivo входили в состав
каких-либо крупных надмолекулярных комплексов. Затем в полученный разбавленный
препарат добавляют лигазу. В этих условиях лигироваться могут только
пространственно сближенные рестрикгные фрагменты - т. е. только фрагменты,
объединенные белковыми сшивками (Д) - иными словами, взаимодействовашие in
vivo. После лигирования
выделяют ДНК и детектируют продукты лигирования
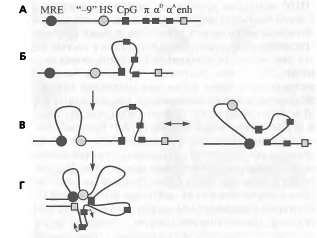
Рис. 11. Формирование единого активаторного
комплекса
На примере домена а-глобиновых генов кур показано, как активация домена отражается на его пространственной организции. Домен а-глобино- вых генов кур (А) включает три гена - эмбриональный п и взрослые aD и аА. Помимо генов, в состав домена входят регуляторные элементы: главный регуляторный элемент (MRE - main regulatory element, аналог области контроля локуса), участок гиперчувствительности к ДНКазе, расположенный на расстоянии 9 т. п. н. перед геном п («-9» HS), CpG-островок и энхансер (enh), расположенный после гена оР. В не-эритроидных клетках взаимодействий между различными функциональными элементами домена практически нет (Б). В не- дифференциированных предшественниках эритробластов наблюдаются отдельные взаимодействия между некоторыми элементами, причем возможно несколько вариантов таких взаимодействий (В). Наконец, в зрелых эритробластах практически все регуляторные элементы, наряду с промоторами транскрибируемых генов, объединены в структуру, получившую название «хроматиновый хаб» (chromatin hub) (Г). Стрелками показано направление транскрипции работающих генов.
В последние годы активно обсуждается модель, связывающая активацию транскрипции с перемещением гена из неактивного в активный ядерный компартмент. Примером активного компартмента могут служить PML-тельца. Это небольшие компартменты, содержащие PML-белки и ряд транскрипционных факторов, наиболее активные генные домены выпетливаются из хромосомных территорий. Показано, что при этом они перемещаются к PML-тельцам, что, по-видимому, способствует активации транскрипции. Область, прилежащая к ядерной оболочке, и области, прилежащие к конститутивному (например, прицентромерному) гетерохроматину, являются неактивными компартментами. Предполагается, что простое перемещение генов в эти компартменты приводит к их долговременной инактивации. В модельном эксперименте показано, что активный трансген, поставленный под контроль сильного энхансера, локализуется в эухроматине. Трансген без энхансера локализуется рядом с центромерными областями хромосом (рис 12,приложение 2 ). Следует подчеркнуть, что речь идет не об интеграции трансгена в эухроматиновую или гетерохроматиновую область хромосомы, а просто о размещении соответствующего хромосомного домена внутри ядра. Существует целый ряд экспериментальных данных, свидетельствующих о том, что локализация в ядре многих тканеспецифичных генов зависит от их транскрипционного статуса. С помощью флуоресцентной гибридизации in situ было продемонстрировано, что в эритроидных клетках глобиновые гены располагаются далеко от конститутивного гетерохроматина, тогда как в неэритроидных они практически контактируют с конститутивным гетерохроматином. В лимфоидных клетках целый ряд генов инактивируется при участии белка «Ikaros». Эта инактивация коррелирует с перемещением соответствующих генов в один из прицентромерных компартментов. Белок Ikaros, по-видимому, играет важную роль в этом перемещении, так как, с одной стороны, на ДНК имеются участки узнавания Ikaros, а с другой стороны, Ikaros способен образовывать комплексы с прицентромерным гетерохроматином.