Материал: Хроматин и его специфическая регуляция экспрессии генов
Обнаружение предпочтительной чувствительности
транскрибирующейся фракции генома к ДНКазе I открыло принципиальную возможность
выделения и характеристики коротких фрагментов транскрипционно-активного
хроматина. Было продемонстрировано, что транскрипционно-активный хроматин
характеризуется повышенным уровнем ацетилирования гистонов нуклеосомной
частицы. Примерно в это же время в лаборатории Олфри был разработан метод
выделения фрагментов транскрипционно-активного хроматина посредством афинной
хроматографии на колонках с иммобилизованной ртутью. И в этом случае было
показано, что транскрипционно-активный хроматин характеризуется повышенным
уровнем ацетилирования гистонов. Другими отличительными признаками активного
хроматина явились обедненность гистоном Н1 и некоторое обогащение различными
типами HMG-белков. Еще
одной характерной чертой нуклеосом активного хроматина является частое
отсутствие одного из димеров Н2А-Н2В. Характерной особенностью
транскрипционно-активной фракции хроматина, является высокий уровень
ацетилирования гистонов. В экспериментах по сборке хроматина in
vitro
продемонстрировано, что хроматин, собранный с использованием
гиперацетилированных гистонов, обладает основными свойствами активного
хроматина, в частности повышенной чувствительностью к нуклеазам.
.2 Транскрипция ДНК, организованной в нуклеосомы
Нуклеосомные частицы должны являться серьезным препятствием на пути транскрипции. Тем не менее четко продемонстрировано, что все РНК-полимеразы, в том числе и прокариотические, способны транскрибировать ДНК, организованную в нуклеосомы. Механизм транскрипции ДНК, организованной в нуклеосомы, остается предметом научных дискуссий. Существует две основные модели, объясняющие возможность транскрипции нуклеосомной нити. Одна из них предполагает, что нуклеосомная глобула, находящаяся на пути транскрипционного комплекса, временно удаляется, оставаясь при этом связанной с самим транскрипционным комплексом, и далее вновь связывается с ДНК за транскрипционным комплексом. Эта модель получила прямые подтверждения в модельных экспериментах по транскрипции бактериальными РНК-полимеразами организованного в нуклеосому фрагмента ДНК. Результаты этих экспериментов не удалось, однако, воспроизвести при использовании эукариотической РНК-полимеразы II. Другая модель транскрипции нуклеосомной нити предполагает, что дестабилизированные нуклеосомы активной фракции хроматина частично разворачиваются непосредственно в момент прохождения транскрипционного комплекса, в результате чего РНК-полимера за может считывать ДНК, не удаляя гистонов. Надо сказать, что в местах входа и выхода ДНК из нуклеосомы ДНК-белковые контакты относительно малочисленны, что допускает возможность постепенного разворачивания накрученной на нуклеосому петли ДНК. Работающий транскрипционный комплекс разворачивает двойную спираль ДНК, что компенсируется возникновением домена положительной суперспирализации перед транскрипционным комплексом. Витки ДНК на нуклеосоме представляют собой негативную суперспираль, стабилизированную взаимодействием с нуклеосомными гистонами. Понятно, что позитивная суперспирализация будет способствовать разворачиванию накрученных на нуклеосому петель ДНК.
В обеспечении возможности транскрипции организованной в нуклеосомы ДНК важную роль играют факторы ремоделирования хроматина.
Сравнительно недавно продемонстрировано, что важную роль в транскрипции организованной в нуклеосомы ДНК играет белковый комплекс, получивший название FACT (facilitator of chromatin transcription). Этот белковый комплекс способствует временному удалению из нуклеосомы одного или обоих димеров Н2А-Н2В, облегчая разворачивание петель нуклеосомной ДНК в местах входа и выхода ДНК из нуклеосомной частицы. Для осуществления своей функции FACT должен быть посажен на активные промоторы. Это достигается при участии вспомогательного комплекса ремоделирования хроматина CHD1, который обладает сродством к FACT и к нуклеосомам, содержащим гистон НЗ, триметилированный по позиции К4.Эта модификация гистона НЗ характерна для активного хроматина. Нуклеосомы, содержащие НЗ, триметилированный по позиции К4, локализуются преимущественно в промоторных областях и в начале активных транскрипционных единиц. Для оптимальной работы FACT существенно еще и моноубиквитинилирование гистона Н2В по К120. Считается, что эта модификация способствует ди- и три- метилированию НЗ по позиции К4.
Исследования, проведенные с использованием метода иммунопреципитации хроматина, выявили неравномерное распределение модифицированных и вариантных форм гистонов в границах транскрипционных единиц . Это объясняется тем, что внесение некоторых модификаций прямо сопряжено с осуществлением транскрипции. В дрожжевых клетках этот процесс происходит следующим образом. Сразу после инициации транскрипции происходит фосфорилирование серинового остатка 5 (Ser5) в составе С-концевого домена (C-terminal domain, CTD) РНК-полимеразы II. Эта модификация способствует привлечению мультибелкового комплекса, известного как фактор элонгации PAF. Этот фактор способствует удержанию
в составе элонгирующего транскрипционного комплекса гис-тонубиквитинлигазы, которая убиквитинилирует гистон Н2В. Одновременно PAF привлекает в состав элонгирующего транскрипционного комплекса НЗК4 гистонметилазу (Set 1 комплекс COMPASS). Этот комплекс осуществляет ди- и триметилиро- вание НЗК4. Монометилирование осуществляется обычной гистонметилазой Set 1 и не зависит от убиквитинилирования гистона Н2В. По мере продвижения элонгирующего РНК-по- лимеразного комплекса вдоль транскрипционной единицы происходит дефосфорилирование Ser5 и фосфорилирование Ser2 в составе CTD. Следствием этого изменения в характере модификации CTD является освобождение гистонметилазы COMPASS и привлечение гистонметилазы Set2, которая осуществляет триметилироване лизинового остатка 36 гистона НЗ. Следствием этой сложной цепи процессов является накопление ди- и триметилированного по К4 гистона НЗ в начале транскрипционной единицы и триметилированного по К36 гистона НЗ в конце транскрипционной единицы. На основании всего вышесказанного можно сделать один вывод, имеющий более общее значение. Определенная группа модификаций гистонов необходима для привлечения РНК-полимеразы II к промоторным областям. Распределение таких модифицированных (и выполняющих ту же функцию вариантных) форм гистонов в границах транскрипционных единиц и в целом в геноме не зависит от уровня транскрипции. Другие модификации осуществляются в прямой связи с процессом транскрипции. Распределение таких модифицированных гистонов прямо коррелирует с уровнем транскрипции соответствующих областей генома.Сопряженная с транскрипцией смена характера метилирования гистона НЗ имеет большое биологическое значение. Триметилирование H3K36 в дрожжевых клетках способствует привлечению гистондезацетилазы Rpd3S, которая снижает общий уровень ацетилирования гистонов на большей части транскриционной единицы после каждого раунда транскрипции. Вероятно, это необходимо для предотвращения возможности инициации транскрипции внутри гена. Так называемые криптические промоторы, т. е. последовательности ДНК, которые в принципе могли бы служить местами посадки РНК-полимеразы II, встречаются в геноме эукариот достаточно часто. Организация ДНК в стабильную нуклеосомную структуру препятствует активации этих промоторов.
В заключение данного раздела следует
подчеркнуть, что связанные с осуществлением транскрипции модификации гистонов
носят динамический характер. С помощью специальных экспериментальных подходов
можно наблюдать последовательное ацетилирование-дезацентилирование гистонов,
сопряженное с прохождением соответствующих раундов транскрипции.
.3 Доменная организация
Эксперименты по изучению предпочтительной чувствительности к нуклеазам активных генов продемонстрировали, что область предпочтительной чувствительности к нуклеазам, как правило, оказывается существенно более протяженной, чем транскрибирующийся ген. В ряде случаев предпочтительно чувствительными к нуклеазам оказывались достаточно протяженные (100 т. п. н. и более) геномные домены, включающие как транскрибирующиеся, так и молчащие гены, а также межгенные области. В качестве примеров можно указать домены Р-глобиновых генов позвоночных и домен генов овальбумина кур (рис. 6). Границы ДНКазо-чув- ствительных доменов являются достаточно четкими. Переход от ДНКазо-чувствительной области к области, характеризующейся относительной устойчивостью к ДНКазам, происходит в пределах фрагмента ДНК протяженностью в несколько т. п. н. (рис. 6). Это позволяет предположить, что существуют специальные элементы генома и соответствующие им структуры хроматина, которые являются границами ДНКазо-чувствительных доменов. ДНКазо- чувствительные домены генома привлекли особое внимание исследователей прежде всего потому, что очевидна была определенная зависимость между статусом этих доменов и транскрипционной активностью соответствующих генов.
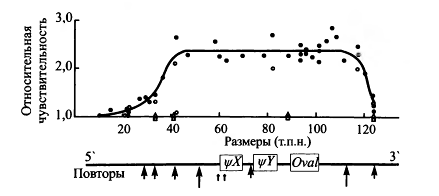
Рис. 6. Профиль чувствительности к ДНКазе I
домена гена овальбумина кур.В состав домена входит ген овальбумина (Oval)
и два псевдогена (\\fX
и у Y). Над схемой
домена приведен профиль относительной чувствительности домена и его
окрестностей к ДНКазе I в клетках яйцевода, где овальбуминовые гены
экспрессируются
Можно говорить о том, что ДНКазо-чувствительные домены хроматина являются структурно-функциональными блоками генома, которые могут находиться в активном либо неактивном состоянии в зависимости от типа клеток, или, иными словами, в зависимости от неких дополнительных сигналов. Это положение можно считать основой так называемой доменной гипотезы структурнофункциональной организации эукариотического генома. Данная гипотеза приобрела особую привлекательность после того, как были обнаружены области контроля локуса (locus control regions, LCRs), которые, как следовало из результатов первоначальных экспериментов, осуществляли контроль над всеми параметрами (чувствительность к ДНКазам, транскрипционный статус и время репликации) протяженных доменов генома. Однако все гены, расположенные в активном хроматиновом домене, являются потенциально активными и могут быть быстро вовлечены в транскрипцию. Вопрос о том, как возникает активный хроматиновый домен, до конца не изучен. Понятно, что появление такого домена является результатом сложной цепи событий, превращающей неактивный хроматин в активный. Наиболее важным процессом, приводящим к активации хроматинового домена, является осуществление комплекса сайт-специфических модификаций гистонов. Хотя о доменной организации генома написаны сотни статей, количество изученных модельных систем является весьма скромным.
В настоящее время процесс создания активных
геномных доменов прямо связывают с процессивным (т. е. распространяющимся)
ацетилированием гистонов в рамках всего домена. Прежде всего, этот процесс
должен инициироваться в каком-то определенном месте. Согласно современным
представлениям, таким местом может быть область контроля локуса, энхансер или
промотор. Связанные с этими регуляторными элементами транскрипционные факторы
способны привлекать гистонацетилазы. Эукариотические гистонацетилазы входят в
состав больших мультисубъединичных комплексов. Наряду с собственно
гистонацетилазой (например, GCN5
в клетках дрожжей) в состав этих комплексов входят субъединицы, способные
взаимодействовать с различными транскрипционными факторами и общими факторами
инициации транскрипции. Это способствует привлечению гистонацетилаз к
промоторам и энхансерам, где они осуществляют локальное аце- тилирование
гистонов. В состав гистонацетилазных комплексов входят и субъединицы,
содержащие так называемый бромодомен, который узнает ацетилированные остатки
лизина в молекулах гистонов. В связи с этим возникновение области локального
ацетилирования гистонов будет способствовать привлечению дополнительных
гистонацетилаз, которые будут ацетилировать гистоны в составе соседних
нуклеосом, перемещаться на эти нуклеосомы и продолжать процесс
распространяющегося ацетилирования (рис. 7). Этот механизм распространяющегося
ацетилирования не является единственным. Согласно гипотезе Траверса,
элонгирующий комплекс РНК-полимеразы II может сам являться тем транспортным
средством, которое используется для перемещения вдоль хроматинового домена
факторов ремоделирования хроматина, гистонацетилаз и других белков, необходимых
для активации хроматиновых доменов. Соответственно, низкоуровневая транскрипция
протяженных геномных доменов может быть необходима для их активации. Основное положение
гипотезы Траверса, а именно то, что распространяющийся процесс модификации
гистонов осуществляется в непосредственной связи с процессом транскрипции,
подтверждено в настоящее время экспериментально
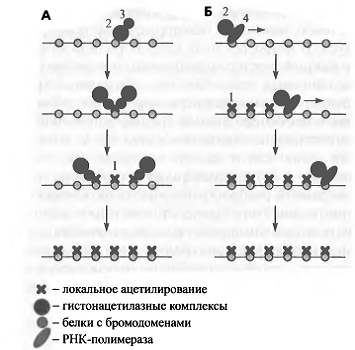
Рис. 7. Механизмы распространения ацетилирования
гистонов по хроматиновому домену
Схематически изображены две общепринятые модели. Согласно модели расширяющегося домена (А), локальное ацетилирование привлекает гистонацетилазные комплексы за счет белков с бромодоменами, которые связываются с ацетилированными гистонами. Таким образом, действует положительная обратная связь и происходит распространение ацетилирования. Модель Траверса (Б) предполагает, что гистонацетилазные комплексы взаимодействуют с РНК-по- лимеразой и ацетилируют гистоны по мере элонгации транскрипции.
С использованием метода ко-иммунопреципитации продемонстрировано, что в живых клетках РНК-полимераза II образует комплексы с гистонацетилазами и факторами ремоделирования хроматина. Протяженные (так называемые «межгенные», а точнее говоря, «полнодоменные») транскрипты обнаружены в целом ряде геномных областей, и выявлена корреляция между началом синтеза этих транскриптов и активацией соответствующих доменов генома. Так, продемонстрировано, что в незрелых эритробластах кур, т. е. еще до начала активной транскрипции глобиновых генов, осуществляется транскрипция протяженной геномной области, включающей кластер α-глобиновых генов и 5'-концевые регуляторные элементы домена α-глобиновых генов.
Вывод: предпочтительной чувствительностью к ДНКазе обладают не только активные гены, но и более протяженные области генома, включающие эти гены. Существуют особые регуляторные элементы, контролирующие транскрипционный статус геномных доменов на уровне упаковки этих доменов в хроматиновый структуры высших порядков. Активные хроматиновые домены формируются посредством процессивного ацетилирования гистонов при участии гистонацетилаз, содержащих бромодомен, который узнает гистон НЗ, ацетилированный по позиции К9. Процессивное ацетилирование гистонов может быть сопряжено с низкоуровневой транскрипцией. При этом гистонацетилазы и комплексы ремоделирования хроматина перемещаются вдоль генномного домена в комплексе с РНК-полимеразой II. Каков бы ни был механизм процессивного ацетилирования гистонов, он инициируется в области контроля локуса, энхансере или промоторе, где собирается необходимый для такой инициации комплекс транскрипционных факторов.
В течение многих лет было принято считать, что
нормальным («заданным по умолчанию») состоянием хроматина является полностью
неактивное состояние, исключающее возможность транскрипции. Соответственно,
предполагалось, что активный хроматин формируется в локальных областях в ответ
на действие специальных сигналов. В последние годы стало очевидным, что
«заданным по умолчанию» является некое промежуточное состояние хроматина и что
особая цепь процессов необходима для формирования как активного, так и
неактивного хроматина. Раскрытию механизмов формирования неактивного хроматина
во многом способствовало изучение мутаций, подавляющих так называемый эффект
положения (т. е. инактивацию гена, оказавшегося рядом с неактивным хроматиновым
доменом - гетерохроматином). Такая инактивация является следствием спонтанного
расширения гетерохроматинового домена. Соответственно, подавляющие эффект
положения мутации, как правило, затрагивают гены, кодирующие необходимые для
формирования гетерохроматина белки. Такими белками являются ДНК-метилазы,
гистонметилазы, гистондезацетилазы, белки, связывающиеся с метилированными
остатками цитозина в ДНК, и так называемые «структурные белки гетерохроматина»
(НР1 у высших эукариот и Sir
- белки у дрожжей).У позвоночных животных одним из основных инструментов
инактивации как протяженных геномных областей, так и отдельных генов или групп
генов является метилирование ДНК. Мишенью для работы эукариотических
ДНК-метилаз являются симметрично расположенные остатки цитозина в составе CpG-динуклеотидов.
В клетках существует поддерживающая ДНК-метилаза (Dnmtl
- DNA methyltransferase
1), которая восстанавливает симметричный характер метилирования после
репликации ДНК (рис. 8). В составе Dnmtl
присутствует особый домен, препятствующий осуществлению метилирования novo.
На определенном этапе эмбрионального развития вся ДНК деметилируется и потом избирательно
метилируется de
novo. Этот процесс
осуществляется особой группой ДНК-метилаз (Dnmt3a,
Dnmt3b).
Каким образом на этой стадии обеспечивается избирательный характер
метилирования определенных генов или фрагментов генома, в настоящий момент не
ясно. В клетке существует целый класс белков, которые связываются с
метилированными остатками цитозина. ДНК может инициировать процесс
дезацетилирования гистонов, результатом которого будет инактивация
хроматинового домена. С помощью метилирования ДНК инактивируется транскрипция
различных повторяющихся последовательностей, транспозонов и многих
тканеспецифичных генов.