Материал: Химия и биологическая роль элементов VA-группы
![]()
Соли <https://ru.wikipedia.org/wiki/%D0%A1%D0%BE%D0%BB%D0%B8> гидразина бесцветны, почти все хорошо растворимы в воде. К числу важнейших относится сульфат гидразина N2H4 · H2SO4.
Гидразин как восстановитель: Гидразин - энергичный восстановитель <https://ru.wikipedia.org/wiki/%D0%92%D0%BE%D1%81%D1%81%D1%82%D0%B0%D0%BD%D0%BE%D0%B2%D0%B8%D1%82%D0%B5%D0%BB%D0%B8>. В растворах гидразин обычно также окисляется до азота:
![]()
Восстановить гидразин до аммиака
можно только сильными восстановителями, такими, как Sn2+, Ti3+,
водородом в момент выделения (Zn + HCl):
![]()
Окисляется кислородом <https://ru.wikipedia.org/wiki/%D0%9A%D0%B8%D1%81%D0%BB%D0%BE%D1%80%D0%BE%D0%B4> воздуха до азота, аммиака и воды. Известны многие органические производные гидразина. Гидразин, а также гидразин-гидрат, гидразин-сульфат, гидразин-хлорид, широко применяются в качестве восстановителей золота <https://ru.wikipedia.org/wiki/%D0%97%D0%BE%D0%BB%D0%BE%D1%82%D0%BE>, серебра <https://ru.wikipedia.org/wiki/%D0%A1%D0%B5%D1%80%D0%B5%D0%B1%D1%80%D0%BE>, платиновых металлов <https://ru.wikipedia.org/wiki/%D0%9C%D0%B5%D1%82%D0%B0%D0%BB%D0%BB%D1%8B_%D0%BF%D0%BB%D0%B0%D1%82%D0%B8%D0%BD%D0%BE%D0%B2%D0%BE%D0%B9_%D0%B3%D1%80%D1%83%D0%BF%D0%BF%D1%8B> из разбавленных растворов их солей. Медь в аналогичных условиях восстанавливается до закиси.
В органическом синтезе гидразин применяется для восстановления карбонильной группы <https://ru.wikipedia.org/wiki/%D0%9A%D0%B0%D1%80%D0%B1%D0%BE%D0%BD%D0%B8%D0%BB%D1%8C%D0%BD%D0%B0%D1%8F_%D0%B3%D1%80%D1%83%D0%BF%D0%BF%D0%B0> альдегидов <https://ru.wikipedia.org/wiki/%D0%90%D0%BB%D1%8C%D0%B4%D0%B5%D0%B3%D0%B8%D0%B4%D1%8B> и кетонов <https://ru.wikipedia.org/wiki/%D0%9A%D0%B5%D1%82%D0%BE%D0%BD%D1%8B> до метиленовой по КижнеруВольфу (-реакция КижнераВольфа <https://ru.wikipedia.org/wiki/%D0%A0%D0%B5%D0%B0%D0%BA%D1%86%D0%B8%D1%8F_%D0%9A%D0%B8%D0%B6%D0%BD%D0%B5%D1%80%D0%B0%E2%80%94%D0%92%D0%BE%D0%BB%D1%8C%D1%84%D0%B0>), реакция идёт через образование гидразонов <https://ru.wikipedia.org/wiki/%D0%93%D0%B8%D0%B4%D1%80%D0%B0%D0%B7%D0%BE%D0%BD%D1%8B>, расщепляющихся затем под действием сильных оснований.
Обнаружение: Качественной реакцией на гидразин служит образование окрашенных гидразонов <https://ru.wikipedia.org/wiki/%D0%93%D0%B8%D0%B4%D1%80%D0%B0%D0%B7%D0%BE%D0%BD%D1%8B> с некоторыми альдегидами <https://ru.wikipedia.org/wiki/%D0%90%D0%BB%D1%8C%D0%B4%D0%B5%D0%B3%D0%B8%D0%B4%D1%8B>, в частности - с p- диметиламинобензальдегидом.
Гидроксилами́н NH2OH - бесцветные кристаллы, легко растворимые в воде с образованием гидрата NH2ОН·Н2О.
Свойства: В водном растворе диссоциирует <https://ru.wikipedia.org/wiki/%D0%94%D0%B8%D1%81%D1%81%D0%BE%D1%86%D0%B8%D0%B0%D1%86%D0%B8%D1%8F_(%D1%85%D0%B8%D0%BC%D0%B8%D1%8F)> по основному типу, являясь слабым основанием:
![]() Ko = 2·10−8
Ko = 2·10−8
Может также диссоциировать и по
кислотному типу с рКа <https://ru.wikipedia.org/wiki/%D0%9A%D0%BE%D0%BD%D1%81%D1%82%D0%B0%D0%BD%D1%82%D0%B0_%D0%B4%D0%B8%D1%81%D1%81%D0%BE%D1%86%D0%B8%D0%B0%D1%86%D0%B8%D0%B8_%D0%BA%D0%B8%D1%81%D0%BB%D0%BE%D1%82%D1%8B>
= 14,02:
![]()
В кислом водном растворе гидроксиламин устойчив, однако ионы переходных металлов <https://ru.wikipedia.org/wiki/%D0%9F%D0%B5%D1%80%D0%B5%D1%85%D0%BE%D0%B4%D0%BD%D1%8B%D0%B5_%D0%BC%D0%B5%D1%82%D0%B0%D0%BB%D0%BB%D1%8B> катализируют его распад.
Подобно NH3,
гидроксиламин реагирует с кислотами, образуя соли гидроксиламиния, например:
![]()
На воздухе соединение является
нестабильным:
![]()
но при давлении в 3 кПа (2,25 мм рт.ст.) плавится при 32 °С и кипит при 57 °С без разложения.
На воздухе легко окисляется
кислородом воздуха:
![]()
Гидроксиламин проявляет свойства
восстановителя, при действии на него окислителей выделяются N2 или N2O:
![]()
В некоторых реакциях NH2OH
проявляются окислительные свойства, при этом он восстанавливается до NH3
или NH4+, например:
![]()
5. Свойства соединений фосфора
Фосфи́н (фосфористый водород, фосфид водорода <https://ru.wikipedia.org/wiki/%D0%92%D0%BE%D0%B4%D0%BE%D1%80%D0%BE%D0%B4>, гидрид фосфора <https://ru.wikipedia.org/wiki/%D0%A4%D0%BE%D1%81%D1%84%D0%BE%D1%80>, по номенклатуре IUPAC - фосфан РН3) - бесцветный, ядовитый газ (при нормальных условиях) со специфическим запахом гнилой рыбы.
Физические свойства: Бесцветный газ. Плохо растворяется в воде, не реагирует с ней. При низких температурах образует твёрдый клатрат <https://ru.wikipedia.org/wiki/%D0%9A%D0%BB%D0%B0%D1%82%D1%80%D0%B0%D1%82%D1%8B> 8РН3·46Н2О. Растворим в бензоле, диэтиловом эфире <https://ru.wikipedia.org/wiki/%D0%94%D0%B8%D1%8D%D1%82%D0%B8%D0%BB%D0%BE%D0%B2%D1%8B%D0%B9_%D1%8D%D1%84%D0%B8%D1%80>, сероуглероде <https://ru.wikipedia.org/wiki/%D0%A1%D0%B5%D1%80%D0%BE%D1%83%D0%B3%D0%BB%D0%B5%D1%80%D0%BE%D0%B4>. При −133,8 °C образует кристаллы с гранецентрированной кубической решёткой <https://ru.wikipedia.org/wiki/%D0%9A%D1%80%D0%B8%D1%81%D1%82%D0%B0%D0%BB%D0%BB%D0%B8%D1%87%D0%B5%D1%81%D0%BA%D0%B0%D1%8F_%D1%80%D0%B5%D1%88%D1%91%D1%82%D0%BA%D0%B0>.
Молекула фосфина имеет форму тригональной пирамиды c молекулярной симметрией C3v (dPH = 0,142 нм, ∠HPH = 93,5°).Дипольный момент <https://ru.wikipedia.org/wiki/%D0%94%D0%B8%D0%BF%D0%BE%D0%BB%D1%8C%D0%BD%D1%8B%D0%B9_%D0%BC%D0%BE%D0%BC%D0%B5%D0%BD%D1%82> составляет 0,58 <https://ru.wikipedia.org/wiki/%D0%94%D0%B5%D0%B1%D0%B0%D0%B9>, существенно ниже, чем у аммиака <https://ru.wikipedia.org/wiki/%D0%90%D0%BC%D0%BC%D0%B8%D0%B0%D0%BA>. Водородная связь <https://ru.wikipedia.org/wiki/%D0%92%D0%BE%D0%B4%D0%BE%D1%80%D0%BE%D0%B4%D0%BD%D0%B0%D1%8F_%D1%81%D0%B2%D1%8F%D0%B7%D1%8C> между молекулами PH3 практически не проявляется и поэтому фосфин имеет более низкие температуры плавления и кипения.
Химические свойства: Фосфин сильно отличается от своего аналога, аммиака <https://ru.wikipedia.org/wiki/%D0%90%D0%BC%D0%BC%D0%B8%D0%B0%D0%BA>. Его химическая активность выше, чем у аммиака, он плохо растворим в воде <https://ru.wikipedia.org/wiki/%D0%92%D0%BE%D0%B4%D0%B0>, как основание значительно слабее аммиака. Последнее объясняется тем, что связи H−P поляризованы слабо и активность неподелённой пары электронов <https://ru.wikipedia.org/wiki/%D0%AD%D0%BB%D0%B5%D0%BA%D1%82%D1%80%D0%BE%D0%BD%D0%BD%D0%B0%D1%8F_%D0%BF%D0%B0%D1%80%D0%B0> у фосфора (3s2) ниже, чем у азота (2s2) в аммиаке.
В отсутствие кислорода при
нагревании разлагается на элементы:
![]()
на воздухе самопроизвольно
воспламеняется (в присутствии паров дифосфина
<https://ru.wikipedia.org/wiki/%D0%94%D0%B8%D1%84%D0%BE%D1%81%D1%84%D0%B8%D0%BD>
или при температуре свыше 100 °C)
![]()
Проявляет сильные восстановительные
свойства:
![]()
![]()
![]()
При взаимодействии с сильными
донорами
<https://ru.wikipedia.org/wiki/%D0%A5%D0%B8%D0%BC%D0%B8%D1%87%D0%B5%D1%81%D0%BA%D0%B0%D1%8F_%D1%81%D0%B2%D1%8F%D0%B7%D1%8C>
протонов фосфин может давать соли фосфония <https://ru.wikipedia.org/w/index.php?title=%D0%A4%D0%BE%D1%81%D1%84%D0%BE%D0%BD%D0%B8%D0%B9&action=edit&redlink=1>,
содержащие ион PH4+ (аналогично аммонию
<https://ru.wikipedia.org/wiki/%D0%90%D0%BC%D0%BC%D0%BE%D0%BD%D0%B8%D0%B9>).
Соли фосфония, бесцветные кристаллические вещества, крайне неустойчивы, легко
гидролизуется
<https://ru.wikipedia.org/wiki/%D0%93%D0%B8%D0%B4%D1%80%D0%BE%D0%BB%D0%B8%D0%B7>.
![]()
![]()
Соли фосфония, как и сам фосфин, являются сильными восстановителями <https://ru.wikipedia.org/wiki/%D0%92%D0%BE%D1%81%D1%81%D1%82%D0%B0%D0%BD%D0%BE%D0%B2%D0%B8%D1%82%D0%B5%D0%BB%D0%B8>.
Фосфи́ды - бинарные соединения <https://ru.wikipedia.org/wiki/%D0%91%D0%B8%D0%BD%D0%B0%D1%80%D0%BD%D1%8B%D0%B5_%D1%81%D0%BE%D0%B5%D0%B4%D0%B8%D0%BD%D0%B5%D0%BD%D0%B8%D1%8F> фосфора <https://ru.wikipedia.org/wiki/%D0%A4%D0%BE%D1%81%D1%84%D0%BE%D1%80> с другими менее электроотрицательными химическими элементами <https://ru.wikipedia.org/wiki/%D0%A5%D0%B8%D0%BC%D0%B8%D1%87%D0%B5%D1%81%D0%BA%D0%B8%D0%B9_%D1%8D%D0%BB%D0%B5%D0%BC%D0%B5%D0%BD%D1%82>, в которых фосфор проявляет отрицательную степень окисления <https://ru.wikipedia.org/wiki/%D0%A1%D1%82%D0%B5%D0%BF%D0%B5%D0%BD%D1%8C_%D0%BE%D0%BA%D0%B8%D1%81%D0%BB%D0%B5%D0%BD%D0%B8%D1%8F>.
Химические свойства: Фосфиды
металлов - неустойчивые соединения, которые разлагаются водой
<https://ru.wikipedia.org/wiki/%D0%92%D0%BE%D0%B4%D0%B0> и разбавленными
кислотами
<https://ru.wikipedia.org/wiki/%D0%9A%D0%B8%D1%81%D0%BB%D0%BE%D1%82%D0%B0>.
При этом получается фосфин
<https://ru.wikipedia.org/wiki/%D0%A4%D0%BE%D1%81%D1%84%D0%B8%D0%BD> и, в
случае гидролиза
<https://ru.wikipedia.org/wiki/%D0%93%D0%B8%D0%B4%D1%80%D0%BE%D0%BB%D0%B8%D0%B7>,
-гидроксид <https://ru.wikipedia.org/wiki/%D0%93%D0%B8%D0%B4%D1%80%D0%BE%D0%BA%D1%81%D0%B8%D0%B4>
металла, в случае взаимодействия с кислотами - соли.
Ca3P2
+ 6H2O → 3Ca(OH)2 + 2PH33P2 +
6HCl → 3CaCl2 + 2PH3
При умеренном нагревании большинство фосфидов разлагаются. Плавятся под избыточным давлением паров фосфора.
Фосфид бора BP, наоборот, тугоплавкое (tпл. 2000 °C, с разложением), весьма инертное вещество. Разлагается только концентрированными кислотами-окислителями, реагирует при нагревании с кислородом <https://ru.wikipedia.org/wiki/%D0%9A%D0%B8%D1%81%D0%BB%D0%BE%D1%80%D0%BE%D0%B4>, серой <https://ru.wikipedia.org/wiki/%D0%A1%D0%B5%D1%80%D0%B0>, щелочами <https://ru.wikipedia.org/wiki/%D0%A9%D0%B5%D0%BB%D0%BE%D1%87%D1%8C> при спекании.
Фосфи́новые кисло́ты - фосфорсодержащие органические соединения <https://ru.wikipedia.org/wiki/%D0%A4%D0%BE%D1%81%D1%84%D0%BE%D1%80%D0%BE%D1%80%D0%B3%D0%B0%D0%BD%D0%B8%D1%87%D0%B5%D1%81%D0%BA%D0%B8%D0%B5_%D1%81%D0%BE%D0%B5%D0%B4%D0%B8%D0%BD%D0%B5%D0%BD%D0%B8%D1%8F> общей формулы R2P(=O)OH, формально являющиеся замещенными производнымифосфиновой кислоты <https://ru.wikipedia.org/wiki/%D0%A4%D0%BE%D1%81%D1%84%D0%BE%D1%80%D0%BD%D0%BE%D0%B2%D0%B0%D1%82%D0%B8%D1%81%D1%82%D0%B0%D1%8F_%D0%BA%D0%B8%D1%81%D0%BB%D0%BE%D1%82%D0%B0> Н2P(=O)OH.
Соли и сложные эфиры <https://ru.wikipedia.org/wiki/%D0%A1%D0%BB%D0%BE%D0%B6%D0%BD%D1%8B%D0%B5_%D1%8D%D1%84%D0%B8%D1%80%D1%8B> фосфиновых кислот - фосфинаты <https://ru.wikipedia.org/wiki/%D0%A4%D0%BE%D1%81%D1%84%D0%B8%D0%BD%D0%B0%D1%82%D1%8B>.
В спектре ЯМР <https://ru.wikipedia.org/wiki/%D0%AF%D0%9C%D0%A0> 31P химические сдвиги для фосфиновых кислот находятся в области 22-75 м.д., полоса поглощения в ИК спектре связи P=O в области 1140-1210 см−1.
Химические свойства: Основные реакции:
1. Образование ангидридов
<https://ru.wikipedia.org/wiki/%D0%90%D0%BD%D0%B3%D0%B8%D0%B4%D1%80%D0%B8%D0%B4%D1%8B>
при 400°С:
![]()
. Образование эфиров при действии
катализатора
<https://ru.wikipedia.org/wiki/%D0%9A%D0%B0%D1%82%D0%B0%D0%BB%D0%B8%D0%B7%D0%B0%D1%82%D0%BE%D1%80>:
![]()
. Разрыв связей P-С при действии растворов щелочей.
. Восстановление до фосфинов
<https://ru.wikipedia.org/wiki/%D0%A4%D0%BE%D1%81%D1%84%D0%B8%D0%BD%D1%8B>:
![]()
Фосфиты - соли ортофосфористой кислоты <https://ru.wikipedia.org/wiki/%D0%A4%D0%BE%D1%81%D1%84%D0%BE%D1%80%D0%B8%D1%81%D1%82%D0%B0%D1%8F_%D0%BA%D0%B8%D1%81%D0%BB%D0%BE%D1%82%D0%B0> Н3РО3. Анион <https://ru.wikipedia.org/wiki/%D0%90%D0%BD%D0%B8%D0%BE%D0%BD> ортофосфористой кислоты <https://ru.wikipedia.org/wiki/%D0%A4%D0%BE%D1%81%D1%84%D0%BE%D1%80%D0%B8%D1%81%D1%82%D0%B0%D1%8F_%D0%BA%D0%B8%D1%81%D0%BB%D0%BE%D1%82%D0%B0> (HPO32−) является многоатомным ионом <https://ru.wikipedia.org/wiki/%D0%98%D0%BE%D0%BD>, в котором центральным атомом является атом фосфора <https://ru.wikipedia.org/wiki/%D0%A4%D0%BE%D1%81%D1%84%D0%BE%D1%80> в степени окисления +3. Его молекулярная геометрия приблизительно тетраэдрическая <https://ru.wikipedia.org/wiki/%D0%A2%D0%B5%D1%82%D1%80%D0%B0%D1%8D%D0%B4%D1%80>.
Связывание может быть объяснено с помощью
резонансных структур, существует три эквивалентые структуры, содержащие одну
двойную связь эффективно делокализующие отрицательные заряды между
эквивалентными атомами кислорода. Четыре резонансные структуры фосфит-иона:
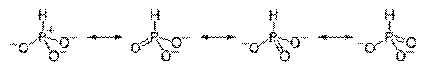 <https://commons.wikimedia.org/wiki/File:Phosphite-ion-resonance-structures-2D.png?uselang=ru>
<https://commons.wikimedia.org/wiki/File:Phosphite-ion-resonance-structures-2D.png?uselang=ru>
Множество солей фосфористой кислоты, такие как фосфит аммония, очень хорошо растворимы в воде. Иногда название фосфиты относят также к эфирам <https://ru.wikipedia.org/wiki/%D0%A1%D0%BB%D0%BE%D0%B6%D0%BD%D1%8B%D0%B5_%D1%8D%D1%84%D0%B8%D1%80%D1%8B> этой кислоты, фосфорорганическим соединениям <https://ru.wikipedia.org/wiki/%D0%A4%D0%BE%D1%81%D1%84%D0%BE%D1%80%D0%BE%D1%80%D0%B3%D0%B0%D0%BD%D0%B8%D1%87%D0%B5%D1%81%D0%BA%D0%B8%D0%B5_%D1%81%D0%BE%D0%B5%D0%B4%D0%B8%D0%BD%D0%B5%D0%BD%D0%B8%D1%8F> с формулой P(OR)3.
Фосфоновые кислоты - тип фосфорсодержащих органических соединений <https://ru.wikipedia.org/wiki/%D0%A4%D0%BE%D1%81%D1%84%D0%BE%D1%80%D0%BE%D1%80%D0%B3%D0%B0%D0%BD%D0%B8%D1%87%D0%B5%D1%81%D0%BA%D0%B8%D0%B5_%D1%81%D0%BE%D0%B5%D0%B4%D0%B8%D0%BD%D0%B5%D0%BD%D0%B8%D1%8F>. Общая формула R-PO(OH)2. Есть связь «углерод-фосфор» Один из важнейших типов фосфоорганических соединений.
Физические свойства: Гигроскопичные белые кристаллы <https://ru.wikipedia.org/wiki/%D0%9A%D1%80%D0%B8%D1%81%D1%82%D0%B0%D0%BB%D0%BB%D1%8B>, с четкими температурами плавления. В среднем - около 2000С
В спектрах ЯМР 31P химически сдвиги для Фосфоновых кислот лежат в области 5-31 м д., полосы поглощения связи P = O в инфракрасных спектрах -в области 1150-1220 см −1.
Химические свойства: образование солей <https://ru.wikipedia.org/wiki/%D0%A1%D0%BE%D0%BB%D0%B8> с основаниями <https://ru.wikipedia.org/wiki/%D0%9E%D1%81%D0%BD%D0%BE%D0%B2%D0%B0%D0%BD%D0%B8%D0%B5_(%D1%85%D0%B8%D0%BC%D0%B8%D1%8F)>
Они бывают как кислыми, так и
средними, в зависимости от количества объёмов основания и кислоты, так как
фосфоновые кислоты двухосновны.
CH3-PO(OH)2+2NaOH=CH3-PO(ONa)23-PO(OH)2+NaOH=CH3-PO(OH)(ONa)
· образуют эфиры <https://ru.wikipedia.org/wiki/%D0%AD%D1%84%D0%B8%D1%80%D1%8B> и ангидриды <https://ru.wikipedia.org/wiki/%D0%90%D0%BD%D0%B3%D0%B8%D0%B4%D1%80%D0%B8%D0%B4%D1%8B>
Фосфонаты - сложные эфиры <https://ru.wikipedia.org/wiki/%D0%A1%D0%BB%D0%BE%D0%B6%D0%BD%D1%8B%D0%B5_%D1%8D%D1%84%D0%B8%D1%80%D1%8B> фосфоновых кислот <https://ru.wikipedia.org/wiki/%D0%A4%D0%BE%D1%81%D1%84%D0%BE%D0%BD%D0%BE%D0%B2%D1%8B%D0%B5_%D0%BA%D0%B8%D1%81%D0%BB%D0%BE%D1%82%D1%8B> общей формулы RP(O)(OR1)n(OH)2-n. В зависимости от числа гидроксильных групп фосфонаты делятся на первичные (n=1, кислые фосфонаты), и вторичные (п = 2, полные фосфонаты).
Фосфонаты с низшими алкильными, алкенильными и арильными заместителями - бесцветные жидкости, фосфонаты с высокими молекулярными массами - масла или кристаллы. Связи при атоме фосфора имеют тетраэдрическую конфигурацию, в ИК-спектрах присутствует характеристическая полоса связи P=O при 1200-1280 см−1.
Химические свойства: Первичные фосфонаты являются умеренно сильными кислотами (например, для n-ClC6H4P(O)(OC4H9)OH рКа = 1,7) и образуют соли аминами, вторичные образуют аддукты <https://ru.wikipedia.org/wiki/%D0%90%D0%B4%D0%B4%D1%83%D0%BA%D1%82> с кислотами Льюиса (например, с галогенидами бора).
Первичные фосфонаты при нагревании
диспропорционируют с образованием полифосфатов, вторичные диалкилфосфонаты при
нагревании выше 150°С разлагаются с образованием первичных фосфонатов и
алкенов:
RP(O)(CH2CH2R1)2
![]() RP(O)(OH)CH2CH2R1
+ R1CH=CH2
RP(O)(OH)CH2CH2R1
+ R1CH=CH2
При взаимодействии с
пятихлористым фосфором и первичные, и вторичные фосфонаты образуют
хлорангидриды фосфоновых кислот:
RP(O)R12
+ PCl5 ![]() RP(O)R1Cl
+ R1Cl + POCl3
RP(O)R1Cl
+ R1Cl + POCl3
6. Качественные
реакции
) Характерной реакцией на ионы NH4+
является реакция с щелочью. При нагревании выделяется газообразный аммиак,
который можно обнаружить по запаху или по посинению мокрой, красной лакмусовой
бумажки.
(NH4)2SO4 + 2KOH = K2SO4 + 2NH3 + H2O
NH4+ + SO42- + 2K+ + 2OH- = 2K+ + SO42- + 2NH3 + 2H2O
NH4+ + 2OH- = 2NH3 + 2H2O4+ + OH- = NH3 + Н2О
) 5NaNO2 + 3H2SO4
+ 2KMnO4 = 5NaNO3 + 2MnSO4 + 3H2O +
K2SO4
3) Реакция с медью и серной кислотой.
Анион NО3- восстанавливается металлической медью в
присутствии серной кислоты до оксида азота:
8NaNO3 + 4H2SO4
+ 3Cu = 2NO↑ + 3Сu(NO3)2
+ 4Н2O.
Выделяющийся оксид азота окисляется кислородом воздуха до бурого диоксида NO2: