Материал: Химия железа
Химия железа
Введение
Желе́зо - элемент восьмой группы четвёртого периода
периодической системы химических элементов
<#"814424.files/image001.gif">
Электронная
формула
s22s22p63s23p63d64s2
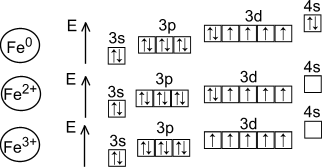
Характерные степени окисления:
|
Степень окисления |
Оксид |
Гидроксид |
Характер |
Примечания |
|
+2 |
FeO |
Fe(OH)2 |
Слабоосновный |
|
|
+3 |
Fe2O3 |
Fe(OH)3 |
Очень слабое основание, иногда - амфотерный |
|
|
+6 |
Не получен |
<H2FeO4>* |
Кислотный |
Сильный окислитель |
* Кислота в свободном виде не существует - получены только её соли
Для железа характерны степени окисления - +2 и +3.
Степени окисления +2 соответствует чёрный оксид FeO и зелёный гидроксид Fe(OH)2. Они имеют основный характер. В солях Fe(+2) присутствует в виде катиона. Fe(+2) - слабый восстановитель.
Степени
окисления +3 соответствуют красно-коричневый оксид Fe2O3 и коричневый гидроксид
Fe(OH)3. Они носят амфотерный характер, хотя и кислотные, и основные свойства у
них выражены слабо. Так, ионы Fe3+ нацело гидролизуются
<#"814424.files/image003.gif">
Железо (+3) чаще всего проявляет слабые окислительные свойства.
Степени окисления +2 и +3 легко переходят между собой при изменении окислительно-восстановительных условий.
Кроме того, существует оксид Fe3O4, формальная степень окисления железа в котором +8/3. Однако этот оксид можно также рассматривать как феррит железа (II) Fe+2(Fe+3O2)2.
Также
существует степень окисления +6. Соответствующего оксида и гидроксида в
свободном виде не существует, но получены соли - ферраты (например, K2FeO4).
Железо (+6) находится в них в виде аниона. Ферраты являются сильными
окислителями.
Нахождение
железа в природе
Железные руды довольно широко распространены на Земле. Названия гор на Урале говорят сами за себя: Высокая, Магнитная, Железная. Агрохимики в почвах находят соединения железа.
Железо входит в состав большинства горных пород. Для получения железа используют железные руды с содержанием железа 30-70% и более.
Основными железными рудами являются:
Магнетит (магнитный железняк) - Fe3O4 содержит 72% железа, месторождения встречаются на Южном Урале, Курской магнитной аномалии.
Гематит (железный блеск, кровавик) - Fe2O3 содержит до 65% железа, такие месторождения встречаются в Криворожском районе.
Лимонит (бурый железняк) - Fe2O3*nH2O содержит до 60% железа, месторождения встречаются в Крыму.
Пирит
(серный колчедан, железный колчедан, кошачье золото) - FeS2 содержит примерно
47% железа, месторождения встречаются на Урале.
Способы
получения железа
В настоящее время основным промышленным способом переработки железных руд является производство чугуна доменным процессом. Чугун - это сплав железа, содержащий 2,2-4% углерода, кремний, марганец, фосфор, серу. В дальнейшем большая часть чугуна подвергается переделу на сталь. Сталь отличается от чугуна главным образом меньшим содержанием углерода (до 2%), фосфора и серы.
В последнее время большое внимание уделяется разработке методов прямого получения железа из руд без осуществления доменного процесса. Еще в 1899 г. Д. И. Менделеев писал: "Я полагаю, что придет со временем опять пора искать способов прямого получения железа и стали из руд, минуя чугун". Слова великого химика оказались пророческими: такие способы найдены и реализованы в промышленности.
Первоначально прямое восстановление железа проводили в слегка наклонных вращающихся печах, похожих на печи, в которых получают цемент. В печь непрерывно загружают руду и уголь, которые постепенно перемещаются к выходу, противотоком идет нагретый воздух. За время нахождения в печи руда постепенно подогревается (до температур ниже температуры давления железа) и восстанавливается. Продуктом такого производства является смесь кусков железа и шлака, которую легко разделить, так как железо до плавления не доводится.
Интерес к прямому восстановлению железа из руд возрос и последнее время в связи с тем, что, кроме экономии кокса, оно дает возможность получать железо высокой чистоты. Получение чистых металлов - одна из важнейших задач современной металлургии. Такие металлы необходимы многим отраслям промышленности.
Получить технически чистое железо прямым восстановлением можно, если руду подвергнуть обогащению: существенно повысить массовую долю железа, отделив пустую породу, и снизить содержание вредных примесей (таких, как сера и фосфор).
Упрощенно процесс подготовки железной руды к восстановлению можно представить так. Руду измельчают в дробильных устройствах и подают на магнитный сепаратор. Он представляет собой барабан с электромагнитами, на который при помощи транспортера подается измельченная руда. Пустая порода свободно проходит через магнитное поле и падает. Зерна руды, содержащие магнитные минералы железа, намагничиваются, притягиваются и отделяются от барабана позднее пустой породы. Такую магнитную сепарацию можно повторить несколько раз.
Лучше
всего подвергаются магнитному обогащению руды, содержащие магнетит Fе3О4,
который обладает сильными магнитными свойствами. Для слабомагнитных руд иногда
перед обогащением применяют магнетизирующий обжиг - восстановление оксидов
железа в руде до магнетита:
Fe2O2 + H2 = 2Fe3O4 + H2O
или
ЗFе2О3
+ CO = 2Fе3О4 + CO2
После магнитной сепарации руду обогащают методом флотации. Для этого руда помещается в емкость с водой, где растворяют флотационные реагенты - вещества, которые избирательно адсорбируются на поверхности полезного минерала и не адсорбируются на пустой породе. В результате адсорбции флотореагента частицы минерала не смачиваются водой и не тонут.
Через раствор пропускают воздух, пузырьки которого прикрепляются к кусочкам минерала и поднимают их на поверхность. Частицы пустой породы хорошо смачиваются водой и падают на дно. Обогащенную руду собирают с поверхности раствора вместе с пеной.
В результате полного процесса обогащения содержание железа в руде может быть повышено до 70-72%. Для сравнения отметим, что содержание железа в чистом оксиде Fе3О4 составляет 72,4%. Так что содержание примесей в обогащенной руде весьма незначительно. К настоящему времени предложено более семидесяти методов прямого получения железа из руд с использованием твердых и газообразных восстановителей. Рассмотрим принципиальную схему одного из них, который используется в нашей стране.
Процесс проводят в вертикальной печи, в которую сверху подают обогащенную руду, а снизу - газ, служащий восстановителем. Этот газ получают конверсией природного газа (т.е. сжиганием природного газа в недостатке кислорода). "Восстановительный" газ содержит 30% СО, 55% Н2 и 13% воды и углекислого газа. Следовательно, восстановителями оксидов железа служат оксид углерода (II) и водород:
O4 + 4H2 = 3Fe + 4H2OO4 + 4CO = 3Fe + 4CO2
Восстановление ведется при температуре 850 - 900°С, что ниже температуры плавления железа (1539°). СО и Н2, которые не прореагировали с оксидами железа, вновь возвращаются в печь после удаления из них пыли, воды и углекислого газа. Эти "оборотные газы" служат и для охлаждения получаемого продукта. В результате процесса прямого восстановления руды получается железо в виде металлических "окатышей" или "губки", содержание металла в которых может достигать 98 - 99%. Если прямым восстановлением получают сырье для дальнейшей выплавки стали, то оно обычно содержит 90 - 93% железа.
Для многих современных отраслей техники требуется железо еще, более высокой степени чистоты. Очистку технического железа проводят карбонильным методом. Карбонилы - это соединения металлов с оксидом углерода (II) СО. Железо взаимодействует с СО при повышенном давлении и температуре 100-200°, образуя пентакарбонил:
е
+ 5СО = Fе(СО)5
Пентакарбонил железа - жидкость, которую можно легко отделить от примесей перегонкой. При температуре около 250° карбонил разлагается, образуя порошок железа:
е(СО)5
= Fе + 5СО
Если полученный порошок подвергнуть спеканию в вакууме или атмосфере водорода, то получится металл, содержащий 99,98- 99,999% железа. Еще более глубокой степени очистки железа (до 99,9999%) можно достичь методом зонной плавки.
Железо высокой чистоты нужно прежде всего для изучения его свойств, т.е. для научных целей. Если не удалось бы получить чистое железо, то не узнали бы, что железо - мягкий, легко обрабатываемый металл. Химически чистое железо намного более инертно, чем железо техническое.
Важной
отраслью использования чистого железа является производство специальных
ферросплавов, свойства которых ухудшаются в присутствии примесей
Физические
свойства простого вещества железа
Железо - типичный металл, в свободном состоянии - серебристо-белого цвета с сероватым оттенком. Чистый металл пластичен, различные примеси (в частности - углерод) повышают его твёрдость и хрупкость. Обладает ярко выраженными магнитными свойствами. Часто выделяют так называемую «триаду железа» - группу трёх металлов (железо Fe, кобальт Co, никель Ni), обладающих схожими физическими свойствами, атомными радиусами и значениями электроотрицательности.
Для железа характерен полиморфизм, оно имеет четыре кристаллические модификации:
· до 769 °C существует α-Fe (феррит) с объёмноцентрированной кубической решёткой и свойствами ферромагнетика (769 °C ≈ 1043 K - точка Кюри для железа);
· в температурном интервале 769-917 °C существует β-Fe, который отличается от α-Fe только параметрами объёмноцентрированной кубической решётки и магнитными свойствами парамагнетика;
· в температурном интервале 917-1394 °C существует γ-Fe (аустенит) с гранецентрированной кубической решёткой;
Металловедение не выделяет β-Fe как отдельную фазу и рассматривает её как разновидность α-Fe. При нагреве железа или стали выше точки Кюри (769 °C ≈ 1043 K) тепловое движение ионов расстраивает ориентацию спиновых магнитных моментов электронов, ферромагнетик становится парамагнетиком - происходит фазовый переход второго рода, но фазового перехода первого рода с изменением основных физических параметров кристаллов не происходит.
Для чистого железа при нормальном давлении, с точки зрения металловедения, существуют следующие устойчивые модификации:
· от абсолютного нуля до 910 °C устойчива α-модификация с объёмноцентрированной кубической (ОЦК) кристаллической решёткой;
· от 910 до 1400 °C устойчива γ-модификация с гранецентрированной кубической (ГЦК) кристаллической решёткой;
· от 1400 до 1539 °C устойчива δ-модификация с объёмноцентрированной кубической (ОЦК) кристаллической решёткой.
Явление полиморфизма чрезвычайно важно для металлургии стали. Именно благодаря α-γ переходам кристаллической решётки происходит термообработка стали. Без этого явления железо как основа стали не получило бы такого широкого применения.
Железо относится к умеренно тугоплавким металлам. В ряду стандартных электродных потенциалов железо стоит до водорода и легко реагирует с разбавленными кислотами. Таким образом, железо относится к металлам средней активности.
Температура плавления химически чистого железа равна 1539о С. Технически чистое железо, полученное путем окислительного рафинирования, плавится при температуре около 1530о С.
Теплота плавления железа составляет 15,2 кДж/моль или 271,7 кДж/кг.
Кипение железа происходит при температуре 2735о С, хотя авторами некоторых
исследований установлены значительно более высокие значения температуры кипения
железа (3227 - 3230о С). Теплота испарения железа составляет 352,5 кДж/моль или
6300 кДж/кг.
Химические свойства простого вещества железа
При
хранении на воздухе при температуре до 200 °C железо постепенно покрывается
плотной плёнкой оксида <#"814424.files/image004.gif">
С
разбавленной серной кислотой
<#"814424.files/image005.gif">
Концентрированные
азотная <#"814424.files/image006.gif">
Взаимодействие
с кислородом
<#"814424.files/image007.gif">
Сгорание
в чистом кислороде:
![]()
Пропускание
кислорода или воздуха через расплавленное железо:
![]()
Взаимодействие
с порошком серы <#"814424.files/image010.gif">
Взаимодействие
с галогенами
<#"814424.files/image011.gif">
При
повышенном давлении паров брома
<#"814424.files/image012.gif">
Взаимодействие
с йодом <#"814424.files/image013.gif">
Взаимодействие
с неметаллами
<#"814424.files/image014.gif">
С фосфором <#"814424.files/image015.gif">
![]()
![]()
С
углеродом <#"814424.files/image018.gif">
С
кремнием
<#"814424.files/image019.gif">
Взаимодействие
раскалённого железа с водяным паром:
![]()
Железо
восстанавливает металлы, которые в ряду активности стоят правее него, из
растворов солей:
![]()
Железо
восстанавливает соединения железа(III):
![]()
При
повышенном давлении металлическое железо реагирует с оксидом углерода(II) CO
<#"814424.files/image023.gif">
Из
солей железа(II) в водных растворах устойчива соль Мора
<#"814424.files/image024.gif">
который внутримолекулярно перегруппировывается в
гексацианоферрат (II) калия-железа (III):
![]()
Для
количественного определения железа (II) в растворе используют фенантролин
<#"814424.files/image026.gif">
Соли Fe3+ склонны к образованию кристаллогидратов. В них ион Fe3+ как правило окружен шестью молекулами воды. Такие соли имеют розовый или фиолетовый цвет.
Ион Fe3+ полностью гидролизуется даже в кислой среде.
При pH>4 этот ион практически полностью осаждается в виде Fe(OH)3:
![]()
При частичном гидролизе иона Fe3+ образуются многоядерные оксо- и гидроксокатионы, из-за чего растворы приобретают коричневый цвет.
Основные свойства гидроксида железа(III) Fe(OH)3
выражены очень слабо. Он способен реагировать только с концентрированными
растворами щелочей:
![]()
Образующиеся при этом гидроксокомплексы железа(III) устойчивы только в сильно щелочных растворах. При разбавлении растворов водой они разрушаются, причём в осадок выпадает Fe(OH)3.
При сплавлении со щелочами и оксидами других металлов Fe2O3 образует разнообразные ферриты <#"814424.files/image003.gif">
Соединения железа(III) в растворах восстанавливаются
металлическим железом:
![]()
Железо(III)
способно образовывать двойные сульфаты с однозарядными катионами
<#"814424.files/image029.gif">
Количественно
ионы Fe3+ определяют по образованию красных (в слабокислой среде) или жёлтых (в
слабощелочной среде) комплексов с сульфосалициловой кислотой
<#"814424.files/image030.gif">