Материал: Жданов-18.70
![]()
Для определения, например, средней мольной теплоемкости в пределах температуры от t1 до t2 надо из соответствующей таблицы взять теплоемкость cm1 и cm2 соответственно в пределах (0 – t1) оС и (0 – t2) оС (средние теплоем-
![]()
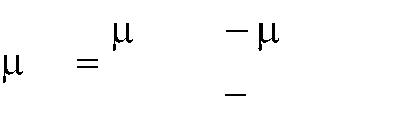
кости помечаются индексом m). Затем по выражению |
cm |
c m t 2 |
c m t1 |
рас- |
|
2 |
1 |
|
|||
|
|
|
|
||
|
|
t 2 |
t1 |
|
|
считать искомую теплоемкость.
Если в процессе участвуют G кг вещества, то количество теплоты в соот-ветствующем процессе определяется по выражению [7]:
-
Q G(c m
t
2
c m t 1 ) .
(1.13)
2
1
![]()
pv-диаграмме линия, изображающая политропный процесс, строится в
соответствии с уравнением pvn = const, где n – показатель политропы. Связь между основными параметрами рабочего тела в политропном процессе выра-жается следующими формулами:
-
p
/ p
2
v
/ v
2
n ;
(1.14)
1
1
T
/ T
v
1
/ v
2
n-1 ;
(1.15)
2
1
n-1
(1.16)
T2 / T1
p1 / p2
.
n
![]()
![]()
![]()
![]()
![]()
![]()
Для адиабатного процесса в формулах (1.14) – (1.16) показатель n заменя-ется показателем адиабаты k = сp/cv.
18
![]()
![]() Изменение
внутренней энергии u1
2 , энтальпии
h1 2
и энтропии s1
2 не зависит
от характера процесса и при постоянной
теплоемкости 1 кг идеаль-ного газа
подсчитывается по формулам:
Изменение
внутренней энергии u1
2 , энтальпии
h1 2
и энтропии s1
2 не зависит
от характера процесса и при постоянной
теплоемкости 1 кг идеаль-ного газа
подсчитывается по формулам:
-
Δu1-2
u2
u1
cv t 2
t1
;
(1.17)
Δh1-2
h 2
h1
cp t 2
t1
;
(1.18)
Δs1-2
s2
s1
cln T2 / T1 .
(1.19)
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
выражении (1.19) с – теплоемкость соответствующего процесса. Для политропного процесса теплоемкость [5]
![]()
-
c n cv
n
k
.
(1.20)
n
1
Работа газа в политропном процессе, кДж,
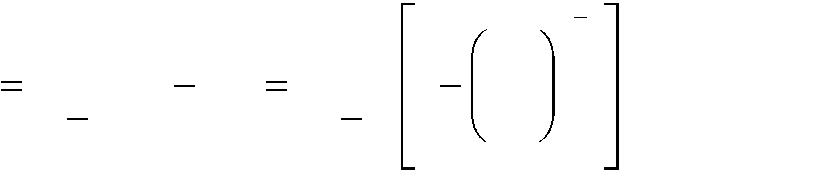
-
n
1
L
GR (T1 T2 )
GRT1 1
p2
n
.
(1.21)
n 1
n 1
p1
изотермическом процессе по первому закону термодинамики теплота равна работе процесса и может быть определена по формуле:
-
Q L GRTln
v2
GRTln
p1
.
(1.22)
v1
p2
![]()
В этом процессе изменение удельной энтропии [5]
-
s1 2
s2s1
R ln
v2
R ln
p1
q1 2
,
(1.23)
v1
p2
T
![]()
где q |
|
Q |
. |
|
2 |
|
|
||
1 |
G |
|
||
|
|
|
||
![]()
19
адиабатном процессе удельная работа равна изменению внутренней энергии с обратным знаком:
-
l L / G u1 u2 cv (t1 t2 ) .
(1.24)
![]()
Задачи № 12 – 18
Задачи решаются при помощи hs-диаграммы водяного пара, практическая часть которой состоит из двух областей [1]. Ниже пограничной кривой сухого насыщенного пара (степень сухости х = 1) будет область влажного насыщенно-го пара (0 < х < 1), выше – область перегретого пара. Поэтому, когда в задаче требуется определять состояние пара, нужно показать, в какой области диа-граммы находится точка данного состояния пара. В hs-диаграмме в области влажного пара соответствующие изобара и изотерма совпадают, так как в этой области определенному давлению соответствует определенная температура на-сыщения. В области перегретого пара изотермы отклоняются от изобар вправо, асимптотически приближаясь к горизонтальной линии.
Удельная внутренняя энергия пара u = h – pv (здесь необходимо обратить внимание на соответствие размерностей всех величин).
Удельная теплота в изобарном процессе равна изменению энтальпии в этом процессе, т. е. q1-2 = h2 – h1. В изотермическом процессе q1-2 = T(s2 – s1).
обратимом адиабатном процессе изменения состояния пара, протекаю-щем при постоянном значении энтропии, удельная работа l1-2 = u1 – u2 =
(h1 – p1v1) – (h2 – p2v2).
Процесс дросселирования пара условно изображается линией постоянной энтальпии.
Для влажного насыщенного пара [2 – 5] – удельный объем
![]()
vx v x v (1 x) ; энтальпия hx h rx ; энтропия sx s rx / Tн ; внутренняя
энергия
ux
![]()
hx
pvx .
Задачи № 19 – 22
Задачи составлены на процессы истечения и дросселирования газов и па-ров. Процесс истечения принимается без теплообмена, т. е. адиабатным, для ко-торого в указаниях к задачам 1 – 11 приведены формулы, связывающие основ-
20
ные параметры идеального газа, и неразрывным (сплошным), когда соблюдает-ся равенство (уравнение неразрывности):
![]()
-
Gv fc ,
(1.25)