Материал: Жданов-18.70
1.5. Методические указания к выполнению контрольной работы 1
Задачи № 1 – 11
Задачи составлены по разделам технической термодинамики: уравнение
состояния идеального газа, смесь идеальных газов, теплоемкость, первый закон 14
термодинамики и основные термодинамические процессы. При решении этих задач могут быть использованы следующие формулы и выражения.
Уравнение состояния идеального газа [2 – 8]:
для 1 кг –
![]()
-
pv RT ;
(1.1)
для G кг –
![]()
-
pv GRT ,
(1.2)
где v – удельный объем идеального газа, м3/кг; R = 8314/μ – газовая постоянная, Дж/(кг∙К);
– масса 1 моля газа, кг (численно равна молекулярной массе газа); р – абсолютное давление, Па:
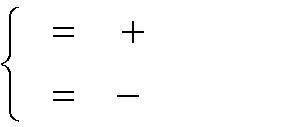
-
p
B
pм
;
(1.3)
p
B
pв ,
где рм – избыточное давление, измеряемое манометром, Па; рв – разряжение, измеряемое вакуумметром, Па;
– атмосферное (барометрическое) давление (В = 750 мм рт. ст. ≈105 Па), Па. Для газовых смесей вводят понятие о так называемой средней (кажущей-
ся) молекулярной массе смеси, значение которой определяется по выражениям:
через объемные доли [3] –
-
n
см
ri i ,
(1.4)
1
![]()
и через массовые доли –
-
n
см 1 / mi i ,
(1.5)
1
15
![]()
где μi – молекулярная масса компонента, входящего в смесь, кг/кмоль;
-
m
i
Gi
– массовая доля газа в смеси (отношение массы этого газа, входя-
G
![]()
щего в смесь, к массе всей смеси), кг;
r |
Vi |
– объемная доля (отношение приведенного объема какого–либо |
|
||
|
|
||||
i |
V |
|
|
|
|
|
|
|
|
||
газа, входящего в смесь, к объему всей смеси). |
|
|
|||
Формулы пересчета состава смеси [4 – 6]: |
|
|
|||
|
|
ri |
miμсм / μi ; |
(1.6) |
|
|
|
mi |
ri i / см , |
(1.7) |
|
![]()
![]()
![]()
Газовую постоянную смеси идеальных газов R можно определить или че-рез газовые постоянные отдельных компонентов Ri, входящих в смесь,
n
![]()
mi Ri , или по средней молекулярной массе смеси R = 8314/μсм, Дж/(кг∙К).
1
Для определения парциального давления отдельного компонента pi, вхо-
дящего в смесь, служат формулы p |
|
r p и p |
i |
m |
i |
Ri |
p , где р – полное давление |
|
|
|
|
||||||
|
i |
i |
|
R |
|
|||
смеси газов, Па. |
|
|
|
|
|
|
|
|
![]()
зависимости от выбранной количественной единицы вещества разли-
чают мольную теплоемкость μс, кДж/(кмоль∙К), массовую – с, кДж/(кг∙К), и
объемную – с´, кДж/(м3∙К). Объемную теплоемкость относят к 1 м3 при нор-мальных физических условиях (ро = 760 мм рт. ст. = 101325 Па, tо = 0 °С). Эти теплоемкости связаны между собой следующими зависимостями:
![]()
-
c
c c
;
(1.8)
0
c
c
c
0 ,
(1.9)
22, 4
![]()
где μ – молекулярная масса газа, кг/кмоль;
16
– плотность газа при нормальных физических условиях, кг/м3.
![]()
Мольная, массовая и объемная теплоемкости могут быть при постоянном давлении ср и при постоянном объеме сv. Отношение теплоемкостей при посто-янном давлении и постоянном объеме называют показателем адиабаты и обо-
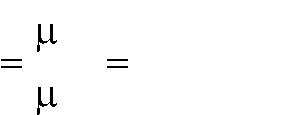
значают буквой k, т. е. k |
c p |
|
cp |
. |
|
|
|
|
|||
|
c v |
|
cv |
|
|
Теплоемкость газа зависит от его температуры. В приближенных расче-тах часто пренебрегают этой зависимостью и теплоемкость газов одинаковой атомности считают величиной постоянной. Значения мольных теплоемкостей и показателей адиабаты приведены в табл. 3.
|
|
Т а б л и ц а 3 |
|
|||
Значения мольных теплоемкостей и показателей адиабаты |
|
|
||||
|
|
|
|
|
||
Газы |
Удельная мольная теплоемкость, кДж/(кмоль∙К) |
k |
|
|||
|
|
|
||||
μсp |
μсv |
|
||||
|
|
|
||||
Одноатомные |
12,56 |
20,93 |
1,67 |
|
||
Двухатомные |
20,93 |
29,31 |
1,40 |
|
||
Трех- и многоатом- |
20,31 |
37,68 |
1,29 |
|
||
ные |
|
|||||
|
|
|
|
|||
Зависимости теплоемкостей газов от температуры имеют нелинейный ха-рактер. В источнике [7] в табл. П.1 приведены средние мольные теплоемкости некоторых газов в пределах от 0 до t, оС. При пользовании данными указанной таблицы в необходимых случаях требуется производить интерполяцию.
Для смесей идеальных газов [5, 6] теплоемкость определяется по формулам:
массовая –
-
n
ссм
mi c ;
(1.10)
1
![]()
объемная –
-
n
cсм
ri ci ;
(1.11)
1
17
![]()
мольная –
-
n
cсм
ri ci .
(1.12)
1