Материал: Гетероядерные комплексы в системах гадолиний(III)–марганец(II)/железо(III)/ - оксиэтилидендифосфоновая кислота как потенциальные МРТ контрастные реагенты
Скорость протонной магнитной релаксации в первой координационной сфере
парамагнитного комплекса обусловлена интенсивностью диполь-дипольных и
скалярных электронно-ядерных взаимодействий, а также связью их с «решеткой» -
со всеми не магнитными степенями свободы [40, 43, 44]. Скорости спин-решеточной
![]() и спин-спиновой
и спин-спиновой ![]() релаксации являются сложной
функцией, зависящей от многих параметров, которую можно записать согласно [37]
как:
релаксации являются сложной
функцией, зависящей от многих параметров, которую можно записать согласно [37]
как:
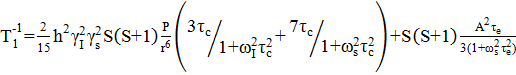
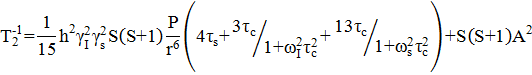
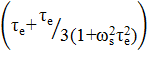 (7)
(7)
где:![]() и
и ![]() , - ларморовские частоты прецессий магнитных моментов ядра и
электрона; S - спин парамагнитного иона;
, - ларморовские частоты прецессий магнитных моментов ядра и
электрона; S - спин парамагнитного иона; ![]() и
и ![]() - гиромагнитное отношение
релаксирующего ядра и неспаренного электрона; r - расстояние между магнитными
моментами ядра и электрона; А - константы изотропного скалярного взаимодействия
времен корреляции для дипольного и скалярного взаимодействий
- гиромагнитное отношение
релаксирующего ядра и неспаренного электрона; r - расстояние между магнитными
моментами ядра и электрона; А - константы изотропного скалярного взаимодействия
времен корреляции для дипольного и скалярного взаимодействий ![]() и
и ![]() ; Р - вероятность нахождения протона
в сольватной сфере парамагнитного иона
; Р - вероятность нахождения протона
в сольватной сфере парамагнитного иона
![]() ;
;
n - число молекул воды в первой координационной сфере; В - концентрация
парамагнитного иона, моль/л; ![]() -концентрация воды, моль/л [35, 36, 45].
-концентрация воды, моль/л [35, 36, 45].
Согласно [35, 46] корреляционным временем диполь-дипольного
взаимодействия ![]() может быть время броуновской диффузии парамагнитного
комплекса
может быть время броуновской диффузии парамагнитного
комплекса ![]() , время электронной релаксации
, время электронной релаксации ![]() и время жизни протона в первой
координационной сфере парамагнитного иона
и время жизни протона в первой
координационной сфере парамагнитного иона ![]() или время корреляции обменных
взаимодействий:
или время корреляции обменных
взаимодействий:
![]() (8)
(8)
Для гадолиния (III),
марганца (II) и железа(III) ![]() [30, 43].
[30, 43].
Корреляционное время ![]() - является характеристикой какого-либо случайного процесса
(броуновское движение, обмен лигандов и так далее), в котором генерируется
Фурье-компонента электромагнитного поля с резонансной частотой. Согласно [46,
47]
- является характеристикой какого-либо случайного процесса
(броуновское движение, обмен лигандов и так далее), в котором генерируется
Фурье-компонента электромагнитного поля с резонансной частотой. Согласно [46,
47]![]() - постоянная времени спада
корреляционной функции; спектральная плотность
- постоянная времени спада
корреляционной функции; спектральная плотность ![]() , определяющая интенсивность
компоненты с частотой
, определяющая интенсивность
компоненты с частотой ![]() , есть Фурье преобразование корреляционной функции [44]. Так как скорости спин-решеточной и спин-спиновой релаксации
линейно зависят от концентрации парамагнитного иона B, то можно записать:
, есть Фурье преобразование корреляционной функции [44]. Так как скорости спин-решеточной и спин-спиновой релаксации
линейно зависят от концентрации парамагнитного иона B, то можно записать:
![]() (9)
(9)
КРЭ является характеристическим параметром, отражающим изменение в
геометрическом и электронном строении первой координационной сферы
парамагнитного иона. В растворе, содержащем ион-комплексообразователь и лиганд,
существует набор различных парамагнитных комплексов, находящихся в равновесии.
Каждый комплекс дает независимый вклад в скорость релаксации протонов [30]:
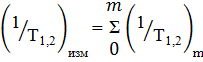 , (10)
, (10)
Используя формулу (8), получаем:
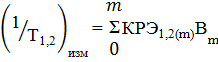 (11)
(11)
Учитывая, что общая концентрация парамагнитного иона выражается как сумма
концентраций всех комплексных частиц, включающих этот ион:
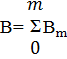 , (12)
, (12)
где Bm- равновесная концентрация
комплексных форм. Из формул (9), (10) и (11) получаем:
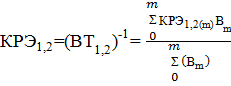 (13)
(13)
Измеряемый коэффициент релаксационной эффективности (или релаксивность R2 в англоязычной литературе) является аддитивной величиной и функцией образования в физико-химических приложениях метода протонной магнитной релаксации. Данное свойство релаксационной эффективности служит физико-химическим откликом и дает возможность определять состав и устойчивость парамагнитных комплексов в растворах при математическом моделировании зависимостей [30, 48].
2.2.3 Метод математического моделирования
Обработку экспериментальных зависимостей тех или иных физико-химических свойств от состава растворов проводили по программе СPESSP (Complex formation Parameters of Еquilibria in Solutions with Solid Phases) [49]. Программа реализована на IBM PC AT и позволяет обрабатывать данные различных методов исследования (ЯМР, рН-метрия, потенциометрия, поляриметрия, спектрофотометрия и т.д.), характеристический параметр которых подчиняется правилу аддитивности.
Рассматриваемая программа позволяет в случае многокомпонентных систем
определять константы образования и физико-химические параметры комплексов. Суть
программы заключается в нахождении в ходе итерационной процедуры минимума
функционала F:
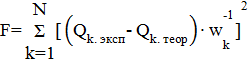 , (14)
, (14)
где Qk,эксп и Qk,теор - экспериментально измеряемое
свойство раствора в k-том эксперименте и его теоретический аналог, N - число экспериментов,
wk-cреднеквадратичная ошибка. При этом
![]() , (15)
, (15)
здесь ![]() и
и ![]() - константа образования и физико-химический параметр i-го
комплекса,
- константа образования и физико-химический параметр i-го
комплекса, ![]() - его доля накопления,
- его доля накопления, ![]() - матрица стехиометрических
коэффициентов.
- матрица стехиометрических
коэффициентов.
Оценка достоверности полученных результатов проводится по критерию
Фишера:
![]() , (16)
, (16)
где σ и σэксп - дисперсии расчета и эксперимента соответственно, u1 и u2 - число степеней свободы числителя и знаменателя (16), р - заданный уровень значимости критерия.
Так как
![]() , (17)
, (17)
![]() (18)
(18)
Выполнение неравенства (18) означает, что найденное решение соответствует истинному с вероятностью, близкой к (1-р).
Построение математической модели процессов комплексообразования, сольватации или ассоциации частиц равновесной системы состоит из этапов:
. Выбор первоначальной модели на основании аналитических и графических методов, литературных данных для сходных систем. Задание нулевого приближения.
. Нахождение в ходе математической обработки минимума целевой функции (![]() ) и оценка по критерию адекватности
(16) согласия модели с экспериментом.
) и оценка по критерию адекватности
(16) согласия модели с экспериментом.
. Последовательное усложнение (если модель не достоверна по критерию Фишера) структуры модели осуществляется за счет включения в нее дополнительных равновесий образования молекулярных или ион-молекулярных ассоциатов.
Таким образом, достоверной можно считать модель в том случае, если она, -
во-первых, адекватно описывает экспериментальные данные и, - во-вторых, если
добавление в нее новых, “разумных” с точки зрения химизма процессов, не дает ощутимого вклада в
![]() .
.
Подробно этапы моделирования многокомпонентных систем по данным различных физических и физико-химических методов приведены в монографии [49].
Была использована последняя версия программы CPESSP, которая позволяет
учитывать влияние изменения ионной силы раствора на активности участников
моделируемых равновесий по уравнению Девис-Васильева [48].
ГЛАВА 3. КОМПЛЕКСООБРАЗОВАНИЕ В СИСТЕМЕ "Gd(III)-Mn(II)-HEDP"
Было проведено pH-метрическое титрование при различных концентрациях, указанных в табл. 5.
Сравнение (рис. 3) экспериментальных кривых и теоретических кривых,
рассчитанных без учета образования гетероядерных комплексов на основе данных по
гомоядерным системам [28, 29] (табл. 3, 4) и протолитическим свойствам HEDP [9] (табл. 1) показало их
существенные отличия, что свидетельствует о гетероядерном комплексообразовании.
Табл. 3 Матрицы стехиометрии и константы образования в системе Mn(II) -
HEDP [29]
№
Равновесие
n
lgKр, δ≤0.16
lgβ, δ≤0.2
1
Mn2+ + H4L 4.0
-12.47
11.2
2
Mn2+ + 2H4L 3.0
-0.78
5.5
3
Mn2+ + 2H4L 4.0
-2.50
6.8
4
Mn2+ + 2H4L 5.0
-7.20
9.7
5
Mn2+ + 2H4L 6.0
-13.77
10.6
6
Mn2+ + 2H4L 7.0
-21.49
14.4
7
Mn2+ + 2H4L 8.0
-31.28
16.1
8
2Mn2+ + 2H4L 2.5
-4.21
12.7
9
2Mn2+ + 2H4L 3.0
-8.55
15.9
10
2Mn2+ + 2H4L 3.5
-14.75
21.2
Табл.4 Матрица стехиометрии и константы
образования иустойчивости в системе «Gd3+ - HEDP» [28]
№
H4L l*)
Gd3+
m*)
K+ k*)
-H+ h*)
n
Форма
lgКр
δ≤0.19
lgβуст. (lgПР) δ≤0.4
1
1
1
0
2
2.0
GdH2L+
14.31
19.0
2
2
1
0
1
0.5
GdH7L22+
22.58
24.3
3
2
1
0
3
1.5
GdH5L20
19.87
26.2
4
2
1
0
4
2.0
GdH4L2-
19.03
28.4
5
2
1
0
5
2.5
GdH3L22-
12.87
29.8
6
2
2
0
8
4.0
Gd2L22-
20.17
67.6
7
2
2
0
9
4.5
Gd2L2(OH)3-
11.82
73.2
8
1
2
0
2
2.0
Gd2H2L4+
17.12 9
1
2
0
3
3.0
Gd2HL3+
16.70
28.9
10
1
2
0
4
4.0
Gd2L2+
13.48
37.2
11
1
2
0
5
5.0
Gd2L(OH)+
6.38
44.1
12
1
2
0
6
6.0
Gd2L(OH)2↓
-1.60**)
(-50.1)
13
2
2
0
6
3.0
Gd2H2L2↓
-30.20**)
(-54.6)
14
3
2
0
6
2.0
Gd2H6L3↓
-42.61**)
(-56.5)
15
2
2
1
7
3.5
KGd2HL2↓
-30.49**)
(-66.4)
16
2
2
1
9
4.5
K3Gd2L2(OH)↓
-20.45**)
(-81.9)
*) для равновесия: **)для растворения осадка: Введение в матрицу кроме гадолиниевых и марганцевых комплексов, а также
кислотно-основных свойств HEDP
[9] дополнительно различных гетероядерных форм, способствовало значительному улучшению общей картины, при этом
математическое моделирование дало возможность корректно описать данную систему
(табл. 6); F-критерий Фишера составил 0.20 (рис. 4).
Итоговые данные по стехиометрии и константам образования соответствующих
форм приведены в таблице 6, а доли накопления форм в зависимости от
концентрационных условий (табл. 5) - на рисунках 5-8.
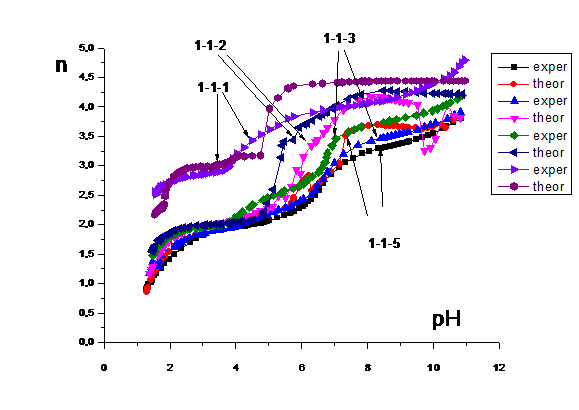
Рис.3 Экспериментально полученные и
теоретически рассчитанные с использованием только гомоядерных форм комлексов
кривые зависимости функции Бьеррума (1-я базисная частица - лиганд) от pH
Табл. 5 Концентрационные условия для
системы "Gd-Mn-HEDP" (Vнач.=50м(для pH-потенциометрии), T=250C)
№
CMn2+
CGd3+
CHEDP
CKOH
Условное обозначение
1
0,00965
0,01008
0,0575
0,225
1-1-5
2
0,00965
0,01008
0,0345
0,1313
1-1-3
3
0,00965
0,0108
0,0230
0,0925
1-1-2
4
0,00965
0,0102
0,0115
0,0441
1-1-1
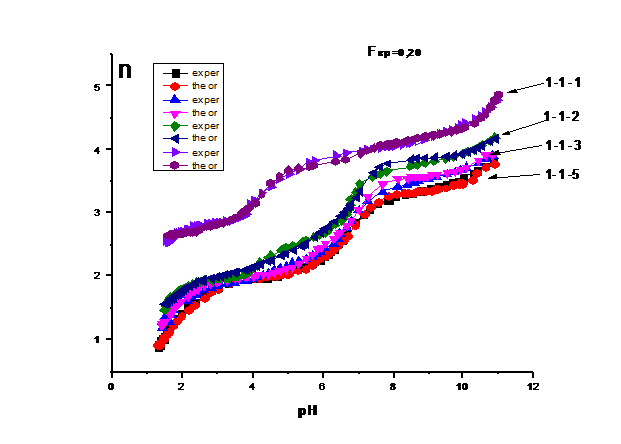
Рис. 4 Экспериментально и теоретически
полученные кривые: зависимости функции Бьеррума (1-я
базисная частица - лиганд) от pH; Fкр=0,20.
Табл. 6 Матрицы стехиометрии и константы
образования в системе Gd(III) - Mn(II) - HEDP
№
Равновесие
n
lgKр, δ≤0.20
lgβ, (lgПР), δ≤0.3
1
Mn2+ + 2H4L 4.0
-31.28
16.1
2
Gd3+ + 2H4L 2.0
19.03
28.4
3
Gd3++Mn2+ +
2H4L 1.5
31.91
37.5
4
Gd3++Mn2+ +
2H4L 2.0
30.26
39.6
5
Gd3++Mn2+ +
2H4L 2.5
26.28
43.0
6
Gd3++Mn2+ +
2H4L 3.0
20.44
45.0
7
Gd3++ Mn2+ +
2H4L 3.5
13.01
49.3
8
Gd3++ Mn2+ +
2H4L 4.0
5.72
53.1
9
Gd3++ Mn2+ +
2H4L 4.5
-5.73
55.6
10
Gd3+ +Mn2+ +
3H4L 1.7
30.91
52.4
11
Gd3+ +Mn2+ +
3H4L 2.0
29.34
43.4
12
2Gd3+ + 2H4L 4.5
-20.45*)
(-81.9)
13
Gd3+ + H4L 2.0
14.31
19.0
14
2Gd3+ + 2H4L+K+ 3.5
-30.49*)
(-66.4)
15
2Gd3+ +2Mn2+
+ 2H4L 3.0
37.72
62.2
16
Gd3+ +Mn2+ +
H4L 4.0
14.02
37.7
17
Gd3+ +Mn2+ +
H4L 6.0
-6.99*)
44.71
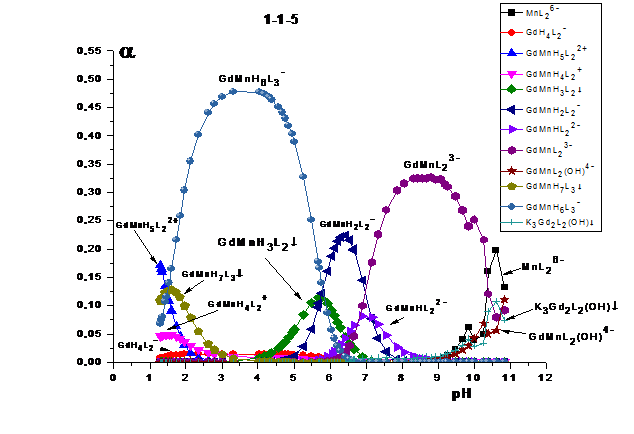
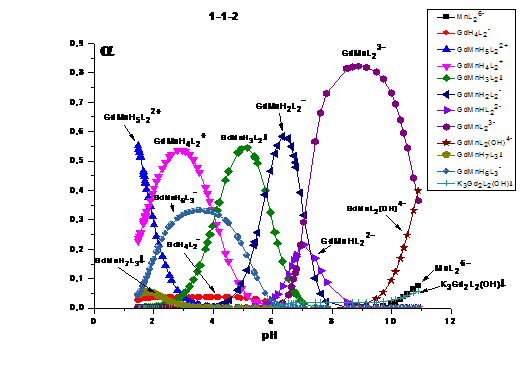
*)для растворения осадка: Рис.5 Зависимости долей накопления (по
отношению к металлу) от pH
среды при СMn(II)=0,00965 моль/л,CGd(III)=0,01008 моль/л и СHEDP=0,0575 моль/л
Рис. 6 Зависимости долей накопления (по отношению к
металлу) от pH среды при СMn(II) =0,00965 моль/л, CGd(III) =0,01008
моль/л и СHEDP=0,0345 моль/л
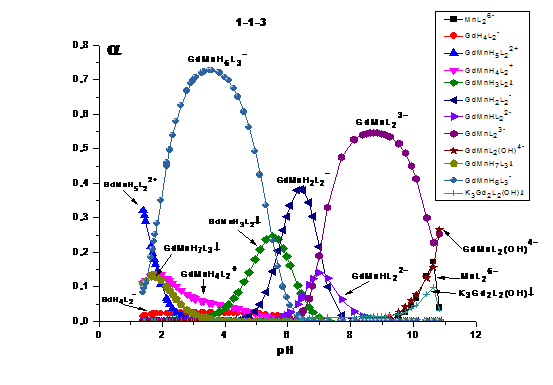
Рис. 7Зависимости долей накопления (по
отношению к металлу) от pH среды при СMn(II) =0,00965 моль/л, CGd(III)
=0,0108 моль/л и СHEDP=0,0230 моль/л
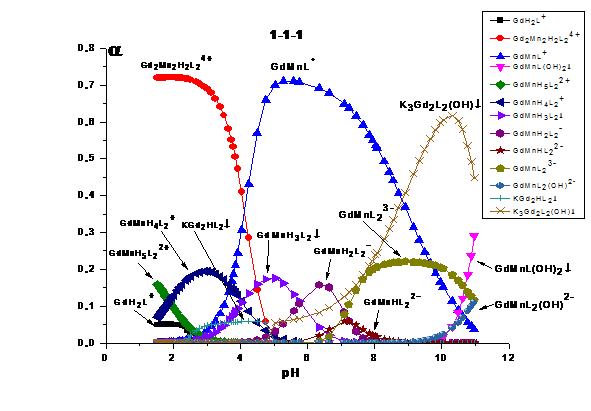
Рис. 8 Зависимости
долей накопления (по отношению к металлу) от pH среды при СMn(II)
=0,00965 моль/л, CGd(III) =0,0102 моль/л и СHEDP=0,0115
моль/л
Таким образом, методом рН-потенциометрии нами была изучена
гетероядерная система Gd3+ - Mn2+ - HEDP, при концентрации
марганца (II) 0,00965 моль/л, концентрации Gd (III) в диапазоне 0,0102-0,0108моль/л
и при разных концентрациях лиганда (табл. 5). Было установлено, что в системе Gd3+ - Mn2+ - HEDP
при значительном избытке лиганда преимущественно накапливаются биядерные (GdMnH6L3-1,GdMnL23-, GdMnH2L2-1) комплексы. При незначительном избытке лиганда наблюдается большее разнообразие
преимущественно накапливающихся гетероядерных форм (GdMnH5L22+,GdMnH4L2+,GdMnH3L20,GdMnH2L2-1, GdMnL23-), а в
отсутствие избытка лиганда наибольшая доля накопления наблюдалась у комплексов,
накопление которых в остальных сериях не наблюдалось, без учета калиевого
комплекса, накопление которого в остальных сериях не превышает 10-11% (Gd2Mn2H2L24+ GdMnL+, K3Gd2L2(OH)↓). В
системе также присутствуют небольшие доли моноядерных
бискомплексов (GdH4L2-, GdH2L+), а в щелочной среде при избытке лиганда
наблюдается накопление гомоядерного комплекса марганца (MnL26-). Для каждой из форм
были рассчитаны константы устойчивости (табл. 6). При значительном избытке
лиганда (рис.5,6) комплексообразование протекает по следующей схеме:
GdMnH3L2
GdMnH5L22- GdMnH3L2
Картина комплексообразования несильно меняется в случае с
небольшим избытком лиганда (рис.7):
GdMnH6L31- GdMnH5L22+ GdMnL2(OH)2- Значительные изменения происходят в процессе
комплексообразования при равных соотношениях металл: металл: лиганд(рис.8):
GdMnH5L22- Как следует из ранее полученных данных, в системе Mn2+ - HEDP
образуется[29] 10 комплексных форм (из них 3 - биядерные), а в системе Gd3+
- HEDP образуется[28] - 16 комплексных форм (из них 3 - биядерные). При этом
следует заметить, что комплексы марганца(II) существенно менее прочные, чем
комплексы гадолиния(III). При совместном же присутствии в растворе обоих катионов
уже в сильнокислой области рН наблюдается накопление гетероядерных форм,
которые с ростом рН, в результате процесса удаления протона, переходят в
гетероядерные комплексы с соотношениями Gd:Mn:HEDP, равным 1:1:1, 1:1:2 и
1:1:3. При этом из гомоядерных форм в растворе обнаруживаются лишь пять
комплексов: MnL26- , GdH4L2-,
GdH2L+ , KGd2HL2↓, K3Gd2L2(OH)↓.
Таким образом, гетероядерные комплексы существенно более
прочные и замещают гомоядерные формыMn(ii), не давая им накапливаться в растворе.
Причиной этого может быть существенно меньший радиус (в 1.5 раза) иона
марганца(II) по сравнению с ионом гадолиния(III), что уменьшает
межкатионное отталкивание в структуре гетероядерных комплексов. Такая же
ситуация реализуется в системах гадолиний(III) - кальций(II) - HEDP[28] и эрбий(III) - кальций(II) - HEDP[11]. Не исключено
также, что комбинация "жесткого", орбитально контролируемого
ковалентного связывания ионов марганца(II) и
"подвижного" электростатического ионного взаимодействия с
нуклеофильными центрами лиганда в случае гадолиния(III) приводит к
энергетически оптимальным конфигурациям гетероядерных комплексов.
Также нашей исследовательской группой, были обработаны
магнитно-релаксационные характеристики по 3-м сериям и проведены сравнительные
измерения спин-спинового коэффициента релаксационной эффективности в
гетероядерной и гомоядерных системах для одинаковых концентрационных условий и
физиологическом значении рН (7.4). КРЭ2 для марганец-содержащей
системы[29] составляет 2500 л·моль-1·с-1, для
гадолиний-содержащей системы[3] - 5500 л·моль-1·с-1. В
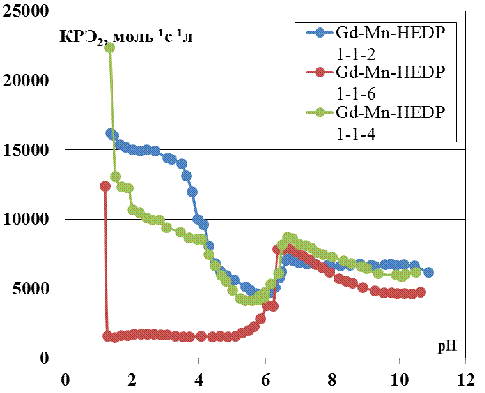
гетероядерной системе КРЭ2 имеет значение 6700 л·моль-1·с-1(рис.
9) (при расчете использовалась сумма концентраций парамагнетиков). Таким
образом, гетероядерная система как контрастный реагент является более предпочтительной
в МРТ.
Рис. 9 Зависимость коэффициента релаксационной
эффективности от pH для различных серий
Кроме того было промоделировано введение раствора (при СMn2+=
0.00965 моль/л, CGd3+= 0.0108 моль/л, СHEDP=
0.0230 моль/л, рН=7,40) с гетероядерными соединениями в организм человека,
предусматривающее 1000-кратное (5мл. раствора на 5л. крови человека)
разбавление. Расчет показал, что свободные катионы отсутствуют ([Mn2+]~10-11
моль/л, [Gd3+] ~10-18 моль/л), а в растворе находятся
лишь три комплекса и они - гетероядерные: GdMnH2L21-, GdMnHL22-, GdMnL23-, доли которых
соответственно составляют 30, 29 и 41%. Таким образом, следует полагать, что
использование выбранной системы в качестве МРТ-контрастного реагента может быть
оправдано и с точки зрения достаточной прочности накапливающихся комплексов.
Было проведено pH-метрическое
титрование при различных концентрациях, указанных в таблице7.Сравнение (рис.
10) экспериментальных кривых и кривых, рассчитанных без учета образования
гетероядерных комплексов на основе данных по гомоядерным системам (табл. 4, 8)
и протолитическим свойствам HEDP
[9] (табл. 1), показало их существенные отличия, что свидетельствует о
гетероядерном комплексообразовании.
Рис. 10 Экспериментально полученные и
теоретически рассчитанные с использованием форм гомоядерных комплексов кривые
зависимости функции Бьеррума (1-ая базисная - Gd(iii)) от pH.
Табл.7 Концентрационные условия для системы«Gd(III) - Fe(III) - HEDP» (Vнач.=
25 мл, T = 25 0C).
№
CоFe3+, моль/л
CоFe3+, моль/л
CоHEDP, моль/л
CоKOH, моль/л
Условное обозначение
1
0.0114
0.0104
0.0121
0.0497
1-1-1
2
0.0114
0.0104
0.0241
0.0993
1-1-2
3
0.0114
0.0104
0.0482
0.1924
1-1-4
4
0.0114
0.0104
0.0723
0.2880
1-1-6
Таблица 8 Матрицы стехиометрии и константы образования (lgKр)и константы устойчивости (lgβ)в системе Fe(III) - HEDP[10]
№
Равновесие
n
lgKр, δ≤0.2
lgβ, δ≤0.3
1
Fe3+ + H4L 4.0
10.6
33.7
2
Fe3+ + H4L 5.0
3.0
12.8
3
Fe3+ + 2H4L 9.0
-19.4
14.4
4
Fe3+ + 2H4L 7.0
-11.0
24.9
5
3Fe3+ + 3H4L 3.3
42.3
90.4
6
Fe3+ + 3H4L 6.0
12.2
26.2
7
Fe3+ + 3H4L 7.0
8.0
29.6
8
2Fe3+ + 2H4L 4.5
16.1
49.5
Добавление в матрицу различных гетероядерных форм, по принципам,
изложенным в разделе 2.2.3., способствовало значительному улучшению общей
картины. При этом математическое моделирование дало возможность корректно
описать данную систему; F-критерий
Фишера составил 0.31 (рис.11).
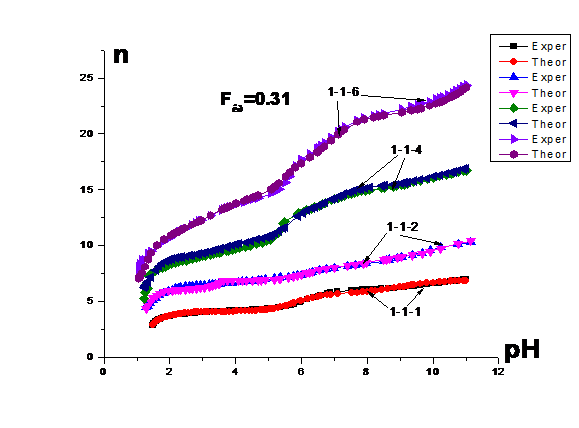
Рис. 11 Экспериментально
и теоретически рассчитанные(табл.9) кривыезависимости функции Бьеррума (1-ая
базисная - Gd(iii))от pH.
Табл. 9 Матрицы стехиометрии и константы
образования в системе Gd(III ) -Fe(III) - HEDP
№
Gd3+
Fe3+
H4L
K+
H+
n
Форма
lgКр, δ≤0.19
lgβуст. (lgПР) δ≤0.4
1
0
1
1
0
4
4
FeL-
10.16
33.7
2
0
1
1
0
5
5
FeL(OH)2-
3.08
12.8
3
0
1
2
0 9
FeL2(OH)6-
-19.37
14.4
4
0
1
2
0
7
7
FeHL24-
-11.03
24.9
5
0
1
3
0
6
6
FeH6L33-
12.19
26.2
6
0
1
3
0
7
7
FeH5L34-
8.02
29.6
7
0
1
0
0
1
1
Fe(OH)2+
-2.56
11.4
8
0
1
0
0
2
2
Fe(OH)2+
-6.21
7.8
9
0
2
2
0
9
4.5
Fe2L2(OH)3-
16.11
49.5
10
1
0
1
0
2
2.0
GdH2L+
14.31
19.0
11
1
0
2
0
1
0.5
GdH7L22+
22.58
24.3
12
1
0
2
0
3
1.5
GdH5L20
19.87
26.2
13
1
0
2
0
4
2.0
GdH4L2-
19.03
28.4
14
1
0
2
0
5
2.5
GdH3L22-
12.87
29.8
15
1
1
1
0
4
4.0
GdFeL2+
16.51
40.2
16
1
1
1
0
5
5.0
GdFeL(OH)+
11.18
48.9
17
1
1
1
0
6
6.0
GdFeL(OH)20
5.12
56.8
18
1
1
1
0
7
7.0
GdFeL(OH)3-
-3.91
61.8
19
1
1
2
0
4
4.0
GdFeH4L22+
35.02
44.4
20
1
1
2
0
7
7.0
GdFeHL2-
28.84
64.7
21
1
1
2
0
8
8.0
GdFeL22-
22.34
69.7
22
1
1
2
0
9
9.0
GdFeL2(OH)3-
13.70
75.1
23
1
1
2
0
10
10.0
GdFeL2(OH)24-
3.08
78.5
24
1
1
2
0
11
11.0
GdFeL2(OH)35-
-8.54
80.9
25
1
2
3
0
10
10.0
GdFe2H2L3-
44.22
92.3
26
1
1
3
0
11
11.0
GdFeHL35-
13.31
72.9
27
1
1
3
0
12
12.0
GdFeL36-
5.19
76.3
28
1
1
3
0
13
13.0
GdFeL3(OH)7-
-5.56
79.5
29
1
1
2
0
6
6.0
GdFeH2L20
-34.85*)
-10.5
30
1
1
2
1
7
7.0
KGdFeHL20
-32.76*)
3.1
для растворения осадка: «Наложение» матрицы, полученной на основе рН-метрических
данных, на ЯМР-релаксационные данные (рис. 16), подтвердило ее адекватность и
математическую достоверность. Итоговые данные по стехиометрии и константам
образования соответствующих форм приведены в таблице 9, а доли накопления форм в зависимости от
концентрационных условий - на рисунках 12-15.
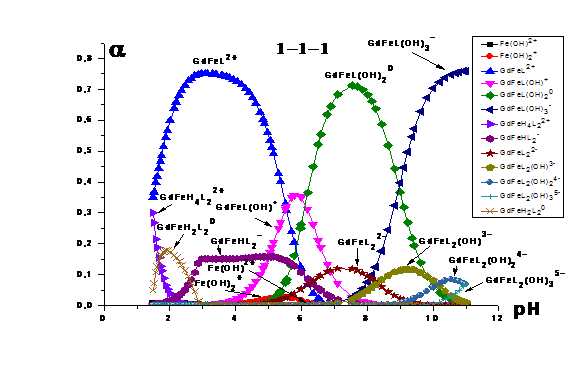
Рис 12 Зависимости долей накопления от pH среды при CGd(III) = 0.0114 моль/л , CFe(III)
= 0.0104 моль/л и СHEDP = 0.0121 моль/л.
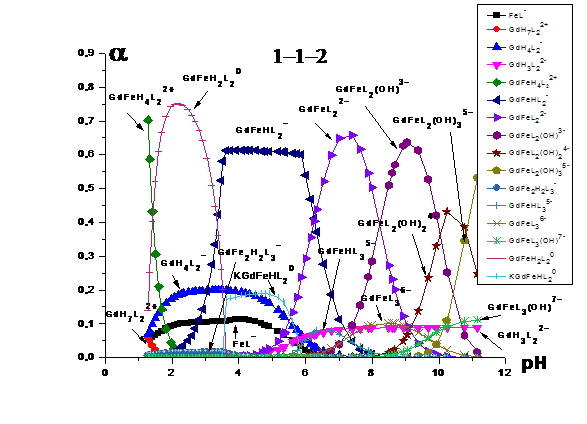
Рис 13 Зависимости долей накопленияот pH среды при CGd(III) = 0.0114 моль/л , CFe(III)
= 0.0104 моль/л и СHEDP = 0.0241 моль/л
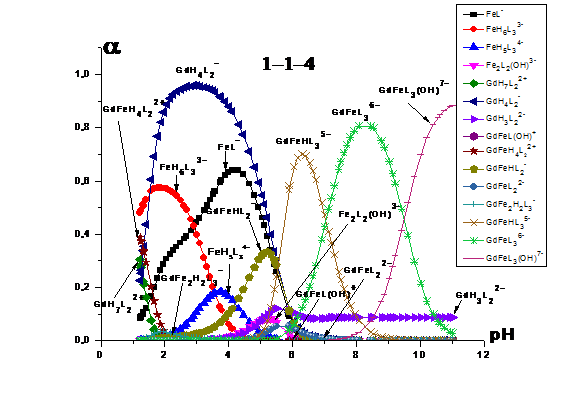
Рис 14 Зависимости долей накопленияот pH среды при CGd(III) = 0.0114 моль/л , CFe(III)
= 0.0104 моль/л и СHEDP = 0.0482 моль/л
Рис 15 Зависимости долей накопления от pH среды при CGd(III) = 0.0114 моль/л, CFe(III)
= 0.0104 моль/л и СHEDP = 0.0723 моль/л
Таким образом, методом рН-потенциометрии нами была изучена
гетероядерная система Gd3+ - Fe3+ - HEDP, при концентрации железа(III) 0,0104 моль/л,
концентрации Gd (III) в диапазоне 0,0114моль/л при разных концентрациях лиганда
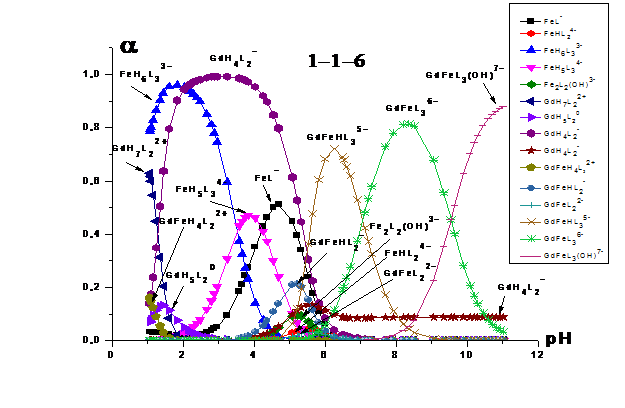
(табл. 7). Как следует из рисунков 12-15, в
системе Gd3+ -Fe3+ - HEDP при значительном избытке лиганда преимущественно
накапливаются следующие (FeH6L33-,GdH4L2-,GdFeL3(OH)7-) комплексы. При избытке лиганда наибольшая доля накопления
наблюдалась у комплексов (GdFeL36-,GdFeHL35-, GdFeL3(OH)7-,
GdMnL23-). При
небольшом избытке лиганда наблюдается бо́льшее разнообразие
преимущественно накапливающихся гетероядерных форм(GdFeH4L22+,
GdFeH2L20, GdFeHL2-,
GdFeL22-, GdFeL2(OH)3-). Для каждой из форм были рассчитаны константы
устойчивости(табл. 9).
Общая схема комплексообразования в системе Gd-Fe-HEDPбудет выглядет следующим образом:
а) в условиях избытка лиганда, б) для соотношения металл : металл :
лиганд 1:1:2 в) в условиях недостатка лиганда.
Как следует из ранее полученных данных[10], в системе Fe3+ - HEDP образуется(табл. 8) 8
комплексных форм (из них 2 - полиядерные), а в системе Gd3+ - HEDP
образуется [28] - 16 комплексных форм (из них 3 - биядерные). При совместном
присутствии в растворе обоих катионов накопление гетероядерных форм в кислой
области наблюдается только в отсутствии избытка лиганда, однако с ростом рН, в
результате отщепления протонов, гомоядерные формы переходят в гетероядерные
комплексы с соотношениями Gd:Fe:HEDP,
равным 1:1:1 и 1:1:2. При этом из гомоядерных форм в сильнокислом растворе
обнаруживаются лишь четыре комплекса: GdH5L20, GdH7L22+, GdH4L2-,
FeH6L33-.
Кроме того было промоделировано введение раствора (при концентрациях,
указанных в табл.7 и рН=7,40) с гетероядерными соединениями в организм человека,
предусматривающее 1000-кратное разбавление. Расчет показал, что свободные
катионы практически отсутствуют, а в растворе преобладают гетероядерные
комплексы (табл. 10). Таким образом, следует полагать, что использование
выбранной системы в качестве МРТ-контрастного реагента может быть оправдано
именно с точки зрения достаточной прочности накапливающихся комплексов.
Табл. 10 Сравнительная характеристика накапливающихся форм
при 1000 кратном разбавлении, pH=7.4
Gd(III)
Fe(III)
HEDP
H+
Форма
α, % (для разных
соотношений концентраций)
1-1-1
1-1-2
1-1-4
1-1-6
1
0
0
0
Gd(III), aqua
10
(5·10-7М)
~0
(10-23М)
~0
(10-20М)
~0
(10-21М)
0
1
0
0
Fe(III), aqua
~0
(10-16М)
~0
(10-26М)
~0
(10-26М)
~0
(10-26М)
0
1
1
4
FeL1-
-
-
4
5
0
1
1
5
FeL(OH)2-
-
-
8
10
1
0
2
5
GdH3L22-
-
10
17
21
1
1
1
5 3
-
-
-
1
1
1
6
GdFeL(OH)2
70
-
-
-
1
1
1
7
GdFeL(OH)31-
2
-
-
-
1
1
2
7
GdFeHL21-
2
10
7
7
1
1
2
8
GdFeL22-
13
76
60
54
1
1
2
9
GdFeL2(OH)3-
-
4
4
3
В исследовании были получены магнитно-релаксационные данные
по сериям (рис. 16) и проведено сравнение спин-спинового коэффициента
релаксационной эффективности в гетероядерной и гомоядерных системах для
одинаковых концентрационных условий и физиологическом значении рН (7.4). КРЭ2
для железо-содержащей системы [10] составляет 3000 л•моль-1•с-1,
для гадолиний-содержащей системы [28] - 5500 л•моль-1•с-1.
В гетероядерной системе КРЭ2 имеет значение 3700 л•моль-1•с-1
(при расчете использовалась сумма концентраций парамагнетиков). Таким образом,
гетероядерная система как контрастный реагент является более предпочтительной в
МРТ.
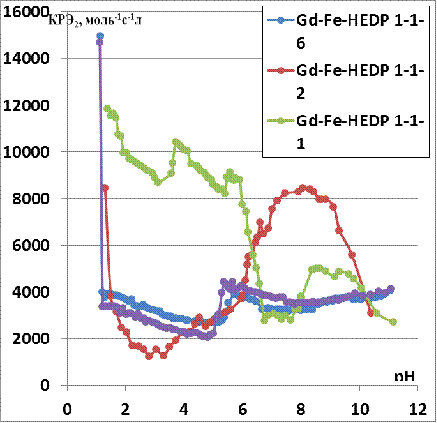
Рис.16 Зависимость коэффициента релаксационной
эффективности от pH для различных серий
Исходя из рис. 9 и 16 можно сделать вывод, что обе
изученные гетероядерные системы демонстрируют высокие значения КРЭ2
(для Gd-Mn-HEDP ~ 6700 M-1•с-1для Gd-Fe-HEDP ~ 3700 M-1•с-1и выше:
~ 8000 M-1•с-1при соотношении концентраций 1-1-2).В обеих
системах в растворе при физиологическом значении pH=7,40 доминируют
гетероядерные формы.
Высокая прочность гетероядерных комплексов в системеGd-Fe-HEDPпо сравнению с системой
Gd-Mn-HEDP(см. табл. 6 и 9)
продиктована большим ионным потенциалом трехзарядного иона железа (~3.82Å-1),что дает ему преимуществов образовании более
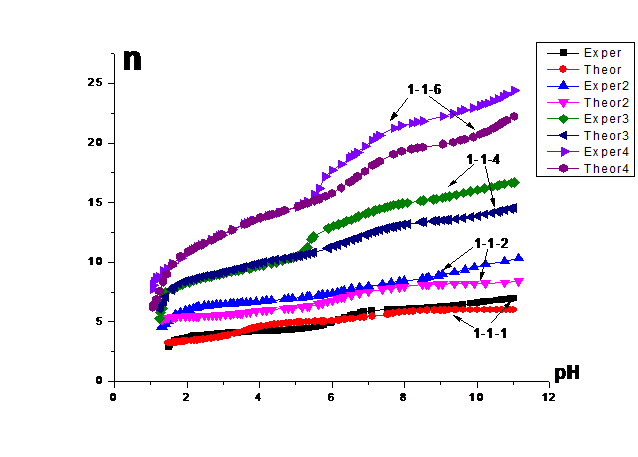
прочных связей перед двухзарядным ионом марганца (~2.06 Å-1), а также меньшим радиусом (0,78Å у Fe3+против 0,97 Åу Mn2+), что уменьшает
межкатионное отталкивание и позволяет найти более энергетически выгодную конфигурацию.
Таким образом, существуют общие положения для обеих
гетероядерных систем.
Во-первых, в них происходит замещение гомобиядерных форм на
гетероядерные, что говорит о более высокой устойчивости последних
[Сравнительную оценку устойчивости аналогов гомо- и
гетерополиядерных комплексов можно проводить, исходя из следующих соображений.
Если представить образование гетерополиядерного комплекса
уравнением
M'nLm + M''nLm 2M'n/2M''n/2Lm, (24)
то легко показать, что сдвиг равновесия вправо будет
происходить, если будет выполняться неравенство:
lgβуст.(M'n/2M''n/2Lm) > ½ [lgβуст.(M'nLm) + lgβуст.(M"nLm)] (25)
К сожалению, подобное сопоставление невозможно провести для
изученных систем, поскольку отсутствуют соответствующие аналоги (см. табл. 3,
4, 6, 8, 9)].
Во-вторых, гетероядерные формы показывают более высокое
значение КРЭ2 в сравнении с аналогичными гомоядерными системами, а
также демонстрируют более высокий процент накопления в практически важных для
медицины областях pH; при этом наблюдается крайне малое наличие свободных катионов,
что позволяет говорить о фактической их нетоксичности.
Основываясь на полученных данных можно предположить, что
гетероядерные комплексы исследованных в этой работе систем могут быть весьма
эффективно использованы в качестве контрастных реагентов и со временем прийти
на замену своим гомоядерным аналогам.
3. 1.Forgacs A., Regueiro-Figueroa M., Barriada J.L., Esteban-Gomez D., de Blas A., Rodriguez-Bias T., Botta M., Platas-Iglesias C. Mono‐, Bi‐, and Trinuclear Bis-Hydrated Mn2+ Complexes as Potential MRI Contrast Agents / A. Forgacs, M. Regueiro-Figueroa, J.L. Barriada, D. Esteban-Gomez, A. De Blas, T. Rodriguez-Bias, M. Botta , C. Platas-Iglesias//Inorg. Chem. -
2015. - V. 54, - P. A - B.
. Kołodynska D., Hubicki Z., Skiba A. Heavy Metal Ions
Removal in the Presence of 1-Hydroxyethane-1,1-diphosphonic Acid From Aqueous
Solutions on Polystyrene Anion Exchangers / D. Kołodynska, Z. Hubicki, A. Skiba// Ind. Eng. Chem. Res. - 2009. - N. 48, - P. 10584.
3. Мусин Д.Р.1-Гидроксиэтан-1,1-дифосфоновая кислота (hedp) и 1-аминоэтан-1,1-дифосфоновая
кислота (aedp): протолитические свойства,
комплексообразование с ионами кальция(ii) и лантаноидов(iii)
иттриевой подгруппы / Дис. канд. хим. наук; Д.Р.Мусин//Казанский (Приволжский)
федеральный университет. -Казань, - 2016. -158 c.
4. Kameda T., Shinmyou T., Yoshioka T.
Kinetic and equilibrium studies on the uptake of Nd3+ and Sr2+
by Li-Al layered double hydroxide intercalated with 1-hydroxyethane-1,1-diphosphonic
acid / T. Kameda, T. Shinmyou, T. Yoshioka// Journal of Industrial and
Engineering Chemistry. -2016. - V. 36, - P. 96 - 101.
. Uchtnan, V.A. Structural
investigations of calcium binding molecules. I. The crystal and molecular
structure of ethane-I-hydroxy-l.l-diphosphonic acid monohydrate / V.A. Uchtnan
// J. Phys. Chem. - 1972. - V. 76. - P. 1298-1304.
. Silvestre, J. P. Refinement by Neutron
Diffraction of the Crystal Structure of Hydroxyethylidene Bisphosphonic ACID
Monohydrate: C(CH3)(OH)(PO3H2)2•H2O
/ J. P. Silvestre, N. Q. Dao, G Heger, A. Cousson // Phosphorus, Sulfur and
Silicon - 2002. - V. 177. - P. 277-288.
. Afonin, G.G. X-Ray Identification of
1-Hydroxyethane-1,1-diphosphonic Acid / E. G. Afonin, G. G. Aleksandrov //
Russ. J. Gen. Chem. - 2003. - V. 73. - P. 340.
. Jansen D.R., Zeevaart J.R., Kolar
Z.I., Djanashvili K., Peters J.A., Krijger G.C. 31P NMR study of the
valence stability of tin in its 1-hydroxyethylene-diphosphonate (HEDP) and N,N′,N′-trimethylenephosphonate-polyethyleneimine
(PEI-MP) complexes / D.R. Jansen, J.R. Zeevaart, Z.I. Kolar, K. Djanashvili,
J.A. Peters, G.C. Krijger// Polyhedron. - 2008. - V. 27, - P. 1779 - 1781.
9. Мусин Д.Р Кислотно-основные свойства
1-гидроксиэтилидендифосфоновой кислоты (ОЭДФК) в водных растворах /Д.Р. Мусин,
А.В.Рубанов , Ф.В.Девятов // Ученые записки Казанского университета. Серия
Естественные науки. - 2011. - Т. 153. - C. 40-47.
. Ямалтдинова А.Ф.,Гомо- и гетероядерное
комплексообразование 1-гидрокси-1,1-бисфосфоновой кислоты (HEDP) с марганцем(II) и железом(III) в водных растворах /
А.Ф.Ямалтдинова // Дипл.работа, К(П)ФУ, Казань, - 2016. - 56 с.
11. Devyatov F., Musin D. Study of homo-
and heteronuclear complex formation in 1-hydroxyethylidene-1,1-diphosphonic
acid (HEDP)-erbium(III) and HEDP-erbium(III)-calcium(II) systems in an aqueous
solution / F. Devyatov, D. Musin// Russian chemical bulletin. -2015. - V. 64, -
P. 1866 - 1870.
12. Кропачева Т.Н. Комплексообразование железа
(III) c
оксиэтилидендифосфоновой кислотой в водных растворах / Кропачева Т.Н., Пагин
А.Н., Корнев В.И. // Вестник удмуртского университета. - 2012. - Вып. 4. - С.
64 .
. Дятлова Н.М. Комплексоны и комплексонаты
металлов / Дятлова Н.М., Темкина В.Я., Попов К.И //. М.: Химия. - 1988. - С.
544.
. Lacour S. Complexation of trivalent
cations (Al(III), Cr(III), Fe(III)) with two phosphonic acids in the pH range
of fresh waters / Lacour S., Deluchat V., Bollinger J.C., Serpaud B // Talanta.
- 1998. -V. 46. - P. 999-1009.
15. Васильев В.П. Комплексообразование Fe3+ с оксиэтилидендифосфоно-вой
кислотой / Васильев В.П, Козловский Е.В., Сердюков В.В // Журн. неорг. химии. -
1990. - Т. 35. - N. 2. - С. 373-376.
. Gumienna-Kontecka E. H. Bisphosphonate chelating agents: complexation of Fe(III) and Al(III) by 1-phenyl-1-hydroxymethylene bisphosphonate and its analogues / Gumienna-Kontecka E., Silvagni R., Lipinski R., Lecoyvey M., Marincola F.C., Crisponi G., Nurchi V.M., Leroux Y., Kozlowski // Inorg. Chim. Acta. - 2002. - V. 339. - P. 111-118. 31.
. Кабачник М.И. О комплексообразующих свойствах
оксиэтилидендифос-фоновой кислоты в водных растворах/ М.И. Кабачник, Р.П.
Ластовский, Т.Я. Медведь //ДАН СССР. - 1967. - Т. 177. - С. 582.
. Claessens, R. Stability-constant of tin(II) and calcium diphoshonat complexes/ R. Claessens, J. Van der Linden //Inorg. Biochem. - 1984. - V. 21. - P. 73.
19. Wada H. Interaction of
methanehydroxyphosphonic acid and ethane-1-hydroxy- 1,1-diphosphonic acid with
alkali and alkaline earth metal ions / H. Wada, Q. Fernando // Anal. Chem. -
1972. - V. 44. - P. 1640-1643.
. Silvestre, J.P. A neutron diffraction
study of the rubidium trihydrogen 1-hydroxy 1,1 - ethanedi(phosphonate)
dihydrate / J.P. Silvestre, I. Brouche-Waksman, G. Heger, N. Q. Dao // New J.
Chem. - 1990. - V. 14, N. 1. - P. 29.
21. Школьникова, Л.М. Кристаллическая и
молекулярная структура дигидрата [1-оксиэтилидендифосфоната (1-)] калия и
дигидрата [1-оксиэтилидендифосфонато (1-)] аммония / Л. М. Школьникова, А. А.
Масюк, Г. В. Полянчук // Координационная химия. - 1989. - Т. 15, №. 4. - С.
486-495.
. Barnard W., Paul S.O., Rooyen P.H.,
Cukrowski I. The analysis of pH-dependent protonated conformers of
1-hydroxyethylidene-1,1-diphosphonic acid by means of FT-Raman spectroscopy,
multivariate curve resolution and DFT modelling / W. Barnard, S.O. Paul, P.H.
Rooyen, I. Cukrowski// J. Raman Spectrosc. -2009. - V. 40, - P. 1935 - 1941.
. Gale E.M., Atanasova I.P., Blasi F.,
Ay I., Caravan P. A Manganese Alternative to Gadolinium for MRI Contrast / E.M.
Gale, I.P. Atanasova, F. Blasi, I. Ay, P. Caravan// J. Am. Chem. Soc. - 2015. -
V. 137, - P. 2 - 5.
. Islam M.K., Kim S., Kim H.K., Park S.,
Lee G.H., Kang H.J., Jung J.C., Park J.S., Kim T.J., Chan Y. Manganese Complex
of Ethylenediaminetetraacetic Acid (EDTA) − Benzothiazole Aniline (BTA)
Conjugate as a Potential Liver-Targeting MRI Contrast Agent / M.K. Islam, S.
Kim, H.K. Kim, S. Park, G.H. Lee, H.J. Kang, J.C. Jung, J.S. Park, T.J. Kim, Y.
Chan// J Med Chem. - 2017. - V. 60, - P. 2997.
. Elhabiri M., Abada S., Sy M., Nonat
A., Choquet Ph., Esteban-Gumez D., Cassino C., Platas-Iglesias C., Botta M., Charbonniere
L. J. Importance of Outer-Sphere and Aggregation Phenomena in the Relaxation
Properties of Phosphonated Gadolinium Complexes with Potential Applications as
MRI Contrast Agents / M. Elhabiri, S. Abada, M. Sy, A. Nonat, Ph. Choquet, D.
Esteban-Gumez, C. Cassino, C. Platas-Iglesias, M. Botta, L. J. Charbonniere//
Chem. Eur. J. - 2015. - N. 21 - P. 6535 - 6543.
. Srivastava K., Weitz E.A., Peterson
K.L., Marjańska M., Pierre
V.C. Fe- and Ln-DOTAm-F12 Are Effective Paramagnetic Fluorine Contrast Agents
for MRI in Water and Blood / K. Srivastava, E.A. Weitz, K.L. Peterson, M. Marjańska, V.C. Pierre// Inorg. Chem. - 2017. - P. 1546 -
1557.
. Cardoso B.P., Vicente A.I., Ward
J.B.J., Sebastião P.J., Chávez F.V., Barroso S., Carvalho A., Keely S.J.
Fe(III) salEen derived Schiff base complexes as potential contrast agents /
B.P. Cardoso, A.I. Vicente, J.B.J. Ward, P.J. Sebastião, F.V. Chávez, S. Barroso,
A. Carvalho, S.J. Keely// Inorganica Chimica Acta. - 2015. - V. 432, - P. 258 -
266.
28. ДевятовФ.В., Д.Р. Мусин.
Комплексообразованиевсистемахгадолиний(III)
1-гидроксиэтилидендифосфоноваякислотаикальций(II)
1-гидроксиэтилидендифосфоновая кислота в водных растворах / Ф.В. Девятов, Д.Р.
Мусин// Журнал общей химии. - 2012. - Т. 83, вып. 11. - С. 1788-1795.
. BogatyrevO., YamaltdinovaA., DevyatovF. Complexationof 1-Hydroxyethylidene-1, 1-DiphosphonicAcid (HEDP) andManganese (II) inAqueousSolution / O. Bogatyrev, A. Yamaltdinova, F. Devyatov// UchenyeZapiskiKazanskogoUniversiteta. - 2016. - V. 158, - P. 44 - 54.
. Попель А.А. Магнитно-релаксационный метод
анализа неорганических веществ / А.А. Попель // Москва Химия, 1978. - 222 c.].
.Вашман, А.А. Ядерная магнитная релаксация и её
применение в химии / А.А. Вашман, И.С. Пронин // Москва, Наука. - 1979. - 236
с.
. Бойченко А.П. Пересмотренные данные о
кислотно-основных свойствах алендроновой кислоты в воде и организованных
растворах и методика простого титриметрического определения алендроната натрия
/ Бойченко А.П., Марков В.В., Иващенко А.Л., Спирина Е.Ю., Логинова Л.П. //
Вісник Харківського національного університету. - 2007. - № 770. - Вып. 15(38).
- С. 62 - 69.
.Алексеев В.Н. Количественный анализ //Москва,
Высш.школа. - 1972. - С. 504.
. Пршибил Р. Комплексоны в химическом анализе /
Пршибил Р., Корыта И. // Москва, Издательство иностранной литературы. - 1960. -
С. 313-314.
35. Blombergen N.J. The relaxation
processes in NMR / N.J. Blombergen, E.M. Pursell, R.V. Pound // Phys. Rev. -
1948. - V. 53, № 7. - P. 679-712.
. Solomon J. The relaxation processes in
the interacting systems / J. Solomon // Phys. Rev. - 1955. - V. 99, N. 2. - P.
559-565.
. Blombergen N.J. Proton relaxation
times of paramagnetic solutions / N.J. Blombergen // Phys. Rev. - 1957. - V. 27, N. 2. - P. 537-572.
.Золин, В. Ф. Редкоземельный зонд в химии и
биологии / В. Ф. Золин, Л. Г. Коренева // Москва : Наука. - 1980. - 350 c.
. Девятов Ф.В. Исследование гомо - и
гетероцентровых комплексов гадолиния(III) и ионов иттриевой группы с лимонной и
трикарбаллиловой кислотами магнитно-релаксационным методом в водных растворах:
Дисс. … канд. хим. наук: 02.00.01 / Девятов Федор Владимирович. - Казань, 1980.
- 196 c.
.Журавлева Н.Е. Гомо- и гетерополиядерные
координационные соединения 4f- ионов иттриевой группы и некоторых 3d- ионов в
цитратрых водных растворах: Дисс. … канд. хим. наук: 02.00.01 / Н.Е. Журавлева.
- Казань, 1986. - 214 с.
. Соловский А.А. Исследование гомо- и
гетероядерных комплексов ионов железа(III), кобальта(II), никеля(II), меди(II)
с d- и dl- винными кислотами методом ядерной магнитной релаксации: Дис. … канд.
хим. наук: 02.00.01 / А.А. Соловский. - Казань, 1985. - 255 c.
.Вашман И.А. Ядерная магнитная релаксация и ее
применение в химической физике / И.А. Вашман, И.С. Пронин. - М.: Наука, 1979. -
224 c.
. Фаррар Т. Импульсная и фурье-спектроскопия
ЯМР / Т. Фаррар, Э. Беккер. - М.: Мир, 1973. - 169 c.
44. Hinton J. NMR studies of ions in
pure and mixed solvents / J. Hinton, E.S. Amis // Chem. Phys. - 1967. - V. 67,
N. 4. - P. 367-392.
. Blombergen N.J. Proton relaxation
times in paramagnetic solution. Effect of electron spin relaxation /
N.J.Bloembergen, L.O. Morgan // J. Chem. Phys. - 1961. - V. 31, N 3. - P. 842-850.
.Керрингтон А. Магнитный резонанс и его
применение в химии / А. Керрингтон, Э. Мак-Лечлан. - М.: Мир. 1970. - 248 c.
.Драго Р. Физические методы в химии / Р. Драго.
- М.: Мир, 1981. - Т. 1. - 424 c.
. Васильев В.П. Термодинамические свойства
растворов электролитов / В.П. Васильев М.: Высш. школа. 1982. - 320 с.
. Сальников Ю.И. Полиядерные комплексы в
растворах / Ю.И. Cальников, А.Н. Глебов, Ф.В. Девятов // Казань.: изд-во
Казанск. ун-та. 1989. - 288 c.
Размещено на Аllbеst.ru
![]() MnL2- + 4H+
MnL2- + 4H+
![]() MnH5L2- + 3H+
MnH5L2- + 3H+
![]() MnH4L22-
+ 4H+
MnH4L22-
+ 4H+
![]() MnH3L23-
+ 5H+
MnH3L23-
+ 5H+
![]() MnH2L24-
+ 6H+
MnH2L24-
+ 6H+
![]() MnHL25- + 7H+
MnHL25- + 7H+
![]() MnL26- + 8H+
MnL26- + 8H+
![]() Mn2H3L2-
+ 5H+
Mn2H3L2-
+ 5H+
![]() Mn2H2L22-
+ 6H+
Mn2H2L22-
+ 6H+
![]() Mn2HL23-
+ 7H+
Mn2HL23-
+ 7H+
![]() (11)
(11)
![]()
![]()
![]() MnL26- +8H+
MnL26- +8H+
![]() GdH4L2-
+4H+
GdH4L2-
+4H+
![]() GdMnH5L22+ + 3H+
GdMnH5L22+ + 3H+
![]() GdMnH4L2+ + 4H+
GdMnH4L2+ + 4H+
![]() GdMnH3L2↓ + 5H+
GdMnH3L2↓ + 5H+
![]() GdMnH2L2-1 + 6H+
GdMnH2L2-1 + 6H+
![]() GdMnHL22- +7H+
GdMnHL22- +7H+
![]() GdMnL23- + 8H+
GdMnL23- + 8H+
![]() GdMnL2(OH)4- + 9H+
GdMnL2(OH)4- + 9H+
![]() GdMnH7L3↓ + 5H+
GdMnH7L3↓ + 5H+
![]() GdMnH6L3-1 + 6H+
GdMnH6L3-1 + 6H+
![]() K3Gd2L2(OH)↓+
9H+
K3Gd2L2(OH)↓+
9H+
![]() GdH2L++ 2H+
GdH2L++ 2H+
![]() KGd2HL2↓+
7H+
KGd2HL2↓+
7H+
![]() Gd2Mn2H2L24++
6H+
Gd2Mn2H2L24++
6H+
![]() GdMnL++ 4H+
GdMnL++ 4H+
![]() GdMnL(OH)2↓+ 6H+
GdMnL(OH)2↓+ 6H+
![]()
![]()
![]() GdMnH6L3-1
GdMnH6L3-1![]() GdMnH2L2
GdMnH2L2![]() GdMnL23-
GdMnL23-![]() GdMnL2(OH)2-
(19)
GdMnL2(OH)2-
(19)
![]()
![]() GdMnH3L20 (20)
GdMnH3L20 (20)
![]()
![]() GdMnH4L2
GdMnH4L2![]() GdMnH3L20
GdMnH3L20![]() GdMnH2L21-
GdMnH2L21-
![]()
![]() GdMnL23+
GdMnL23+
![]() Gd2Mn2H2L24+
Gd2Mn2H2L24+![]() GdMnL+
GdMnL+![]() K3Gd2L2(OH)
(21)
K3Gd2L2(OH)
(21)
ГЛАВА 4.
КОМПЛЕКСООБРАЗОВАНИЕ В СИСТЕМЕ "Gd(III)-Fe(III)-HEDP"
![]() FeL- + 4H+
FeL- + 4H+
![]() FeL(OH)2-+ 5H+
FeL(OH)2-+ 5H+
![]() FeL2(OH)6-+ 9H+
FeL2(OH)6-+ 9H+
![]() FeHL24- + 7H+
FeHL24- + 7H+
![]() Fe3H2L3- + 10H+
Fe3H2L3- + 10H+
![]() FeH6L33- + 6H+
FeH6L33- + 6H+
![]() FeH5L34- + 7H+
FeH5L34- + 7H+
![]() Fe2L2(OH)3- + 9H+
Fe2L2(OH)3- + 9H+
![]()

ОСНОВНЫЕ
РЕЗУЛЬТАТЫ И ВЫВОДЫ
1. Методами
pH-потенциометрии и протонной магнитной
релаксации в сочетании с методом математического моделирования установлены
стехиометрия, константы образования, коэффициенты релаксационной эффективности
и константы устойчивости комплексных форм в системах «Gd(III) -Mn(II)-HEDP» и «Gd(III) -Fe(III) -HEDP».
. Установлено,
что в гетероядерных системах наблюдается разнообразие и высокая устойчивость
гетероядерных комплексов, благодаря чему происходит
замещение гомополиядерных форм на гетероядерные. Причиной этого может
быть существенно меньший радиус 3d-
ионов по сравнению с ионом гадолиния(III), что уменьшает межкатионное отталкивание
в структуре гетероядерных комплексов. Кроме того, комбинация
"жесткого", орбитально контролируемого ковалентного связывания 3d- ионов и "подвижного"
электростатического ионного взаимодействия с нуклеофильными центрами лиганда в
случае гадолиния(III) приводит к энергетически оптимальным конфигурациям
гетероядерных комплексов.
Установлено, что
гетероядерные формы системы «Gd(III) -Fe(III) -HEDP»устойчивее гетероядерных комплексов
системы «Gd(III) -Mn(II) -HEDP». Это связано с существенно меньшим ионным радиусом и
большим ионным потенциалом Fe3+
в сравнении с Mn2+, что приводит к различиям в энергии
связей и пространственной координации донорных групп лиганда. Результаты
моделирования гетероядерных композиций в организм человека (с 1000-кратным
разбавлением) демонстрируют доминирование устойчивых гетероядерных форм с
высокими значениями коэффициента релаксационной эффективности и практически
нулевыми концентрациями свободных катионов.Это дает возможность говорить об
изученных гетероядерных системах как о потенциальных эффективных нетоксичных
МРТ контрастных реагентах.
СПИСОК
ЛИТЕРАТУРЫ