Материал: Гетероядерные комплексы в системах гадолиний(III)–марганец(II)/железо(III)/ - оксиэтилидендифосфоновая кислота как потенциальные МРТ контрастные реагенты
Гетероядерные комплексы в системах гадолиний(III)–марганец(II)/железо(III)/ - оксиэтилидендифосфоновая кислота как потенциальные МРТ контрастные реагенты
Министерство образования и науки РФ
Федеральное государственное автономное образовательное учреждение высшего образования
«КАЗАНСКИЙ (ПРИВОЛЖСКИЙ) ФЕДЕРАЛЬНЫЙ
УНИВЕРСИТЕТ»
ВЫПУСКНАЯ КВАЛИФИКАЦИОННАЯ РАБОТА
Гетероядерные комплексы в системах
гадолиний(III)-марганец(II)/железо(III)/ - оксиэтилидендифосфоновая кислота как
потенциальные МРТ контрастные реагенты
СОДЕРЖАНИЕ
ВВЕДЕНИЕ
ГЛАВА 1. ЛИТЕРАТУРНЫЙ ОБЗОР
1.1 Физико-химические свойства HEDP
1.2. Комплексообразование HEDP c марганцем (ii)
1.3. Комплексообразование HEDP с гадолинием (iii)
1.4. Комплексообразование HEDP с железом (iii)
1.5. Комплексообразование HEDP с ионами щелочных металлов
1.6. Использование ионов Mn2+ в МРТ
1.7. Использование ионов Gd3+ в МРТ
1.8. Использование ионов Fe3+ в МРТ
ГЛАВА 2. ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
2.1 Постановка задачи.
2.2 Методика эксперимента
2.2.1 Приборы и реактивы
2.2.2 Метод протонной магнитной релаксации
2.2.3 Метод математического моделирования
ГЛАВА 3. КОМПЛЕКСООБРАЗОВАНИЕ В СИСТЕМЕ"Gd(III)-Mn(II)-HEDP"
ГЛАВА 4. КОМПЛЕКСООБРАЗОВАНИЕ В СИСТЕМЕ "Gd(III)-Fe(III)-HEDP"
ОСНОВНЫЕ РЕЗУЛЬТАТЫ И ВЫВОДЫ
СПИСОК ЛИТЕРАТУРЫ
ВВЕДЕНИЕ
Введение некоторых комплексов на основе Gd3+ в качестве контрастных веществ в МРТ бурно развивали исследовательскую деятельность в координационной химии этого иона металла и других ионов лантанидов. Коммерчески доступные контрастные агенты на основе Gd3+ представляют собой комплексы с полиамино/поликарбоксилат октадентатным лигандом, который оставляет координационное положение для молекулы воды вакантным. Скоординированная молекула воды участвует в быстром обмене с водой окружающих тканей, что дает эффективный механизм для увеличения скорости релаксации протонных ядер молекулы воды. Ион Gd3+ был выбран в качестве контрастного агента из-за его высокого эффективного магнитного момента и относительно медленной релаксации электронного спина, которая связана с его симметричным основным состоянием 4f7. Однако высокоспиновые комплексы Mn2+ и Fe3+ с конфигурацией 3d5 также обладают относительно медленной релаксации спина и довольно высоким эффективным магнитным моментом, таким образом, устойчивые комплексы этих ионов металлов могут применяться в качестве контрастных агентов в МРТ, заменяя соединения на основе Gd3+. Применение комплексов Mn2+ в качестве контрастных агентов в МРТрассматривали ужев конце 1980-х годов [1].
Цель данной работы - описать закономерности комплексообразования в гетероядерных системах «гадолиний(III) -марганец(II) - HEDP» и «гадолиний(III) - железо(III)-HEDP» в водном растворе и рассмотреть возможность комплексов данных систем выступать в качестве контрастных реагентов в МРТ.
гетероядерный гадолиний марганец контрастный
ГЛАВА 1. ЛИТЕРАТУРНЫЙ ОБЗОР
1.1 Физико-химические свойства HEDP
1-гидроксиэтан-1,1-дифосфоноваякислота (HEDP) обладает уникальными физико-химическими свойствами. Она водорастворима, химически устойчива при высоком значении рН, с трудом гидролизуется [2]. HEDP является четырехосновной кислотой и содержит наряду с кислотными центрами (P-OH) основный атом, в качестве которого выступает кислород от гидроксогруппы (C-OH) (рис.1).1-Гидроксиэтан-1,1-дифосфоноваякислотавзаимодействует с кислотами, щелочами, а также окисляется хлором лучше, чем другие соли фосфорорганических кислот. Молекула HEDP содержит в своем составе семь электронодонорных атомов кислорода, которые могут образовывать координационные связи с ионами металлов даже в сильнокислой среде. Химический сдвиг HEDP 31Р составляет 19.8 м.д. относительно ортофосфорной кислоты, при этом наблюдается только один сигнал, что свидетельствует об эквивалентности ядер фосфора в молекуле [3].
HEDP-удивительно мощный хелатирующий агент в умереннокислых растворахдля ионов актинидов или лантанидов. Фосфоновыегруппы могут координироваться с ионами актинидов или лантаноидов без полного депротонирования. Поэтому НEDPнашла применение для усиления селективностиразделения f -элементов от других ионов металлов. Она также имеет широкое применение в различных областях техники [2].
Также можно сделать вывод о металлохелатирующих функциях ионов HEDP, вследствие того, что комплекс HEDPLi-AlLDH поглощает ионы Nd3+ и Sr2+ из водных растворов [4].
В кристаллическом состояний изучен моногидрат HEDP ∙ H2O методами рентгеновской
дифракции [5] и нейтронографии [6]. HEDP ∙ H2O относится к моноклинной
пространственной группе симметрии. Примечательно, что в молекуле моногидрата HEDP водородная связь
образуется между соседними молекулами лиганда и между молекулами лиганда и
воды, однако водородных связей между молекулами воды не возникает [6]. Об обширных
водородных связях свидетельствует и высокая температура дегидратации (выше
70°C), о чем свидетельствуют данные порошкового рентгеноструктурного анализа
[7].

Рис. 1 Структурная формула HEDP
Дифосфонаты стали широко распространены в их применении для лечения заболеваний, связанных с костями, и рака, так как они замедляют процесс разрушения костей остеокластами, препятствуя их апоптозу (апоптоз - форма клеточной смерти).
В последние годы проявился интерес в применении дифосфонатов в качестве потенциальных радиофармацевтических препаратов для эффективного обезболивания метастатического рака кости [8].1-Гидроксиэтан-1,1-дифосфоновая кислота (HEDP), применяется в медицине в виде препаратов ксидифон и этидронат.
Благодаря полученным данным[9] по рН максимального
накопления различных форм HEDP (табл.1)сделан вывод о том, что диссоциация
иона водорода энергетически благоприятнее в случае образования дианиона, чем
при образовании моноаниона, что связано со стабилизацией димерных анионов
межчастичными водородными связями. Об этом свидетельствует и
анализсоответствующих ступенчатых констант диссоциации для моно- и дианионов.
Табл.1 Кислотно-основные свойства и калиевые комплексы HEDP в водных растворах [9]
|
№ |
Равновесие |
n |
рНmax накопл. |
lgK, δ ≤ 0.12 |
|
1 |
|
1 |
2.3 |
-1.65 |
|
2 |
|
2 |
5.2 |
-4.67 |
|
3 |
|
3 |
9.2 |
-12.20 |
|
4 |
|
4 |
>12 |
-23.70 |
|
5 |
|
1 |
1.8 |
-2.90 |
|
6 |
|
1,5 |
2.6 |
-5.54 |
|
7 |
|
2 |
4.8 |
-9.23 |
|
8 |
|
2.5 |
6.8 |
-16.77 |
|
9 |
|
3 |
8.9 |
-24.79 |
|
10 |
|
3 |
8.9 |
-11.23 |
|
11 |
|
4 |
>11 |
-20.89 |
1.2 Комплексообразование HEDP c марганцем (ii)
Авторы работы [10] методами рН-потенциометрии и ЯМР релаксации определили
константы равновесия и долевые распределенияв системе «Mn2+ - HEDP».
Было установлено, что при значительном избытке
лиганда образуются преимущественно моноядерные бискомплексы. При увеличении рН
устойчивость образующихся комплексов увеличивается. Комплексообразование
протекает по следующей схеме:
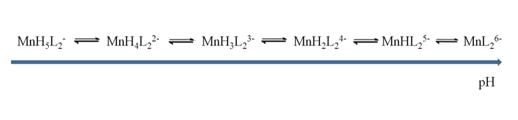 (1)
(1)
При эквимолярных соотношениях металл : лиганд схема
комплексообразования усложняется, в системе в значительном количестве
образуются моно- и биядерные комплексы состава 1:1 , 1:2 и 2:2. Схема комплексообразования:
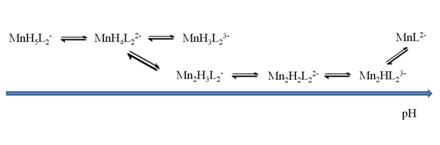 (2)
(2)
Авторы отмечают, что гидролиз с образованием гидроксида марганца Mn(OH)2 не наблюдался при эксперименте. Также не происходит окисления марганца(II) кислородом воздуха в более высокие степени окисления.
Метод ЯМР-релаксации выявил высокий коэффициент
эффективности релаксации (КРЭ2) комплексов (Mn2HL23-,MnL26- , Mn2H2L22-) по времени
спин-спиновой релаксации (T2) и их значительную устойчивость, что
позволяет рассматривать их как потенциальные МРТ-контрастные реагенты [10].
1.3 Комплексообразование HEDP с гадолинием (III)
Автор работы [3, 11]выделяет два вида
зависимости при движении по ряду для всех
ионов лантаноидов иттриевой подгруппы: а)
падение значений констант в ряду Gd3+ - Dy3+ - Ho3+ и возрастание при
переходе к Er3+ и Tm3+ для комплексов LnH2L+, Ln2H2L4+; б) возрастание устойчивости комплекса при
переходе от Ho3+ к Er3+ и убывание при переходе от Gd3+ к Ho3+ и от Er3+ к Tm3+ для комплексов LnH4L2-, LnH3L22-, Ln2L22-, Ln2L2+, Ln2L2(OH)3- и Ln2L(OH)+.
В том числе нас интересует вывод, обобразовании разнообразного набора комплексных форм в
системе «Gd-HEDP»- с разной степенью депротонизации лиганда. При
значительном избытке лиганда накапливаются преимущественно комплексы с
соотношением металл:лиганд = 1:2 (GdH4L2-, GdH7L22+, GdH3L22-) и 2:2 (Gd2L22-, Gd2L2(OH)3-).При значительно больших концентрациях
катиона-комплексообразователя по сравнению с лигандом наряду с накоплением
комплексов состава металл:лиганд 1:2 и 2:2 образуются и биядерные комплексы состава
2:1 (Gd2L(OH)+, Gd2L(OH)2↓
и Gd2L2+ ). Автор отмечает, что гидролиз
катиона Gd3+ с образованием гидроксида не наблюдается, однако при рН
> 7 наблюдается образование растворимых Gd2L2(OH)3-,Gd2L(OH)+ и
нерастворимых гидроксокомплексов Gd2L(OH)2, K3Gd2L2(OH).
Суммарная схема комплексообразования ионов гадолиния (III) с HEDP, основанная на анализе
долевого распределения
1.4 Комплексообразование HEDP с железом (III)
HEDP связывается с катионами d-элементов в прочные
водорастворимые комплексы. Как и для других фосфорорганических комплексонов,
для HEDP характерно образование протонированных комплексов с Fe(III) уже в
сильнокислой среде [12]; в области рН близкой к нейтральной в растворе
существует средний комплексонат FeL-, устойчивость которого (lg β=22-23) лишь немного уступает устойчивости комплекса FeEdta- (lgβ=25.1). Дальнейшее повышение рН раствора приводит к образованию
моногидроксокомплекса, устойчивого вплоть до рН<11 [12]. Так как в работах
[13-16] схемы комплексообразования системы «Fe-HEDP» и константы
равновесий существенно различаются, нашей исследовательской группой система «Fe-HEDP» была изучена
самостоятельно[10].Было установлено, что комплексы железа (III) cHEDP значительно устойчивее комплексов
марганца (II) cHEDP. Это связано с существенно меньшим ионным радиусом и
бóльшим ионным потенциалом Fe3+(3,82) в сравнении с Mn2+(2,06),
что приводит к пространственным различиям в координации донорных групп лиганда.
Бóльшей устойчивости комплекса FeL- по сравнению MnL2- соответствует и бóльший ионный потенциал у иона Fe3+ в сравнении с Mn2+. С последним также связано и наличие
гидроксокомплексов железа: Fe2L2(OH)3-,
FeL(OH)2- и FeL2(OH)6-. Эти гидроксоформы
образуются в щелочной области по следующей схеме комплексообразования:
FeH6L33-![]() FeH5L34-
FeH5L34-![]() FeL-
FeL-![]() Fe2L2(OH)3-
Fe2L2(OH)3-![]() FeL(OH)2-
FeL(OH)2-![]() FeL2(OH)6-
FeL2(OH)6-
![]()
FeHL24- FeHL24- (4)
В случае с одинаковым соотношением металл:лиганд
значительно большую долю накопления показывает комплекс Fe3H2L34-, а дальнейшее
комплексообразование идет по следующей схеме:
Fe3H2L34-![]() FeL-
FeL-![]() Fe2L2(OH)3-
Fe2L2(OH)3-![]() FeL(OH)2- (5)
FeL(OH)2- (5)
1.5 Комплексообразование HEDP с ионами щелочных металлов
Молекула HEDP содержит в своем составе семь электронодонорных атомов кислорода, которые могут образовывать координационные связи с ионами металлов вплоть до сильно кислых сред [17, 18].
Особенностью HEDP является образование довольно устойчивых комплексов с щелочными катионами при рН > 7. Известны комплексонаты состава MH2L- , MHL2- и M2HL-.
Исходя из данных работы [19] применение в качестве «фоновых» электролитов солей щелочных катионов при изучении комплексообразования HEDP является нежелательным. Расчеты показывают, что при концентрации ионов натрия 0,1 моль/л (I=0.1) в области рН от 5 до 7 около 25% HEDP связано в комплекс NaH2L, а при рН = 7 - 70%. При концентрации ионов калия 0,05 моль/л в области рН = 9 приблизительно 50% комплексона связано в комплексы щелочного катиона [19].
HEDP формирует с щелочными катионами не только
устойчивые нормальные комплексонаты ML3-, но и протонированные
комплексы MH2L-. При этом речь может идти о формировании
полноценных комплексов с хелатной структурой. На возможность наличия таковой у
протонированных комплексонатов HEDP указывают результаты рентгеноструктурных
исследований кристаллов Na2H2L ∙ 4H2О
и изоструктурного ряда MH3L ∙ 2H2O, где
M = Na+, K+, Rb+,
Cs+ (табл.2).
Табл.2 Межатомное расстояние M-O (где M = Na+, K+, Rb+ и Сs+)[21].
|
№ |
Комплекс |
Среднее межатомное расстояние М-О (Å) |
КЧ катиона металла |
|
1 |
KH3L ∙ 2H2O |
2.880 |
7 |
|
2 |
RbH3L ∙ 2H2O |
3.028 |
7 |
|
3 |
RbH3L ∙ 2H2O |
3.030 |
7 |
|
4 |
RbH3L ∙ 2H2O* |
3.028 |
7 |
|
5 |
CsH3L ∙ 2H2O |
3.366 |
11 |
|
6 |
Na2H2L ∙ 4H2O |
2.394; 2.471 |
6 →Na(1) 4 + 1 →Na(2) |