Материал: Физхимия коллоквиум
7.Энтропия и термодинамическая вероятность. Уравнение Больцмана. Расчёт изменения энтропии в изотермическом, изобарном и изотермическом процессах.
Энтропия (S)– мера неупорядоченности системы.
Уравнение Больцмана:
S=klnW, где W – ТД вероятность; k – постоянная Больцмана.
ТД вероятность(W)– величина, которая определяется числом микросостояний, которым может быть реализовано макросостояние.
Энтропия зависит от:
Агрегатного состояния - Sг>Sж>Sтв
От давления – чем выше давление, тем ниже энтропия
От объема – чем выше объем, тем выше энтропия
От температуры =>>
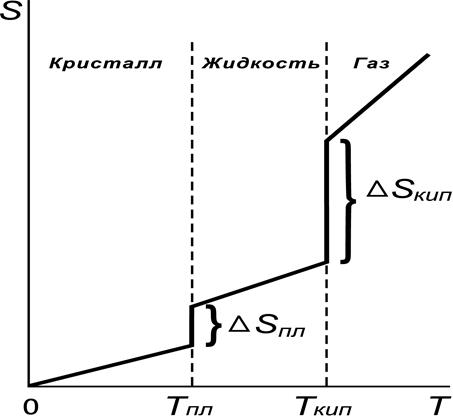 Расчёт
изменения энтропии в изотермическом,
изобарном и изохорных процессах:
Расчёт
изменения энтропии в изотермическом,
изобарном и изохорных процессах:
Изотермический T=const
Фазовый переход ∆S=∆Hфп/Тфп
Расширение идеального газа ∆S= νRlnV2/V1
Изобарный P=const ∆S= νCplnT2/T1
Изохорный V=const ∆S= νCvlnT2/T1
8.Постулат Планка. Абсолютная энтропия. Зависимость энтропии от температуры. Расчёт энтропии при различных температурах.(задачи?)
Постулат Планка:
Энтропия идеального кристалла при Т=0К равна нулю.
Расчет абсолютной энтропии:
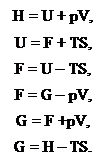
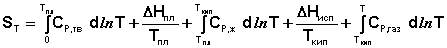

9. Термодинамические потенциалы. Фундаментальное уравнение термодинамики.
Смысл ТД потенциала:
Падающий груз летит вниз, а не вверх, в сторону уменьшения потенциальной энергии. Т.о. самопроизвольные процессы, где ∆S<0. Когда груз достигает земли (равновесие), то изменение силы равно 0, а максимальная работа груза при падении Amax=-∆E.
Фундаментальное уравнение термодинамики:
Связывает 1 и 2 законы ТД.
Для закрытых систем:
dU=TdS-∑Yidyi
Для открытых систем:
dU=TdS-∑Yidyi+∑μidni, где μ - химический потенциал, dni – изменение числа моль для этого в-ва, ∑μidni – обмен энергией, связанный с обменом в-ва.
10.Энергия Гиббса и Гельмгольца. Критерии равновесия и самопроизвольного протекания процессов. Энтальпийный и энтропийный фактор.
Энергия Гиббса G – это та часть всей энергии системы, которую можно использовать для совершения максимальной работы.
Энергия Гельмгольца A — это та часть внутренней энергии системы, также определяющая работоспособность и может быть применена для совершения максимальной работы.
Они не зависят друг от друга и их величины противоположны, и процесс идет в сторону той реакции, при которой изменение величины больше. Разность между этими величинами определяет свободную энергию реакции (при постоянных температуре и давлении). Ее изменение в реакции определяется разностью сумм энергий Гиббса конечных продуктов реакции и исходных веществ:
ΔG= Gкон – Gисх
При постоянных температуре и давлении изменение энергии Гиббса связано с энтальпией и энтропией следующим выражением:
ΔG = ΔH– TΔS
Здесь изменение энергии Гиббса учитывает одновременно изменение энергетического запаса системы и степень ее беспорядка (самопроизвольность протекания процесса).
Т.к. энергия Гиббса является мерой самопроизвольности протекания процесса, то между знаком ΔG для любой реакции и ее самопроизвольным протеканием (при постоянных температуре и давлении) существуют такие зависимости:
Если ΔG отрицательно (ΔG<0), то реакция протекает самопроизвольно в прямом направлении.
Если ΔG равно нулю (ΔG=0), то реакция находится в равновесном состоянии.
Если ΔG положительно (ΔG>0), то реакция протекать самопроизвольно в прямом направлении не может. Однако обратная реакция идет самопроизвольно.
ΔH |
ΔS |
ΔG |
Протекание реакции |
˂0 |
>0 |
Всегда ˂0 |
Реакция самопроизвольна при любых температурах, обратная реакция всегда несамопроизвольна |
>0 |
˂0 |
Всегда >0 |
Реакция несамопроизвольна при любых температурах, обратная реакция самопроизвольна |
˂0 |
˂0 |
При низких температурах ˂0, при высоких температурах >0 |
Реакция самопроизвольна при низких температурах, обратная реакция становится самопроизвольной при высоких температурах |
>0 |
>0 |
При низких температурах >0, при высоких температурах ˂0 |
Реакция несамопроизвольна при низких температурах, но при высоких температурах становится самопроизвольной |
11.Фаза. Условия фазового равновесия. Правило фаз Гиббса. Понятия: независимый компонент, вариативность системы.
Фаза(Ф) – совокупность гомогенных частей системы, одинаковых по всем физ-хим св-вам и ограниченных от других частей некоторой повторностью раздела фаз.
Фазовые равновесия – гетерогенные равновесия, связанные с переходом в-ва из одной фазы в другую без изменения хим. состава. Примеры: плавление, испарение, кристаллизация, сублимация, аллотропные переходы, переход парамагнетиков в ферромагнетики и тд
Рассмотрим условия фазового равновесия при T, P=const. Пусть имеется система из 2 фаз: α и β. Один из компонентов самопроизвольно переходит из α в β.
dGαi =μαidnαi , dGβi=μβidnβi
Общее: dG= μαidnαi+ μβidnβi=0
Очевидно, что dnαi = - dnβi , тогда dG=0 => μαi > μβi
Правило фаз Гиббса устанавливает связь между числом ТД степеней свободы (f), числом независимых компонентов (К) и числом фаз системы (Ф).
f=К-Ф+m, где m – число ТД параметров.
Независимый компонент (К) – наименьшее число индивидуальных в-в в системе, достаточное для образования всех фаз системы.
К= число компонентов – число уравнений связи
Вариативность системы (f) – число независимых ТД параметров (P, V, состав и тд), которые можно менять в некоторых пределах без изменения числа фаз.
12.Равновесные соотношения при фазовых переходах (уравнение Клаузиуса-Клапейрона). Вывод уравнений линий фазового равновесия твёрдо-жидкое; жидкое-газ; твёрдое-газ для фазовой диаграммы воды.
Уравнение Клаузиуса - Клапейрона:
Дано две фазы α и β. При T, P=const данные фазы в равновесии, следовательно
Gα=Gβ , ∆G=Gα – Gβ = 0
Если изменим внешние условия, то поменяется T и изменится G.
Gα + dGα = Gβ + dGβ
dG = -SdT + νdP => dGα=dGβ
Рассмотрим данное выражение для данных условий:
-SαdT + ναdP = -SβdT + νβdP => dT(Sβ-Sα)=dP(νβ-να)
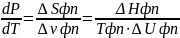 – уравнение
Клаузиуса-Клапейрона
– уравнение
Клаузиуса-Клапейрона
Вывод уравнений линий фазового равновесия:
1.
Плавление (тв-жид)
P=P*+(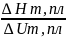 )lnT/T*
)lnT/T*
где Т*, Р* - любые координаты с фазовой диаграммы (часто берут либо 0, либо Ткип).
2. Испарение (жид-газ)
P=P*exp
3. Сублимация (газ-тв)
P=P*exp
13. Фазовые диаграммы однокомпонентных систем. Фазовые диаграммы воды. Фазовые переходы второго рода.
Фазовые диаграммы однокомпонентных систем изображаются на плоскости в координатах p–T. На них присутствуют поля, отвечающие существованию той или иной фазы вещества (газообразной, жидкой, различных твердых модификаций), разделенные линиями фазового равновесия, вдоль которых возможно сосуществование граничащих фаз. Места, где сходятся три различные линии фазовых равновесий, образуют так называемые тройные точки, в которых могут сосуществовать три фазы. Это максимальное число фаз, способных равновесно сосуществовать в однокомпонентных системах.
Число фаз, присутствующих в точке фазовой диаграммы, определяется правилом фаз Гиббса и составляет n + 2 – f, где n — число компонентов.
Кроме того, на фазовой диаграмме однокомпонентной системы могут изображаться метастабильные фазы, т. е. фазы, не являющиеся равновесными, но способные существовать в определенной области параметров в течение длительного времени вследствие кинетической стабильности, а также критическая точка — точка на линии равновесия жидкость–газ, после которой исчезает скачкообразное различие свойств этих фаз, и понятие фазового перехода теряет смысл.
Помимо температуры и давления могут рассматриваться и другие параметры состояния системы, например, напряженность магнитного поля (H). Тогда фазовая диаграмма становится многомерной и рассматриваются различные ее сечения, например H–T, а в правиле фаз число 2 меняется на соответствующее число обобщенных сил (полей).
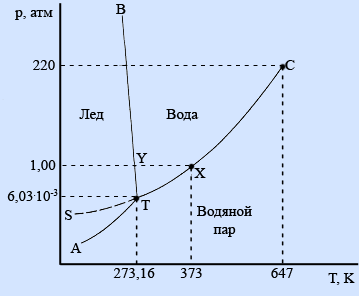 Рассмотрим
диаграмму состояния однокомпонентной
системы на примере диаграммы состояния
воды.
Рассмотрим
диаграмму состояния однокомпонентной
системы на примере диаграммы состояния
воды.
Области фазовой диаграммы, ограниченные кривыми, соответствуют тем условиям (температурам и давлениям), при которых устойчива только одна фаза вещества. Например, при любых значениях температуры и давления, которые соответствуют точкам диаграммы, ограниченным кривыми ВТ и ТС, вода существует в жидком состоянии. При любых температуре и давлении, соответствующих точкам диаграммы, которые расположены ниже кривых АТ и ТС, вода существует в парообразном состоянии.
Кривые фазовой диаграммы соответствуют условиям, при которых какие-либо две фазы находятся в равновесии друг с другом. Например, при температурах и давлениях, соответствующих точкам кривой ТС, вода и ее пар находятся в равновесии. Это и есть кривая давления пара воды. В точке Х на этой кривой жидкая вода и пар находятся в равновесии при температуре 373 К (100°С) и давлении 1 атм (101,325 кПа); точка Х представляет собой точку кипения воды при давлении 1 атм.
Кривая АТ является кривой давления пара льда; такую кривую обычно называют кривой сублимации.
Кривая ВТ представляет собой кривую плавления. Она показывает, как давление влияет на температуру плавления льда: если давление возрастает, температура плавления немного уменьшается. Такая зависимость температуры плавления от давления встречается редко. Обычно возрастание давления благоприятствует образованию твердого вещества. В случае воды повышение давления приводит к разрушению водородных связей, которые в кристалле льда связывают между собой молекулы воды, заставляя их образовывать громоздкую структуру. В результате разрушения водородных связей происходит образование более плотной жидкой фазы.
В точке Y на кривой ВТ лед находится в равновесии с водой при температуре 273 К (0°С) и давлении 1 атм. Она представляет собой точку замерзания воды при давлении 1 атм.
Кривая SТ указывает давление пара воды при температурах ниже ее точки замерзания. Поскольку вода в нормальных условиях не существует в виде жидкости при температурах ниже ее точки замерзания, каждая точка на этой кривой соответствует воде, находящейся в метастабильном состоянии. Это означает, что при соответствующих температуре и давлении вода находится не в своем наиболее устойчивом (стабильном) состоянии. Явление, которое соответствует существованию воды в метастабильном состоянии, описываемом точками этой кривой, называется переохлаждением.
На фазовой диаграмме имеются две точки, представляющие особый интерес. Прежде всего, отметим, что кривая давления пара воды заканчивается точкой С. Она называется критической точкой воды. При температурах и давлениях выше этой точки пары воды не могут быть превращены в жидкую воду никаким повышением давления. Другими словами, выше этой точки паровая и жидкая формы воды перестают быть различимыми. Критическая температура воды равна 647 К, а критическое давление составляет 220 атм.
Точка Т фазовой диаграммы называется тройной точкой. В этой точке лед, жидкая вода и пары воды находятся в равновесии друг с другом. Этой точке соответствуют температура 273,16 К и давление 6,03 10-3 атм. Лишь при указанных значениях температуры и давления все три фазы воды могут существовать вместе, находясь в равновесии друг с другом.
Фазовые диаграммы P-T-состав в тетради.
Существуют фазовые переходы первого и второго рода.
Фазовый переход I рода.
Фазовым переходом первого рода называют процесс, при котором скачком изменяются внутренняя энергия, плотность, энтропия и др. свойства физической системы.
Процесс перехода I рода сопровождается поглощением или выделением тепла (теплота фазового перехода).
Примером фазового превращения I рода являются изменения агрегатного состояния вещества: превращение жидкости в газ (испарение) и обратный процесс превращение газа в жидкость (конденсация); переход вещества из твердого состояния в жидкое (плавление) и обратный переход из жидкого в твердое состояние (кристаллизация); превращение твердого тела непосредственно в газ (сублимация или возгонка).
Например, для превращения 1 кг воды в пар нужна энергия Q = 2,3106 Дж. Эта энергия необходима для преодоления сил притяжения, действующих между молекулами воды.
Полиморфные превращения из одной кристаллической модификации в другую также относятся к фазовым переходам I рода, например, полиморфное превращение алмаза в графит и обратно.
Фазовый переход II рода.
Фазовым переходом второго рода называют процесс, при котором скачком изменяется зависимость свойств вещества от температуры и давления.
При фазовых переходах второго рода энтропия, плотность, внутренняя энергия скачка не испытывают. Поэтому фазовые превращения II рода не сопровождаются поглощением или выделением тепла.
К фазовым переходам II рода относятся, например, переход жидкого гелия в сверхтекучее состояние; переход некоторых металлов и сплавов из нормального состояния в сверхпроводящее; переход магнитного вещества из ферромагнитного в парамагнитное состояние при нагревании магнетика до определенной температуры, называемой точкой Кюри.