Материал: ФХ лр37
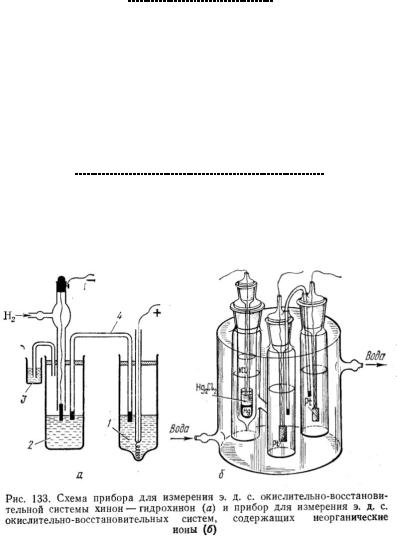
Экспериментальная часть
Задание на работу Изучить зависимость ЭДС от температуры.
По полученной зависимости рассчитать термодинамические функции реакций окисления-восстановления.
Гальванический эемент: |
|
|
||
|
| |
‖ |
| |
0,420 В |
|
|
Порядок выполнения р боты |
|
|
1. |
Собр т |
г л в нический элемент |
|
|
2. |
Собр т |
уст новку для измерения э д с |
|
|
3.Составить рабочий электролит из растворов, содержащих ионы различных степеней окисления, в равных объемных соотношениях.
4.Подкислить растворы H2SO4 с расчетом, чтобы электролитический ключ был заполнен кислотой.
5.Измерения потенциала проводить до постоянного его значения.
6.Растворы налить в термостатированную ячейку, погрузить платиновые электроды и присоединить элемент к потенциометрической измерительной схеме
7.Измерения ЭДС производить после установления температуры через каждые 15-20 минут до тех пор, пока четыре последующих измерения не покажут значения, совпадающие в пределах 0,5 мВ.
8.Далее произвести расчет
Обработка экспериментальных данных
T , K |
|
E, B |
|
E T |
p |
, B K |
|
r S , Дж K |
|
rG , |
кДж |
|
|
|
|
||||||||
|
|
|
|
|
|
||||||
288 |
|
0,413 |
|
-0,0006 |
|
-115,8 |
|
-79,709 |
|||
295 |
|
0,409 |
|
-0,0006 |
|
- |
|
- |
|
||
301 |
|
0,404 |
|
-0,0006 |
|
- |
|
- |
|
||
309 |
|
0,401 |
|
-0,0006 |
|
- |
|
- |
|
||
315 |
|
0,396 |
|
-0,0006 |
|
- |
|
- |
|
||
323 |
|
0,392 |
|
-0,0006 |
|
-115,8 |
|
-75,656 |
|||
|
|
|
|
|
|
|
|
|
|
|
|
1. Гальванический элемент:
r H , кДж
-113,059
-
-
-
-
-113,059
| |
‖ |
| |
0,420 В |
2.Уравнения электрохимических реакций (полуреакций), протекающих на электродах:
На аноде (окисление): |
|
̅ |
1,19B |
к тоде восст новление |
̅ |
|
1,61B |
Уравнение Нернста:
3.Уравнение суммарной реакции, протекающей в элементе:
4.Уравнение Нернста для расчѐта ЭДС элемента:
5.Построим график зависимости E f (T ) , на основании которого
определим величину и знак температурного коэффициента ЭДС.
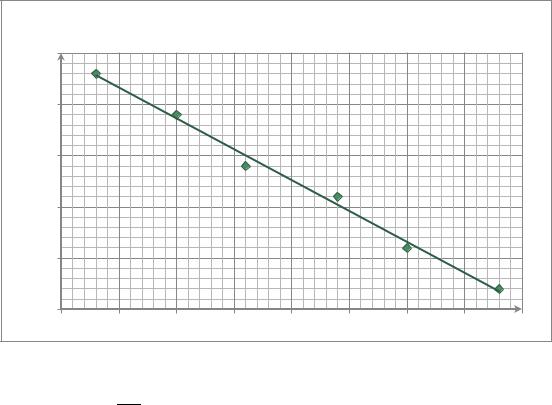
Е, В |
|
График зависимости E=f(T) |
|
|
||||
|
|
|
|
|
|
|
|
|
0,415 |
|
|
|
|
|
|
|
|
0,41 |
|
|
|
|
|
y = -0,0006x + 0,5865 |
||
|
|
|
|
|
|
|
|
|
0,405 |
|
|
|
|
|
|
|
|
0,4 |
|
|
|
|
|
|
|
|
0,395 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
T,К |
0,39 |
|
|
|
|
|
|
|
|
285 |
290 |
295 |
300 |
305 |
310 |
315 |
320 |
325 |
Из данного графика температурнй коэффициент: |
|
|
|
|||||
( )
Как видим ( |
|
) |
, поэтому с ростом температуры величина ЭДС |
|
|||
понижается. |
|
||
6.Рассчитаем изменения термодинамических функций ( rS, rG, rН) для электрохимической реакции при различных температурах.
При Т = 288К
|
|
ж |
к ж |
( |
|
) |
Дж/К |
|
ж |
к ж |
При Т = 323К
|
|
ж |
к ж |
( |
|
) |
Дж/К |
|
ж |
к ж |
При Т = 298К
о |
|
|
ж |
к ж |
|
|
|
||
о |
( |
|
) |
Дж/К |
|
|
|||
о |
о |
о |
ж |
|
|
|
|
|
|
|
|
|
|
к ж |

7.Рассчитаем константу химического равновесия реакции по данным о стандартных электродных потенциалах при 298 K.
о
о
о
Вывод:
В ходе данной лабораторной работы мы познакомились с методикой составления гальванических элементов, содержащих окислительновосстановительные электроды на примере:
| |
‖ |
| |
Так же изучили влияние температуры на ЭДС элемента:
температурнй коэффициент: ( |
|
) |
, поэтому с ростом |
|
температуры величина ЭДС понижается. Рассчитаны:
изменения термодинамических функций в процессе протекания электрохимической реакции:
И определили, что реакция экзотермическая (т.к. же отрицательна r S <0.
константа химического равновесия реакции при
|
H |
r |
|
298
<0 ). Энтропия так
K: