Материал: ФХ лр10
|
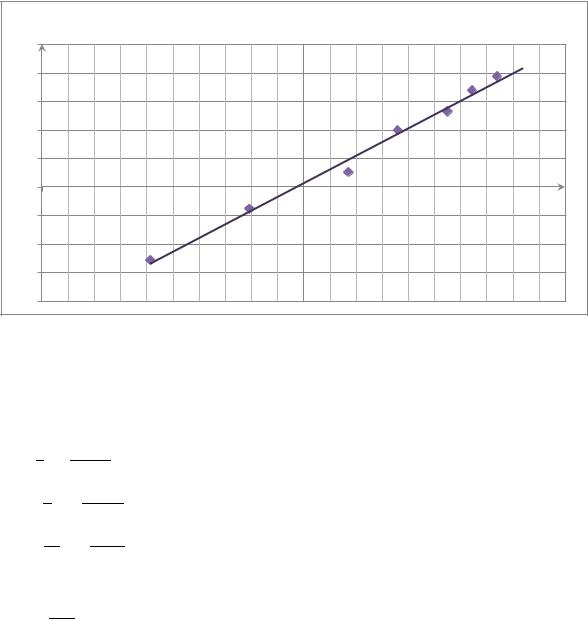
График зависимости: = ( ∆ |
) |
|
1 |
|
2 |
|
|
y = 0,9635x - 3,8232 |
||
|
|
||
|
|
|
|
0,8 |
|
|
|
0,6 |
|
|
|
0,4 |
|
|
|
0,2 |
|
|
∆ 2 |
|
|
|
|
0 |
|
|
|
3 |
|
4 |
5 |
-0,2 |
|
|
|
-0,4 |
|
|
|
-0,6 |
|
|
|
-0,8 |
|
|
|
Из графика |
|
. Т.е. реакция первого порядка |
|
Рассчитаем среднюю аналитическую константу скорости реакции: |
|||
|
) - |
для 1-го порядка |
|
( |
) |
мин-1 |
|
( ) мин-1
Аналогично рассчитываем для остальных значений (см. таблицу выше)
∑0,01894 мин-1
Период полупревращения исходного вещества:
⁄ |
|
|
|
мин |
|
|
|||
|
|
|
|
Ответ:
n=1, т.е. реакция N2O5= N2O4 + ½ O2 1-го порядка (доказано графическим вариантом дифференциального метода Вант-Гоффа)
0,01894 мин-1
⁄ мин
Экспериментальная часть
Задание на работу Исследовать процесс разложения пероксида водорода:
Н2О2 = Н2О + 0,5О2 Условия проведения эксперимента:
Катализатор: ионы Fe2+ , Fe3+, Cr2O72- , CrO42-, WO42-, MoO42-; CuSO4+MoO42-, CuSO4+NiSO4
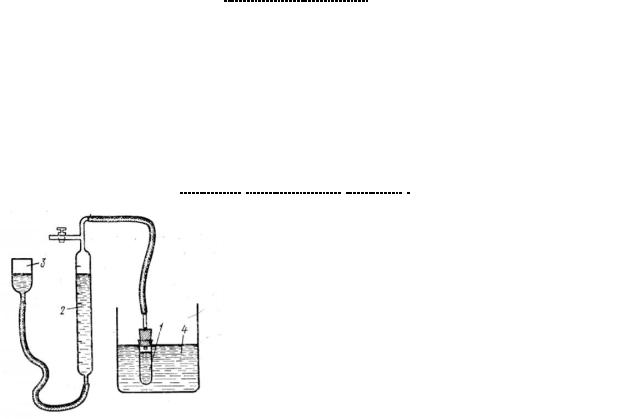
Порядок выполнения работы
Схема установки для изучения скорости разложения Н2О2 газометрическим методом: 1-реакционный сосуд 2-бюретка 3-уравнительный сосуд 4-термостат
1.Термостатировать раствор катализатора
2.Влить в колбу с раствором катализатора определѐнное количество пероксида водорода.
3.Раствор тщательно размешать и поместить в предварительно термостатированный реакционный сосуд и поместить в термостат.
4.Уравнительный сосуд и бюретку наполнить подкрашенной водой и, присоединив реакционный сосуд к бюретке, проверить установку на герметичность.
Установить одинаковые уровни жидкости в бюретке и уравнительном сосуде.
Записать первое и последующие измерения с интервалом 2-5 минут.
5.После того, как реакция практически прекратится, реакционный сосуд поместить в кипящую водяную баню на некоторое время. Реакция считается законченной, если уровень газа в бюретке не изменяется.
6.После полного разложения пероксида водорода реакционный сосуд охладить до температуры термостата.
7.Произвести расчет.

Обработка экспериментальных данных
№ |
t, мин |
VO2, мл |
, мл |
) |
k, мин-1 |
п/п |
|
|
|
|
|
|
|
|
|
|
|
1 |
5 |
6,4 |
60,8 |
4,108 |
0,02002 |
|
|
|
|
|
|
2 |
7 |
12,0 |
55,2 |
4,011 |
0,0281 |
|
|
|
|
|
|
3 |
9 |
17,2 |
50 |
3,912 |
0,0329 |
|
|
|
|
|
|
4 |
11 |
21,6 |
45,6 |
3,820 |
0,0353 |
|
|
|
|
|
|
5 |
13 |
25,8 |
41,4 |
3,723 |
0,0373 |
|
|
|
|
|
|
6 |
15 |
29,6 |
37,6 |
3,627 |
0,0387 |
|
|
|
|
|
|
7 |
17 |
32,8 |
34,4 |
3,538 |
0,0394 |
|
|
|
|
|
|
8 |
19 |
35,4 |
31,8 |
3,459 |
0,0394 |
|
|
|
|
|
|
9 |
21 |
37,2 |
30 |
3,401 |
0,0384 |
|
|
|
|
|
|
10 |
23 |
39,6 |
27,6 |
3,318 |
0,0387 |
|
|
|
|
|
|
11 |
25 |
42,0 |
25,2 |
3,227 |
0,0392 |
|
|
|
|
|
|
12 |
27 |
44,4 |
22,8 |
3,127 |
0,04003 |
|
|
|
|
|
|
13 |
29 |
46,2 |
21 |
3,045 |
0,0401 |
|
|
|
|
|
|
14 |
31 |
47,6 |
19,6 |
2,976 |
0,0397 |
|
|
|
|
|
|
15 |
33 |
49,4 |
17,8 |
2,879 |
0,0403 |
|
|
|
|
|
|
16 |
35 |
51,0 |
16,2 |
2,785 |
0,0406 |
|
|
|
|
|
|
17 |
37 |
52,2 |
15 |
2,708 |
0,0405 |
|
|
|
|
|
|
18 |
39 |
53,4 |
13,8 |
2,625 |
0,0406 |
|
|
|
|
|
|
19 |
41 |
54,2 |
13 |
2,565 |
0,04007 |
|
|
|
|
|
|
∞ |
∞ |
67,2 |
- |
- |
- |
|
|
|
|
|
|
Рассчитаем среднюю аналитическую константу скорости реакции:
,
где - объем кислорода, выделившийся после разложения всего Н2О2, - объем кислорода, выделившийся в момент измерения t.
( |
|
|
|
) |
|
|
|
( |
|
|
) |
мин-1 |
|
|
|
|
|
|
|
|
|||||||
( |
|
) |
|
|
( |
|
|
) |
мин-1 |
||||
|
|
|
|
|
|||||||||
|
( |
) |
( |
) |
|
мин-1 |
|
|
|
Аналогично рассчитываем для остальных значений, данные занесены в |
|||||||||
таблицу выше. |
|
|
|
|
|
|
|
|
|
Тогда получаем, |
|
∑ |
0,03733 мин-1 |
|
|
|
|||
|
|
|
|
|
|||||
Теперь определим константу скорости графическим методом. Для этого |
|||||||||
построим график зависимости в координатах |
|
) = f(t) |
|
||||||
|
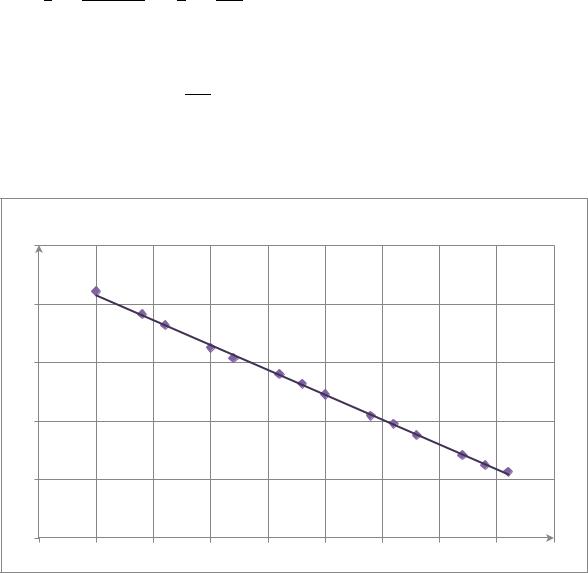
График зависимости в ( |
− ) = f(t) |
|
||||||
4,5 |
|
|
|
|
|
∞ |
|
|
|
( ∞− ) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
y = -0,0428x + 4,2918 |
||
4 |
|
|
|
|
|
|
|
|
|
3,5 |
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
2,5 |
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
t, мин |
|
|
|
|
|
|
|
|
|
|
0 |
5 |
10 |
15 |
20 |
25 |
30 |
35 |
40 |
45 |
По графику |
|
|
; |
|
|
|
|
|
|
Из этого следует, что |
|
мин-1 |
|
|
|
|
|||
Определим порядок реакции графическим методом. Для этого построим |
|||||||||
график зависимости |
|
|
. По нему определим скорость реакции |
||||||
в определенный момент времени: |
|
. Далее построим график |
|||||||
зависимости: |
|
|
|
, где |
|
|
|
|
|
|
|
|
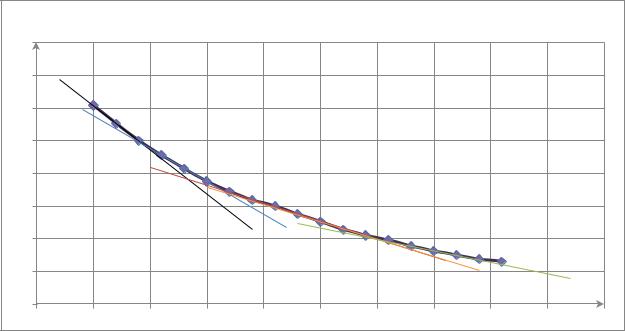
График зависимости ( |
∞ |
− )= ( ). |
|
|
|||||
80 |
∞− , |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
мл |
|
|
|
|
|
|
|
|
|
|
|
70 |
|
|
|
|
|
|
|
|
|
|
|
|
60 |
|
|
|
|
|
|
|
|
|
|
|
|
50 |
|
|
|
|
|
|
|
|
|
|
|
|
40 |
|
|
|
|
|
|
|
|
|
|
|
|
30 |
|
|
|
|
|
|
|
|
|
|
|
|
20 |
|
|
|
|
|
|
|
|
|
|
|
|
10 |
|
|
|
|
|
|
|
|
|
|
|
|
0 |
|
|
|
|
|
|
|
|
|
|
|
, мин |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0 |
5 |
10 |
15 |
20 |
25 |
30 |
35 |
40 |
45 |
50 |
|
Из данного графика : |
|
|
При |
мл/мин |
|
При |
мл/мин |
|
При |
мл/мин |
|
При |
мл/мин |
|
При |
мл/мин |
|
Далее построим график зависимости: |
, по которому и |
|
определим порядок реакции: |
|
|
при
при
при
при
при