Материал: ФХ лр10
Работа №10
Изучение скорости разложения пероксида водорода газометрическим методом.
Цель работы: изучить реакцию разложения пероксида водорода, газометрическим методом определить константу скорости реакции. Используя результаты расчета и графические зависимости определить, протекает ли данная реакция по первому порядку.
Литература: Практикум 1986, с.319-324, 328-333, 339-340, 354-356 или Практикум 1974, с.322-346, 365-367.
Теоретическая часть
Скорость химической реакции определяется изменением количества данного компонента в единицу времени в единице объема:
|
|
1 |
dn |
i 0 |
|
|
|||
i |
|
V d |
||
|
|
|||
где n-число молей данного компонента в объеме V данной фазы в момент времени t.
Если объем величина постоянная, то скорость определяется изменением концентрации реагирующего вещества за единицу времени:
V const : |
|
d n |
i |
/ V |
|
d c |
i |
|
|
|
|||||
i |
|
d |
|
d |
|||
|
|
|
|||||
Скорость реакции всегда положительна.
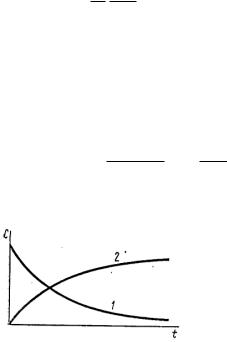
Кинетические кривые для исходных веществ(1) и продуктов реакции(2)
Основной постулат химической кинетики:
скорость реакции в каждый момент времени пропорциональна произведению возведенных в некоторую степень концентраций реагирующих веществ (закон действующих масс).
|
А |
А |
B |
B |
D |
D ... продукты, |
||
|
|
|
|
|
||||
|
|
|
|
d ci |
kcAp cBq cDr |
|||
|
|
|
|
|||||
|
|
|
|
|
i d |
|
||
Коэффициент пропорциональности k называется константой скорости химической реакции. Ее физический смысл: константа скорости равняется
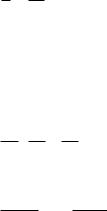
скорости реакции при единичной концентрации, поэтому ее называют также удельной скоростью реакции.
k (c |
1) |
i |
|
Величина константы зависит от всех факторов, которые влияют на скорость химической реакции, за исключением изменения концентрации реагирующих веществ. Числовое значение зависит так же от выбора единиц времени и концентрации. Размерность определяется тем кинетическим уравнением, по которому производится ее расчет, т.е. зависит от порядка реакции
Порядок реакции является эмпирической величиной. Частным называется порядок, характеризующийся изменением концентрации одного из веществ, вступающих в реакцию. Чтобы определить порядок по данному веществу, необходимо создать такие условия, чтобы в процессе реакции изменялась концентрация только данного вещества. Для этого концентрации всех остальных участников должны быть взяты в большом избытке. Сумма частных порядков дает общий порядок реакции.
Молекулярность реакции определяется числом частиц, участвующих в одном элементарном акте химического превращения.
Период полупревращения-это время, за которое исходная концентрация реагента уменьшится в 2 раза. Измерение периода полупревращения приносит большую пользу при исследованиях порядка реакции.
Математические выражения для расчета констант скорости реакций: 1. Необратимые реакции 1-го порядка
k1 ln c0
c
, k, с 1
2. Необратимые реакции 2-го порядка
|
1 |
|
1 |
|
1 |
|
|
1 |
|
x |
|
л |
|||
k |
|
|
|
|
|
|
|
|
|
|
|
|
|
, k, |
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
с |
|
|
|
|
c0 c0 x |
|
с моль |
|||||
|
|
|
с0 |
|
|
||||||||||
3. Необратимые реакции 3-го порядка
k |
1 |
|
1 |
|
|
|
|
2 |
|
|
2 |
|
c |
|
|
|
|
||
|
|
|
|
|
|
1 |
||
c |
2 |
||
|
|||
|
0 |
||
|
|
||
, k, |
л2 |
моль2 с |
4. Необратимые реакции нулевого порядка
k
c |
0 |
c |
|
|
|
|
|
|
,
k, |
моль |
|
л с |
||
|
Где с0– начальная концентрация исходных веществ, с – концентрация после протекания реакции, t – время, х – концентрация прореагировавшего вещества за промежуток времени
Методы определения порядка реакции 1. Интегральные методы определения порядка реакции
а) метод подбора уравнения
1)аналитический – суть метода состоит в подстановке ci реагирующего
вещества для различных моментов времени от начала реакции в кинетические уравнения различных порядков (1го, 2го , 3го и т.д ). Искомым является тот порядок, для которого наблюдается постоянство (неизменность) значения константы скорости реакции при различных концентрациях
2)графический – состоит в нахождении такой функции концентрации от времени, которая имела бы линейный характер:
1 порядок -
2 порядок -
3 порядок -
0 порядок -
lnc k const lnc0 |
, |
|||
1/ c k const 1/ c0 , |
|
, |
||
1/ c |
2 |
2 |
||
|
2k const 1/ c0 |
|
||
с k c0 .
б) метод Оствальда-Нойеса – использует зависимость
|
lg |
/ |
|
|
|
n |
1/ 2 |
1/ 2 |
1 |
||
lg c |
|
/ c |
|
||
|
0,2 |
0,1 |
|
||
|
|
|
|
||
1
2
f
c |
0 |
|
:
3. Дифференциальные методы Вант-Гоффа а) Аналитический метод – по двум значениям
dc d
при двух
c
1) по одной кинетической кривой – временной порядок
|
|
|
dc |
|
|
dc |
||
|
lg |
|
|
|
lg |
|
|
|
|
|
|
||||||
n |
|
|
d 1 |
|
|
d 2 |
||
|
|
lg c1 |
lg c2 |
|
|
|||
|
|
|
|
|
||||
2) по 2ум начальным концентрациям – концентрационный порядок
|
|
|
dc |
|
|
|
dc |
|
|
lg |
|
|
lg |
|
|||
n |
|
|
d |
0,1 |
|
|
|
d |
|
|
|
|
|
|
|
|
|
|
|
|
lg c |
0,1 |
lg c |
0,2 |
||
|
|
|
|
|
|
|||
0,2
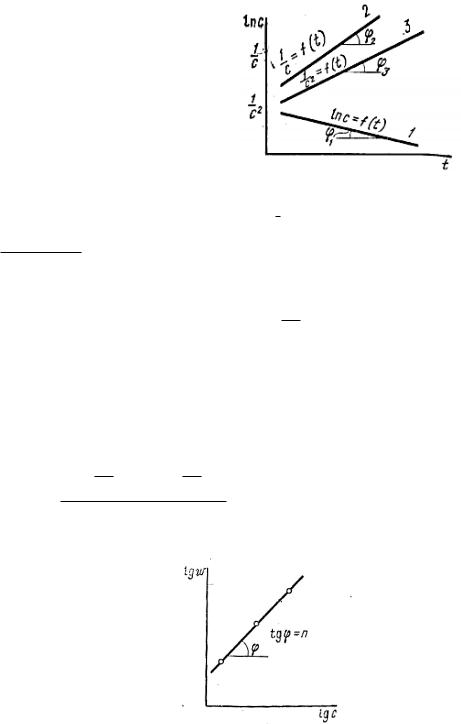
б) Графический вариант метода Вант-Гоффа
lg lg k n lg c
tg n
Задача
Кинетику реакции разложения N2O5 в жидком CCL4 изучали при температуре 42оС газоволюметрическим методом. Результаты измерений объемов кислорода, выделившегося в разные моменты времени, представлены в таблице:
t, |
5 |
10 |
15 |
20 |
30 |
40 |
60 |
80 |
100 |
∞ |
мин |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
VO2, |
12,45 |
23,8 |
34,15 |
43,5 |
59,85 |
73,3 |
93,7 |
107,7 |
117,7 |
138,1 |
мл |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Графическим вариантом дифференциального метода Вант-Гоффа определить порядок химической реакции: N2O5= N2O4 + ½ O2
Рассчитать среднюю аналитическую константу скорости реакции и период полупревращения исходного вещества при указанной температуре.
Решение.
Определим порядок реакции графическим методом. Для этого построим
график зависимости |
|
. По нему определим скорость реакции в |
определенный момент времени: |
. Далее построим график |
|
зависимости: |
, где |
|
, |
|
, где |
|
мл |
|
|
|
|
|
|
|
|
|
t, мин |
, мл |
|
) |
v, мл/мин |
lnv |
k, мин-1 |
|
|
|
|
|
|
|
5 |
125,65 |
4,83 |
|
- |
- |
0,01890 |
|
|
|
|
|
|
|
10 |
114,3 |
4,74 |
|
2,17 |
0,775 |
0,01892 |
|
|
|
|
|
|
|
15 |
103,95 |
4,64 |
|
1,97 |
0,678 |
0,01894 |
|
|
|
|
|
|
|
20 |
94,6 |
4,55 |
|
1,7 |
0,531 |
0,01892 |
|
|
|
|
|
|
|
30 |
78,25 |
4,36 |
|
1,49 |
0,399 |
0,01894 |
|
|
|
|
|
|
|
40 |
64,8 |
4,17 |
|
1,11 |
0,104 |
0,01892 |
|
|
|
|
|
|
|
60 |
44,4 |
3,79 |
|
0,86 |
-0,151 |
0,01891 |
|
|
|
|
|
|
|
80 |
30,4 |
3,41 |
|
0,6 |
-0,511 |
0,01892 |
|
|
|
|
|
|
|
100 |
20,4 |
3,02 |
|
- |
- |
0,01912 |
|
|
|
|
|
|
|
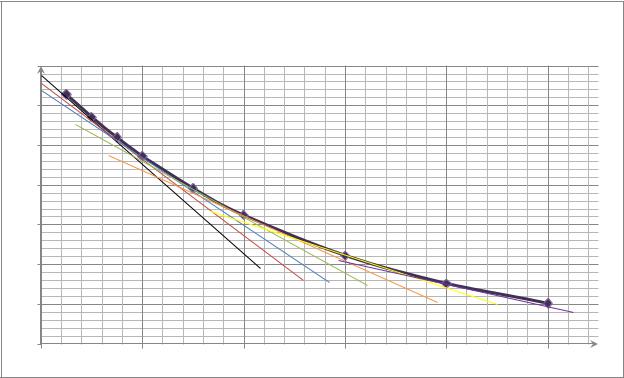
∆ |
2 |
, |
|
График зависимости ∆ 2= ( ). |
|
||
|
|
|
|
|
|
|
|
мл |
|
|
|
|
|
|
|
140 |
|
|
|
|
|
|
|
120 |
|
|
|
|
|
|
|
100 |
|
|
|
|
|
|
|
80 |
|
|
|
|
|
|
|
60 |
|
|
|
|
|
|
|
40 |
|
|
|
|
|
|
|
20 |
|
|
|
|
|
|
|
0 |
|
|
|
|
|
|
t, мин |
|
|
|
|
|
|
|
|
0 |
|
|
20 |
40 |
60 |
80 |
100 |
Из данного графика : |
|
|
При |
мл/мин |
|
При |
мл/ мин |
|
При |
мл/ мин |
|
При |
мл/ мин |
|
При |
мл/ мин |
|
При |
мл/ мин |
|
При |
мл/ мин |
|
Далее построим график зависимости: |
, по которому и |
|
определим порядок реакции: |
|
|