Материал: Фазовое равновесие - лекция 3
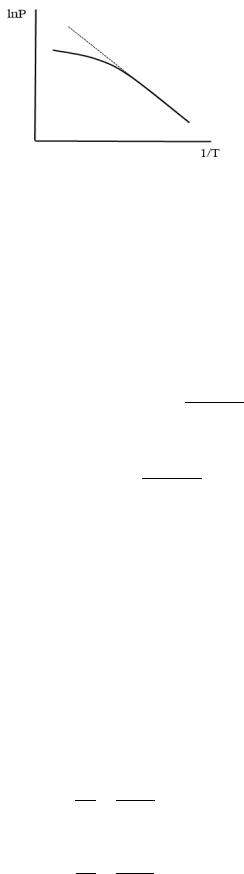
Правило Трутона
Теплоты испарения различных жидкостей закономерно связаны с их нормальными
температурами кипения.
Существует эмпирическое правило, которое носит название правила Трутона: Мольные
энтропии испарения неполярных неассоциированных жидкостей при нормальной
температуре кипения примерно одинаковы и в среднем составляют:
∆исп. = |
∆исп. |
≈ |
± |
Дж |
н.т.к. |
моль ∙ К |
В справочнике, на стр. 109 правило Трутона приведено в следующем виде:
∆исп. |
≈ , |
Дж |
н.т.к. |
моль ∙ К |
Это правило выполняется только для неполярных, неассоциированных в паровой фазе жидкостей и только при нормальной температуре кипения, которая у каждого вещества
единственная.
Интегрирование уравнения Клапейрона для процесса плавления
Т.к. мольные (удельные) объемы твердой и жидкой фаз очень близки друг другу по величине ( ж ≈ тв), уравнение Клапейрона для процесса плавления (а равно как и для процессов полиморфного превращения) преобразовать нельзя, и оно используется только в
таком виде:
= ∆пл.
∆
Или, что больше отвечает физическому смыслу процесса:
= ∆
∆пл.
Величина , определяющая наклон линии плавления к оси температур, хоть и является,
в свою очередь, функцией давления и температуры, но изменяется незначительно при
6

достаточно большом увеличении давления. Поэтому при изменении давления до 10 атм (иногда
и более) в хорошем приближении можно считать, что |
= |
, и линия плавления является |
||||||||
прямой линией. |
|
|
|
|
|
|
|
|
|
|
Соответственно, интегрирование уравнения Клапейрона-Клаузиуса для процесса |
||||||||||
плавления проводится следующим образом: |
|
∆пл. |
|
|
|
|||||
|
|
|
|
|
= |
|
|
|
||
|
|
|
|
|
|
|
||||
|
|
|
приблизительно постоянная величина, рассчитанная, |
|||||||
Cоотношение |
∆ |
берется как |
|
|
|
|
∆ |
|
|
|
|
∆ |
|
|
|
|
|
|
|
|
|
например, при температуре , и выносится за знак интеграла: |
|
|||||||||
|
|
|
= |
∆пл. |
|
|
||||
|
|
|
|
∆ |
|
|
|
|||
∆
Другими словами, заменяем на ∆ .
∆ |
= |
∆пл. |
|
∆ |
|||
− |
= |
∆пл. |
|
|
∆ |
||
= |
+ |
∆пл. |
|
|
∆ |
||
∆
( − )
( − )
Так можно рассчитать, при каком давлении температура плавления станет равной ,
если известна при ,
или рассчитать температуру плавления при заданном давлении:
= + |
∆ |
( − ) |
∆пл. |
Расчет теплоты плавления
В основе – уравнение Клапейрона:
= ∆пл.
∆
1) Аналитический расчет Проводится по известной зависимости = ( ).
Пусть эта зависимость имеет вид:
=+ +
где А, В, С – постоянные коэффициенты уравнения.
Выразим теплоту плавления из уравнения Клапейрона:
7
∆пл. = ∆
Продифференцируем зависимость = ( ) по давлению:
=+ 2
∆
∆ = ( + 2 )
Подставляя в полученное выражение необходимые значения p и Т, находим ∆Н.
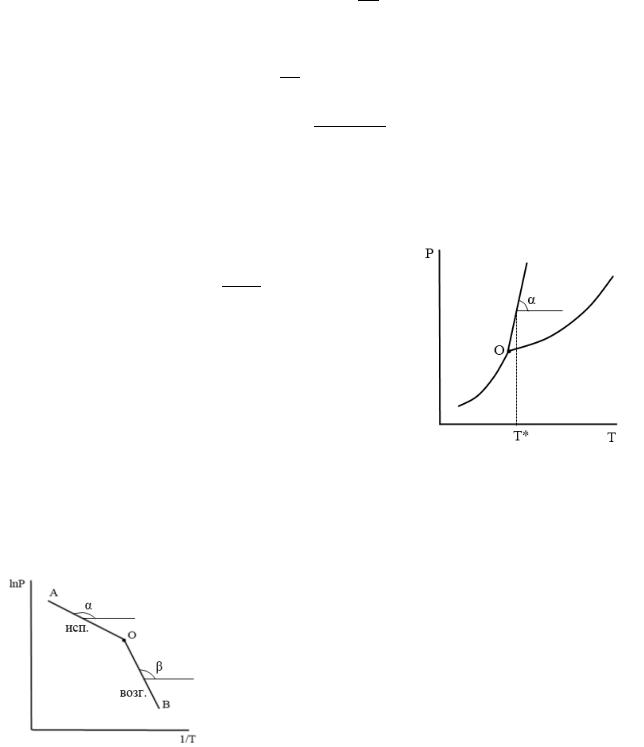
2) Графический расчет По наклону линии плавления:
= |
|
|
= |
∆пл. |
|
|
∆ |
||
Отсюда выражаем ∆ |
: |
|
|
|
∆пл. = ∆
Подставляя сюда значение Т* и тангенса угла наклона линии плавления, получаем значение теплоты плавления.
3) Расчет теплоты плавления в тройной точке по теплотам испарения и возгонки
а) по графику |
− |
|
. |
|
Находим теплоты испарения и возгонки по тангенсу угла наклона соответствующих прямых:
∆исп. = − ∙
∆возг. = − ∙
Затем находим теплоту плавления по соотношению:
∆пл. = ∆возг. − ∆исп.
ОА – линия испарения, ОВ – линия возгонки, т. О – тройная точка.
8
Если известны уравнения линий испарения и возгонки:
ln |
ж = |
+ |
′ |
ln |
тв = |
+ |
′′ |
то можно найти теплоты испарения и возгонки через коэффициенты уравнений:
∆исп. = − ∙ и ∆возг. = − ∙ ′′
Теплоту плавления находим по разности теплот испарения и возгонки.
∆пл. = ( − )
Теплота плавления:
∆пл. = ∆возг. − ∆исп.
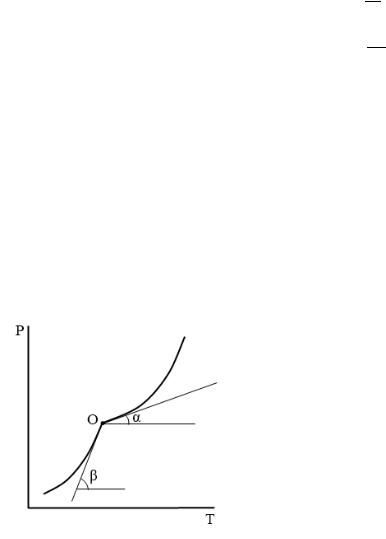
б) по графику − .
Проводим касательные к кривым испарения и возгонки в тройной точке:
|
|
|
|
|
∆исп. |
= |
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
∆возг. |
= |
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
В этих формулах Т и Р соответствуют температуре и |
|||||||||
|
|
давлению тройной точки. |
= ∆возг. − ∆исп. или: |
||||||||
|
|
Теплота плавления: |
∆пл. |
||||||||
∆пл. = |
|
− |
|
= |
|
( |
− |
) |
|
||
|
|
|
|
||||||||
Расчет изменения внутренней энергии и энтропии при фазовых превращениях
Расчет изменения внутренней энергии |
|
и энтропии |
|
∆ |
для фазового перехода осуще- |
|
ствляется после того, как найдено значение |
теплового эффекта |
. |
||||
|
∆ |
|
∆ |
|
|
|
Изменение внутренней энергии
Рассчитывается по соотношению:
∆ф.п. = ∆ф.п. − ∆ф.п.
а) Плавление
∆пл. = 0
Следовательно
∆пл. = ∆пл.
9

б) Испарение, возгонка
∆исп.(возг.). = 1 ∆исп.(возг.) = ∆исп.(возг.) −
Для обратного перехода (конденсации):
∆конд = −1
∆конд. = −∆исп.(возг.)
Изменение энтропии
∆ф.п. = ∆ф.п.
Для конденсации:
∆конд. = −∆исп.(возг.)
10