Материал: Энергоснабжение космических аппаратов
В КЭУ на основе ЭХИТ используются электрические аккумуляторы
с одноразовым или многоразовым режимами разряда, а также водородно-кислородные
топливные элементы. [6]
3.1 Химические источники тока
Электродвижущей силой (ЭДС) химических источников называется разность его электродных потенциалов при разомкнутой внешней цепи:
где ![]() и
и ![]() - соответственно
потенциалы положительного и отрицательного электродов.
- соответственно
потенциалы положительного и отрицательного электродов.
Полное внутреннее сопротивление Rхимического источника
(сопротивление постоянной силе тока) состоит из омического сопротивления ![]() и сопротивления
поляризации
и сопротивления
поляризации ![]() :
:
![]() ,
,
где ![]() - ЭДС поляризации;
- ЭДС поляризации; ![]() - сила тока разряда.
- сила тока разряда.
Сопротивление поляризации ![]() обусловлено изменением
электродных потенциалов
обусловлено изменением
электродных потенциалов ![]() и
и ![]() при протекании тока и
зависит от степени заряженности, силы разрядного тока, состава электродов и
чистоты электролита.
при протекании тока и
зависит от степени заряженности, силы разрядного тока, состава электродов и
чистоты электролита.
Напряжение химических источников электроэнергии отличается от
ЭДС на значение падения напряжения во внутренней цепи, что определяется полным
внутренним сопротивлением и протекающим током:
![]() ;
;
![]() ,
,
где ![]() и
и ![]() - разрядные и зарядные
напряжения на источнике соответственно;
- разрядные и зарядные
напряжения на источнике соответственно; ![]() и
и ![]() - сила токов разряда и
заряда соответственно.
- сила токов разряда и
заряда соответственно.
Для гальванических элементов одноразового применения
напряжение определяется как разрядное![]() .
.
Разрядная емкость Q (А·ч) химического источника есть количество
электричества, отдаваемое источником во время разряда при определенных
температуре электролита, окружающем давлении, силе раз рядного тока и конечном
разрядном напряжении:
![]() ,
,
и в общем случае при постоянной во время разряда силе тока
![]() ,
,
где ![]() - текущее значение силы тока разряда, А;
- текущее значение силы тока разряда, А; ![]() - время разряда, ч.
- время разряда, ч.
Номинальная емкость химического источника тока - это емкость, которую должен отдавать источник при оговоренных техническими условиями режимах работы. Для аккумуляторов КА за номинальную и силу тока разряда чаще всего принимают силу тока одно-двух или 10 часового режима разряда.
Саморазряд - бесполезная потеря емкости химическим источником
при разомкнутой внешней цепи. Обычно саморазряд выражается в% за сутки
хранения:
![]() ,
,
где ![]() и
и![]() - емкости химического источника до и после
хранения; Т - время хранения, сут.
- емкости химического источника до и после
хранения; Т - время хранения, сут.
Удельная энергия химического источника тока представляет
собой отношение отдаваемой энергии к его массе:
![]() .
.
Значение удельной энергии зависит не только от типа источника, но и от силы разрядного тока, т.е. от отбираемой мощности. Поэтому химический источник электроэнергии более полно характеризуется зависимостью удельной энергии от удельной мощности.
В качестве химических источников тока рассмотрены
серебряноцинковые, кадмиево-никелевые и никель-водородные аккумуляторные
батареи. [8]
3.2 Серебряно-цинковые аккумуляторные батареи
Серебряно-цинковые аккумуляторы благодаря меньшей массе и объему при той же емкости и меньшему внутреннему сопротивлению при заданном напряжении получили распространение в космическом электрооборудовании. Активным веществом положительного электрода аккумулятора является окись серебра AgO, а отрицательной пластины - металлический цинк. В качестве электролита используется водный раствор щелочи КОН плотностью 1,46 г./см3.
Заряд и разряд аккумулятора происходит в две ступени. При разряде на обеих ступенях на отрицательном электроде протекает реакция окисления цинка
+ 2OH ˉ разряд → ZnO + H2O + 2e.
На положительном электроде в-две ступени протекает реакция
восстановления серебра. На первой ступени двухвалентная окись серебра
восстанавливается до одновалентной:
2AgO + 2e + H2Oразряд → Ag2O + 2OH ˉ.
ЭДС аккумулятора при этом равна 1,82.. 1,86 В, На второй ступени, когда аккумулятор разрядится примерно на 30%, происходит восстановление одновалентной окиси серебра до металлического серебра:
2O + 2e + H2Oразряд → 2Ag + 2OH ˉ.
ЭДС аккумулятора в момент перехода от первой ступени разряда
до второй снижается до 1,52.. 1,56 В. Вследствие этого кривая 2 изменения ЭДС
при разряде номинальным током (рисунок 3.2) имеет характерный скачок. При
дальнейшем разряде ЭДС аккумулятора остается постоянной, пока аккумулятор не
разрядится полностью. При заряде реакции протекает в две ступени. Скачок
напряжения и ЭДС возникает, когда аккумулятор зарядится примерно на 30%
(кривая1), В этом состоянии поверхность электрода покрывается двухвалентной
окисью серебра.
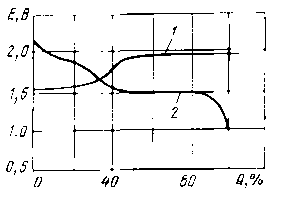
Рис. 3.2 - ЭДС аккумулятора при заряде (1) и разряде (2)
В конце заряда, когда прекращается окисление серебра из одновалентного в двухвалентное во всей толще электрода, начинается выделение кислорода по уравнению
OH ˉ разряд → 2H2O + 4e +O2
ЭДС аккумулятора при этом повышается на 0,2…0,3 В (см. рисунок 5.1, пунктирный участок на кривой 1). Выделяющийся при перезарядке кислород ускоряет процесс разрушения целлофановых параметров аккумулятора и возникновения внутренних коротких замыканий.
В процессе заряда вся окись цинка может быть восстановлена до
металлического цинка. При перезаряде восстанавливается окись цинка электролита,
находящегося в порах электрода, а затем и в сепараторах отрицательных пластин,
роль которых выполняют несколько слоев целлофановой пленки. Цинк выделяется в
виде кристаллов, которые растут в сторону положительного электрода, образуя
цинковые дендрита. Такие кристаллы способны протыкать целлофановые пленки и
вызывать короткие замыкания электродов. Цинковые дендриты не вступают в
обратные реакции. Опасны поэтому даже кратковременные перезаряды. [5]
3.3 Кадмиево-никелевые аккумуляторные батареи
Активным веществом отрицательного электрода в кадмиево-никелевом аккумуляторе является металлический кадмий. Электролитом в аккумуляторе служит водный раствор едкого калия КОН плотностью 1,18… 1,40 г./см3.
В кадмиево-никелевом аккумуляторе используется окислительно-восстановительная реакция между кадмием и гидратом окиси никеля:
+ 2Ni(OH)3 → Cd(OH)2
+ 2Ni(OH)2
Упрощенно химическую реакцию на электродах можно записать следующим образом. На отрицательном электроде при разряде происходит окисление кадмия:
- 2e → Cd++
Ионы кадмия связываются с гидроксильными ионами щелочи, образуя гидрат кадмия:
- 2e + 2OH ˉ разряд → Cd(OH)2.
На положительном электроде при разряде восстанавливается
никель с трехвалентного до двухвалентного:
2Ni(OH)3 + 2eразряд → 2Ni(OH)2 + 2OH ˉ.
Упрощение состоит в том, что состав гидроокиси не соответствует точно их формулам. Соли кадмия и никеля малорастворимы в воде, поэтому концентрация ионов Cd++, Ni++, Ni+++определяется концентрацией КОН, от которой в электролите косвенно зависит и величина ЭДС аккумулятора.
Электродвижущая сила только что заряженного аккумулятора
равна 1,45 В.В течение нескольких суток после конца заряда происходит снижение
ЭДС до 1,36 В.
3.4 Никель-водородные аккумуляторные батареи
Никель-водородные аккумуляторные батареи (НВАБ), обладая высокой надежностью, большими ресурсом и удельной энергией, отличными эксплуатационными показателями, найдут широкое применение в КА взамен никель-кадмиевых аккумуляторов.
Для работы НВАБ на низкой околоземной орбите (НОО) требуется ресурс порядка 30 тыс. циклов в течение пяти лет. Использование АБ на НОО с малой глубиной разряда (ГР) ведет к соответственному снижению гарантируемой удельной энергии (30 тыс. циклов может быть достигнуто при ГР 40%). Трехлетнее непрерывное циклирование в режиме НОО при ГР = 30% двенадцати стандартных НВАБ (RNH-30-1) емкостью 30 А · ч показали, что все НВАБ проработали стабильно 14 600 циклов.
Достигнутый уровень удельной энергии для НВАБ составляет в
условиях околоземной орбиты 40 Вт · ч/кг при глубине разряда 100%, ресурс
при ГР 30% составляет 30 тыс. циклов.
4/ Выбор параметров солнечных батарей и
буферных накопителей
Исходные данные:
Предельная масса КА - Мп = до 15 кг;
Высота круговой орбиты - h = 450 км;
Масса целевой системы - не более 0,5 кг;
Передающая частота - 24 ГГц;
Потребляемое напряжение - 3.3 - 3.6 В;
Минимальная потребляемая мощность трансивера - 300 мВт;
Потребляемая мощность плазмено-ионного двигателя - 155 Вт;
Срок активного существования - 2-3 года.
4.1 Расчет параметров буферного накопителя
Расчет параметров буферного накопителя (БН) из аккумуляторных батарей и определение их состава ведется исходя из ограничений, накладываемых на аккумуляторы по силам зарядного и разрядного токов, интегральной емкости разряда, разовым глубинам разряда, надежности, температурных условий работы и т.д.
При расчете параметров никель-водородных аккумуляторов, воспользуемся следующими характеристиками и формулами [«Конструирование автоматических космических аппаратов» авторы: Д.И. Козлов, Г.Н. Аншаков, В.Ф. Агарков, Ю.Г. Антонов § 7.5], а также техническими характеристиками АБ HB-50 НИАИ Источник, информация о котором взята с сайта [#"883662.files/image013.gif">, (1)
![]() , (2)
, (2)
где ![]() и
и ![]() - разрядные и зарядные
напряжения на источнике соответственно;
- разрядные и зарядные
напряжения на источнике соответственно; ![]() и
и ![]() - сила токов разряда и
заряда соответственно.
- сила токов разряда и
заряда соответственно.
Для гальванических элементов одноразового применения
напряжение определяется как разрядное![]() .
.
![]() , (3)
, (3)
Номинальная емкость химического источника тока - это емкость, которую должен отдавать источник при оговоренных техническими условиями режимах работы. Для аккумуляторов КА за номинальную и силу тока разряда чаще всего принимают силу тока одно-двух или 10 часового режима разряда.
Саморазряд - бесполезная потеря емкости химическим источником
при разомкнутой внешней цепи. Обычно саморазряд выражается в% за сутки
хранения:
![]() (4)
(4)
где ![]() и
и![]() - емкости химического источника до и после
хранения; Т - время хранения, сут.
- емкости химического источника до и после
хранения; Т - время хранения, сут.
Удельная энергия химического источника тока представляет
собой отношение отдаваемой энергии к его массе:
![]() (5)
(5)
Значение удельной энергии зависит не только от типа источника, но и от силы разрядного тока, т.е. от отбираемой мощности. Поэтому химический источник электроэнергии более полно характеризуется зависимостью удельной энергии от удельной мощности.
Расчет параметров:
Определим максимальное и минимальное время разряда из формулы
[3]:
![]() (3)
(3)
Следовательно, максимальное время разряда:
![]() ;
;
минимальное время разряда:
![]() .
.
Отсюда следует, что время разряда позволяет проектируемому спутнику использовать электрический ток в среднем в течении 167 мин или 2,8 часа, так как наша целевая установка использует 89 мА, время разряда будет не существенным, что положительно сказывается на обеспечение электрическим током других жизненно важных систем спутника.
Определим напряжение разряда и полное внутреннее
сопротивление аккумулятора из формулы [1]:
![]() ; (1)
; (1)
![]()
![]()
![]() (2)
(2)
![]() .
.
Отсюда видно, что напряжение заряда в достаточной мере может обеспечиваться при помощи использования солнечных батарей, даже не большой площади.
Также можно определить саморазряд по формуле [4]:
![]() (4)
(4)
Возьмем за время работы аккумулятора Т = 0,923 ч, Q1 = 50 (А·ч) и Q2 = 6 (А·ч) за тридцать минут работы:
![]() ,
,
то есть при минимальном потреблении тока в 12 А, за 30 минут аккумуляторная батарея разредится на 95% при разомкнутой цепи.
Найдем удельную энергию химического источника по формуле [5]:
![]() ,
,
то есть 1 кг химического источника может обеспечить 61,2 Вт в
течении часа, что также подходит для нашей целевой установки, которая при
работает при максимальной мощности 370 мВт.
4.2 Расчет параметров солнечных батарей
Для расчетов основных параметров СБ влияющих на конструкцию КА, его технических характеристик воспользуемся следующими формулами [«Конструирование автоматических космических аппаратов» авторы: Д.И. Козлов, Г.Н. Аншаков, В.Ф. Агарков, Ю.Г. Антонов § 7.5]:
Расчет параметров СБ сводится к определению ее площади и массы.
Расчет мощности СБ производится по формуле:
![]() (6)
(6)
где ![]() - мощность СБ; Рн - среднесуточная
мощность нагрузки (без учета собственных нужд СЭП);
- мощность СБ; Рн - среднесуточная
мощность нагрузки (без учета собственных нужд СЭП);![]() - время ориентации СБ на
Солнце за виток; tT - время, в течение которого СБ не освещена;
- время ориентации СБ на
Солнце за виток; tT - время, в течение которого СБ не освещена; ![]() - КПД регулятора избытка
мощности СБ, равный 0,85;
- КПД регулятора избытка
мощности СБ, равный 0,85; ![]() - КПД регулятора разряда БН, равный 0,85;
- КПД регулятора разряда БН, равный 0,85; ![]() р.3 - КПД
регулятора заряда БН, равный 0,9;
р.3 - КПД
регулятора заряда БН, равный 0,9; ![]() - КПД аккумуляторных
батарей БН, равный 0,8.
- КПД аккумуляторных
батарей БН, равный 0,8.