Материал: Буферные растворы
Буферные растворы
Содержание
Введение
Буферные смеси
Кислотно-основные буферные растворы
Классификация буферных систем
Свойства буферных растворов
Сущность буферного действия
Буферная емкость
Буферные свойства растворов сильных кислот и оснований
Применение буферных растворов в химическом анализе
Заключение
Библиографический список
Введение
БУФЕРНЫЕ РАСТВОРЫ (буферные смеси, буферы) - растворы, содержащие буферные системы и обладающие вследствие этого способностью поддерживать рН на постоянном уровне. Их обычно готовят путем растворения в воде взятых в соответствующих пропорциях слабой кислоты и ее соли, образованной щелочным металлом, частичной нейтрализацией слабой кислоты сильной щелочью или слабого основания сильной кислотой, растворением смеси солей многоосновной кислоты. Величина рН приготовленных таким образом буферных растворов незначительно меняется с температурой. Интервал значений рН, в котором буферный раствор обладает устойчивыми буферными свойствами, лежит в пределах рК ± 1 (рК - отрицательный десятичный логарифм константы диссоциации слабой кислоты, входящей в его состав). Наиболее известными буферными растворами являются: глициновый Серенсена, ацетатный Вальполя, фосфатный Серенсена, боратный Палича, вероналовый Михаэлиса, карбонатный Кольтгофа, трис-буфер, универсальный вероналовый Михаэлиса и др.
В лабораторной практике буферные растворы применяются для
сохранения активной реакции среды на определенном неизменном уровне и для
определения водородного показателя (рН) - в качестве стандартных растворов с
устойчивыми значениями рН и др.
Буферные смеси
Если к раствору какой-либо кислоты или щелочи прибавить воду, то, разумеется, концентрация ионов водорода или гидроксила соответственно уменьшается. Но если прибавить некоторое количество воды к смеси уксусной кислоты и ацетата натрия или к смеси гидроокиси аммония и хлорида аммония, то концентрация ионов водорода и гидроксила в этих растворах не изменится.
Свойства некоторых растворов сохранять неизменной концентрацию ионов водорода при разбавлении, а также при добавлении небольших количеств сильных кислот или щелочей известно под названием буферного действия.
Растворы, содержащие одновременно какую-либо слабую кислоту и ее соль или какое-либо слабое основание и его соль и оказывающие буферное действие, называют буферными растворами. Буферные растворы можно рассматривать как смеси электролитов, имеющих одноименные ионы. Присутствие в растворе слабой кислоты или слабого основания и их солей уменьшает влияние разбавления или действия других кислот и основании на рН раствора.
Такими буферными растворами являются следующие смеси СН3СООН+СН3СOONа, NH4OH + NH4Cl, Na2CO3 + NaHCO3 и др.
Буферный растворы, представляющие собой смеси слабых кислот и их солей, как правило имеют кислую реакцию (рН<7). Например, буферная смесь 0,1М раствора СН3СООР + 0,1М раствора СН3СОONa имеет рН = 4,7.
Буферные растворы, представляющие собой смеси слабых
основании и их солей, как правило, имеют щелочную реакцию (рН>7). Например,
буферная смесь 0,1М раствора NН4ОН + 0,1М раствора NН4С1 имеет рН
= 9,3.
Кислотно-основные буферные растворы
В широком смысле буферными называют системы, поддерживающие определенное значение какого-либо параметра при изменении состава. Буферные растворы могут быть
кислотно-основными - поддерживают постоянное значение рН при добавлении небольших количеств кислоты или основания.
окислительно-восстановительными - сохраняют постоянным потенциал системы при введении окислителей или восстановителей.
· известны металлобуферные растворы, которые поддерживают постоянное значение рН.
Во всех случаях буферный раствор представляет собой
сопряженную пару. В частности, кислотно-основные буферные растворы содержат
сопряженную кислотно-основную пару. Буферное действие этих растворов
обусловлено наличием кислотно-основного равновесия общего типа:
НА ↔ Н+ + А-
кислота сопряженное
основание
В + Н+ ↔ ВН+
основание сопряженная
кислота
Так как в данном разделе рассматриваются только кислотно-основные буферные растворы, будем называть их буферными, опуская в названии "кислотно-основные".
буферный раствор сильная кислота
Буферными растворами называют растворы, поддерживающие постоянное значение рН при разбавлении и добавлении небольших количеств кислоты или основания.
Классификация буферных систем
1. смеси растворов слабых кислот и их солей. Например, ацетатный буферный раствор.
. смеси растворов слабых оснований и их солей. Например, аммонийный буферный раствор.
. смеси растворов солей многоосновных кислот различной степени замещения. Например, фосфатный буферный раствор.
. ионы и молекулы амфолитов. К ним относятся, например, аминокислоты и белковые буферные системы. Находясь в изоэлектрическом состоянии, аминокислоты и белки не являются буферными. Буферное действие проявляется только тогда, когда к ним добавляется некоторое количество кислоты или щелочи.
При этом образуется смесь двух форм белка: а) слабая "белок кислота" + соль этой слабой кислоты; б) слабое "белок основание" + соль этого слабого основания. Таким образом, этот тип буферных систем можно отнести к буферным системам первого или второго типа.
Расчет рН буферных растворов
![]() В основе расчета рН буферных систем лежит закон действующих масс
для кислотно-основного равновесия.
В основе расчета рН буферных систем лежит закон действующих масс
для кислотно-основного равновесия.
Для буферной системы, состоящей из слабой кислоты и ее соли,
например, ацетатной, концентрацию ионов H+ легко
вычислить, исходя из константы равновесия уксусной кислоты:
CH3COOH ↔ CH3COO - + H+
![]() (1).
(1).
Из (1) следует, что концентрация ионов водорода равна
![]() (2)
(2)
В присутствии CH3COONa кислотно-основное равновесие уксусной кислоты сдвинуто влево. Поэтому концентрация недиссоциированной уксусной кислоты практически равна концентрации кислоты, т.е. [СН3COOH] = скисл.
Главный источник ацетат-ионов - сильный электролит CH3COONa:
CH3COONa → Na+ + CH3COO-,
Поэтому можно принять, что [CH3COO-] = ссоли. С учетом сделанных допущений уравнение (2)
принимает вид:
![]() .
.
Отсюда получают уравнение Гендерсона-Хассельбаха для буферных
систем, состоящих из слабой кислоты и ее соли:
![]() (3)
(3)
Для буферной системы, состоящей из слабого основания и его соли,
например, аммиачной, концентрацию ионов водорода в растворе можно рассчитать
исходя из константы диссоциации слабого основания.
NH3×H2O = NH4OH ↔ NH4+ + OH-
![]() (4)
(4)
Выразим концентрацию ионов OH - из
ионного произведения воды
![]() (5)
(5)
и подставим в (4).
![]()
![]() (6)
(6)
Из (6) следует, что концентрация ионов водорода равна
![]() (7)
(7)
В присутствии NH4Cl кислотно-основное равновесие сдвинуто влево. Поэтому концентрация недиссоциированного аммиака практически равна концентрации аммиака, т.е. [NH4OH] = сосн.
Главный источник катионов аммония - сильный электролит NH4Cl:
NH4Cl → NH4+ + Cl-,
Поэтому можно принять, что [NH4+] = ссоли. С учетом сделанных
допущений уравнение (7) принимает вид:
![]() (8)
(8)
Отсюда получают уравнение Гендерсона-Хассельбаха для буферных систем, состоящих из слабого основания и его соли:
Аналогичным образом можно рассчитать рН буферной системы,
состоящей из смеси растворов солей многоосновных кислот различной степени
замещения, например, фосфатной, состоящей из смеси растворов гидрофосфата (Na2HPO4)
и дигидрофосфата (NaH2PO4) натрия.
В основе ее действия лежит кислотно-основное равновесие:
H2PO4 - ↔ Н+ + HPO42-
слабая кислота сопряженное основание
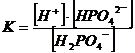 (10)
(10)
Выразив из (10) концентрацию ионов водорода и сделав следующие
допущения:
[H2PO4-] = c (H2PO4-); [HPO42-] = c (HPO42-), получим:
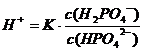 (11).
(11).
Прологарифмировав это выражение и поменяв знаки на
противоположные, получим уравнение Гендерсона-Хассельбаха для рассчета рН
фосфатной буферной системы
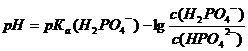 (12),
(12),
Где рКb (H2PO4-) - отрицательный десятичный логарифм константы диссоциации фосфорной кислоты по второй ступени; с (H2PO4-) и с (HPO42-) соответственно концентрации кислоты и соли.
Свойства буферных растворов
Значение рН буферных растворов остается неизменным при разбавлении, что следует из уравнения Гендерсона-Хассельбаха. При разбавлении буферного раствора водой концентрации обоих компонентов смеси уменьшаются в одинаковое число раз. Следовательно, величина рН при этом не должна изменяться. Однако опыт показывает, что некоторое изменение рН, хотя и незначительное, все же происходит. Это объясняется тем, что уравнение Гендерсона-Хассельбаха является приближенным и не учитывает межионных взаимодействий. При точных расчетах следует учитывать изменение коэффициентов активности сопряженных кислоты и основания.
Буферные растворы мало изменяют рН при добавлении небольших
количеств кислоты или основания. Способность буферных растворов поддерживать
постоянство рН при добавлении к ним небольших количеств сильной кислоты или
сильного основания, основана на том, что одна составная часть буферного
раствора может взаимодействовать с H+ прибавляемой кислоты, а другая
с OH - прибавляемого основания. Вследствие этого буферная система
может связывать как H+, так и OH - и до определенного предела сохранять постоянство
величины рН. Продемонстрируем это на примере формиатной буферной системы,
представляющей собой сопряженную кислотно-основную пару HCOOH/ HCOO-. Равновесие в растворе
формиатного буферного раствора можно представить уравнением:
HCOOH ↔ HCOO - + H+
При добавлении сильной кислоты сопряженное основание HCOO - связывает добавленные
ионы H+, превращаясь в слабую муравьиную кислоту:
HCOO - + H+ ↔ HCOOH
В соответствии с принципом Ле Шателье равновесие смещается влево.
При добавлении щелочи протоны муравьиной кислоты связывают
добавленные ионы ОН - в молекулы воды:
HCOOH + ОН - → HCOO - + H2O
Кислотно-основное равновесие согласно Ле Шателье смещается вправо.
В обоих случаях происходят небольшие изменения в соотношении HCOOH/ HCOO-, но логарифм этого соотношения меняется мало. Следовательно, незначительно меняется и рН раствора.
Сущность буферного действия
Действие буферных растворов основано на
том, что отдельные компоненты буферных смесей связывают ионы водорода или
гидроксила вводимых в них кислот и основании с образованием слабых
электролитов. Например, если к буферному раствору, содержащему слабую кислоту
НАn и соль этой кислоты KtАn, прибавить щелочь, то
произойдет реакция образования слабого электролита-воды:
Н+ + ОН → Н2О
Следовательно, если к буферному раствору, содержащему кислоту, прибавить щелочь, то ионы водорода, образующиеся при электролитической диссоциации кислоты НАn, связываются с ионами гидроксила прибавленной щелочи, образуя слабый электролит-воду. Вместо израсходованных ионов водорода, вследствие последующей диссоциации кислоты НАn, появляются новые ионы водорода. В результате прежняя концентрация Н+ - ионов в буферном растворе восстановятся до первоначального значения.
Если к указанной буферной смеси прибавить сильную
кислоту, то произойдет реакция:
Н+ + Аn - → НАn
т.е. Аn - ионы, образующиеся при электролитической диссоциации соли КtАn, соединяясь с ионами водорода прибавленной кислоты, образуют молекулы слабой кислоты. Поэтому концентрация ионов водорода от прибавленной сильной кислоты к буферной смеси практически не изменится. Подобным же образом можно объяснить действие других буферных смесей.
Значение рН в буферных растворах
Меняя соотношения и можно получить буферные
растворы, отличающиеся плавным изменением
рН от них минимально возможных значений. В водном растворе слабой кислоты
[Н+] = √KHAn * CHAn
откуда
pH = − lg [Н+] = −
− lg KHAn− − lg CHAn
Но так как KHAn представляет собой
постоянную величину, то ее лучшее представить в виде pKHAn т.е. показателя
константы электролитической диссоциации:
pKHan = − lg KHAn.
Тогда получим, что в водном растворе
слабой кислоты:
рН = − lg [Н+] = −
− pKHAn − − pCHAn
По мере прибавления к водному раствору слабой кислоты ее соли рН раствора будет меняться.
Согласно уравнению, в растворе, содержащем
смесь слабой кислоты и ее соли [Н+] = KHan то
рН = − lg [Н+] = −
lg KHAn − lg CHAn + lg CKtАn.
Аналогично выводим формулу применительно к
слабым основаниям:
[ОН] = √KKtOH * CKtOH
pOH = − lg [ОН] = − − lg KKtOH − − lg CKtOH
Концентрацию ионов водорода также выражают
следующей формулой [Н+] =, поэтому
рН = pKw − (− pKKtOH − − lg CKtOH)
Согласно уравнению, в растворе, содержащем
смесь слабого основания и его соли
[Н+] = т.е. рН = − lg [Н+] = −
lg Kw + lg KKtOH − lgCKtАn + lg CKtOH.
Нет никакой необходимости запоминать выведенные формулу значении рН, так как они очень легко выводятся путем логарифмирования простых формул, выражающих значение [Н+].
Буферная емкость
Способность буферных растворов поддерживать постоянство значения рН небезгранична и зависит от качественного состава буферного раствора и концентрации его компонентов. При добавлении к буферному раствору значительных количеств сильной кислоты или щелочи наблюдается заметное изменение рН. причем для различных буферных смесей, отличающихся друг от друга по составу, отличающихся друг от друга по составу, буферное действие неодинаково. Следовательно, буферные смеси можно различать по силе оказываемого ими сопротивления по отношению к действию кислот и щелочей, вводимых в буферный раствор в одинаковых количествах и определенной концентрации. Предельное количество кислоты или щелочи определенной концентрации (в моль/л или г-экв/л), которое можно добавить к буферному раствору, чтобы значение рН его изменилось только на одну единицу, называют буферной емкостью.