Материал: Биологическая активность кремнийорганических соединений
M=Si
C6H5(CH3)2SiOH
C6H5MH(CH3)2+
CH3 CH3
M=C
C6H5(CH3)2COH
+C6H5CHCH2O-G+C6H5CHCOOH
Триметилфенилсилан в организме крыс окисляется
как в метильной, так и в фенильной группах. В противоположность этому в
трет-бутилбензоле окисляется только метильная группа:
M=Si C6H5(CH3)2SiCH2OH(31%)+
+HOC6H4Si(CH3)3(17%)+
C6H5M(CH3)3 +C6H5(CH3)2SiCH2O-X
M=C
C6H5(CH3)2CCH2O-G
(глюкуронид)
90%
3. ДЕЙСТВИЕ КРЕМНИЙОРГАНИЧЕСКИХ СОЕДИНЕНИЙ НА
ЖИВЫЕ ОРГАНИЗМЫ И ИХ АКТИВНОСТЬ
.1 Инсектицидное
действие
Инсектицидное действие некоторых неорганических соединений кремния (кремнефторидов щелочных и щелочноземельных металлов или цинка) известно уже давно. Указанные соли кремнефтористоводородной кислоты нашли применение для борьбы с вредителями зерновых, бобовых, овощных и цитрусовых культур, клевера, люцерны, сахарной свеклы, хлопчатника, а также с комарами, молью и мухами. Упоминалась уже и инсектицидная способность силикагеля.
Сравнительно недавно обнаружена инсектицидная активность кремнийсодержащих карбаматов (CH3)3SiC6H4OCONHCH3 и сульфамидов (C2H5О)3Si (CH2)3NHSO2R триалкилсилиловых эфиров фосфоновых кислот R3SiOSiR2CH2P(О)•(ОС2Н5)2, (CH3О)2P(О)CH(CCIО3)ОSiR3 (акарициды), медных солей кремнийсодержащих дитиокарбаминовых кислот R3Si(CH2)nNHCSSH и медьсодержащих полиорганилсилоксанов, бис(триметилсилил) диацетилена (CH3)3SiC=CC=CSiCH3)3, N-триметилсилилпирролидона-2 (CH3)3SiN (СН2)3СО, циклических кремнийорганических производных непредельных диолов R2SiOCH2CH = CHCH2O (паразитиниды), кремнийорганических аналогов ДДТ (p-CIC6H4)3SiCI3, (p-CIC6H4)4Si(CH3)CH2CI. (p-CIC6H4)4Si, изотиоцианатосиланов R4-nSi(NCS)n. органилфторсиланов RnSiF4-n, фторалкоксисиланов (CF3)2CCIOSiHCI2, циклосилтианов (R2SiS)n галогеналкилтрисилиламинов (BrCH2SiR2)2NSiR3 аминоалкилтриэтоксисиланов, триалкил(3-пиперидинопропил) сплавов, триалкил (триалкилсилокси) станнанов R3SiOSnR3, а также мелкодиспергированного полисилоксанового масла.
При этом установлено, что исследованные кремнийорганические аналоги ДДТ значительно менее активны, чем данный инсектицид. м-Триметилсилилфенил (N-метил) карбамат в 1,75 раза менее эффективно ингибирует холинэстеразу комнатной мухи (Musca domestica L.), чем изостерный ему м-трет-бутилфенил (N-метил) карбамат. Тем не менее его ингибирующая активность все же в 285 раз выше, чем несилилированного фенил (N-метил) карбамата. Сравнение инсектицидного действия о-, м и n-триметилсилилзамещенных фенил (N-метил) карбаматов показывает, что по отношению к москитам Culex pipiens quinquefasciatus Say наибольшей инсектицидной активностью обладает о-изомер. В то же время о-изомер наиболее токсичен для комнатной мухи [7].
Значительным фумигационным действием обладает диметил- диизотиоцианатосилан. 6-15-часовая экспозиция в атмосфере со сравнительно невысокой концентрацией паров (CH3)2Si(NCS)2 приводит к 100%-ной гибели сельскохозяйственного вредителя клопа-черепашки Eurygaster integriceps Put.
Гидрохлорид триэтилпиперидинометилсилана в концентрации 0,06% вызывает уменьшение плодовитости зерно4вой моли Sitotroga cerealella Oliv. на 84%. Несколько меньшим хемостерилизирующим эффектом по отношению к зерновой моли обладают 1-хлор-3-триметилсилилпропин-2 и метилдиэтил (3-хлорпропил) силан. Трибутил(3-аминопропил) силан в концентрациях 0,5-2% обеспечивает полное бесплодие фасолевой зерновки Acantlioscelides obtectus.
Интересно отметить, что добавление 0,1-2%
полисилоксана к пище шелкопряда увеличивает массу их гусениц (8-10%) и коконов
(15-18%).
.2 Инсекторепеллентное
действие
В качестве средств для отпугивания кровососущих членистоногих (инсекторепеллентов) предложены N-этил-N-триалкилсилилметиламиды уксусной кислоты RR/2SiCH2N(C2H5)COCH3. Ткань, обработанная спиртовым раствором этих соединений, при дозе 40 г/м2 сохраняет репеллентные свойства более 14 сут (при R = C3H7 или С4Н9). Продолжительность отпугивающего действия соединений с R'=CH3 и С2Н5 значительно меньше (соответственно 2 и 6 сут).
Ипсекторепеллентным действием по отношению к
Aedes aegypti обладают производные 1,3,5,7-тетрасилаадамантана I и
2-окса-1,3,5,7-тетрасилаадамантана II. Хорошими отпугивающими свойствами
обладает также циклический кремнийорганический эфир инсекторепеллента
2-этил-1,3-гександиола III.
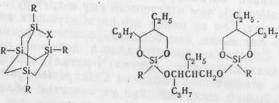 , II, III
I Х = СН2; II Х = 0
, II, III
I Х = СН2; II Х = 0
Циклические эфиры 2-этил- 1,3-гександиола и метилсилантриола, в которых атом кремния связан также с м-оксифеноксигруппой, инсекторепеллентной активностью не обладают. При их гидролизе отщепляется не 2-этил-1,3-гександиол, а резорцин, что приводит к образованию силанола, который также неактивен.
Исследование инсекторепеллентного действия серии амино- алкоксисиланов и кремнийорганических аминоспиртов по отношению к инсектарной культуре блох X. cheopis показало, что силилирование повышает активность и продолжительность отпугивающего действия аминоспиртов. Наилучшими инсекторепеллентными свойствами обладают диорганилбис(2-дибутиламиноэтокси) силаны (коэффициентотпугивающего действия при дозе 20 г/м2 составляет 94-98%, продолжительность действия до 22 сут). Ипсекторепеллентная активность и продолжительность действия диметил (дибутиламинометил) силанов (C4H9)2NCH2Si(CH3)2OR мало зависят от характера заместителя R (2-дибутиламиноэтил, этил, ацетил) и при дозе 20 г/м2 составляет 92-98% в течение 12 сут.
Активность кремнийорганических спиртов R3SiCH2NR'CH2•СН2ОН
(97-99%) выше, чем у соответствующих аминов R3SiCH2NHR',
однако продолжительность их действия небольшая (2-5 сут). Инсекторепеллентная
активность и продолжительность действия кремнийорганических аминов зависят от
природы органических радикалов, связанных с атомом азота.
R2NCH2Si (ОС2Н5)3 (C4H9)2NCH2Si (OR)3 [R2Si(CH2)nNR/2]2O.
IV
V VI
В ряду (органиламинометил) триэтоксисиланов (IV) инсекторепеллентная активность соединений в зависимости от природы радикалов, связанных с атомом азота, уменьшается в следующем порядке:(C4H9)2N> (СН3)2N> (C5H11)2N> СН2=CHCH2NH > C4H9NH > 2-фурфуриламино> C6H5NH > (i-C5H11)2N>пергидроазепино > (i-C4H9)2N> (С3Н7)2N>пиперидино>морфолино> (C2H5)2N.
При этом последние четыре соединения слабо отпугивают насекомых и не представляют интереса как репелленты. Первые же два соединения ряда (дибутиламино и диметиламино) обладают высоким коэффициентом отпугивающего действия (KOD при дозе 20 г/м2 выше 90%).
Наибольшая продолжительность репеллентного действия среди аминов IV наблюдается также у дибутилпроизводного. В связи с этим была изучена зависимость инсекторепеллентных свойств дибутиламинопроизводных V от природы радикалов, связанных с атомом кремния. Установлено, что активность и устойчивость отпугивающего действия (дибутиламино) триалкоксисиланов (V) в зависимости от природы алкоксигруппы уменьшаются в следующем ряду: С2Н5> СН3 O > С3Н7 O > С4Н9O.
Замена одной этоксигруппы в (дибутиламинометил) триэтоксисилане пропокси- или бутоксигруппой повышает активность соединения, но резко снижает продолжительность отпугивающего действия. Введение вместо этоксильных триметилсилокси- или метальной группы повышает активность соединения [в случае диметил (дибутиламинометил) этоксисилана KOD достигает 100%]. Однако продолжительность инсекторепеллентного действия, как и в случае соответствующего триалкилпроизводного, опять-таки уменьшается [8].
Активность кремнийорганических аминов значительно повышается при переходе к дисилоксанам (VI). В случае 1,3-бис (пиперидинометил) -,1,3-бис (у-аминопропил) -, 1,3-бис (у-дибутиламипопропил) - и, особенно, 1,3-бис(у-диэтиламинопропил) тетраметилдисилоксана инсекторепеллентная активность и продолжительность действия были наибольшими (97-98%-ная активность в течение 75 сут при дозе 20 г/м2). Это значительно превышает данные для известного эталонного инсекторепеллента ДЭТА (ж-диэтилтолуамид), высокая активность которого (95-100%) сохраняется в течение 20 сут.
Наличие алкоксигрупп у атома кремния в соединениях IV, V позволяет применять их для обработки тканей, которую можно сочетать с отделкой кремнийорганическими гидрофобизаторами [8].
Следует также отметить, что полиорганосилоксаны
могут быть использованы в качестве носителей обычных инсекторепеллентов.
.3 Фунгистатическая
активность
Ряд кремнийорганических соединений обладает определенной фунгистатической активностью. К ним относятся кремнийсодержащие амиды карбоновых кислот, сульфамиды (C2H5O)3Si(CH2)3NHSO2R, тиолы (R2SiCH2SH)2O и изотиоцианаты R3SiCH2SCN, циклосилтианы, органилфторсиланы R4-nSiFn , фенилэтинил- и бутилэтинилсиланы R3SiC=CR', кремнийорганические ацетиленовые кетоны R3Si(Cs=C)nCOR' и амины R3SiC=CCH2NR'2 изотиоцианатосиланы R4-nSi(NCS)n, пентахлорфеноксисиланы и силоксаны (C6CI5O)nSi(OR)4-n, (C6CI5O)3•SiOSi(ОС6СI5)3, соли кремнийорганических дитиокарбаминовых кислот [(RO)3Si•(CH2)nNHCSS]nM, медь, ртуть, олово, титан, фосфор и мышьяксодержащие органилсиланы, силоксаны и силикаты, (триорганилсилокси)титанатраны, 2-(n-триметилсилр метилфенил) этиламин, 1-имидазолилметилсиланы бензимидазолилалкилсиланы, 4-хинолилампнопропилланы, сульфоны 2-хлор-3-бензотиениламинопропилланов и 3-аминопропилсиланы.
Добавление к питательной среде, зараженной культурами плесени Macrosporium, Cladosporium, 0,3-1,0%-ной C4H9Si•(NCS)3, (CH3)2Si(NCS)2, (C2H5)2Si(NCS)2 или (C2H5)3SiNCS вызывает значительное подавление или даже полное прекращение ее развития на срок до одного года, а также способствует предотвращению поселения на этой среде плесени и бактерии из окружающего воздуха. Никакой зависимости между строением (в частности, числом групп NCS в молекуле) и фунгистатическим действием изотиоцианатосиланов не наблюдается. Фунгистатическое действие органилизотиоцианатосиланов не может быть обусловлено лишь токсичностью, образовавшейся при их гидролизе роданистоводородной кислоты, ибо наиболее легко гидролизующиеся метилтриизотиоцианатосилан и этилтриизотио цианатосилан наименее эффективны. В то же время и наибольее трудно гидролизующиеся трибутилизотиоцианатосилан и дибутилдиизотиоцианатосилан оказываются нетоксичными. По своей фунгицидной активности алкилизотиоцианатосиланы значительно уступают своим органическим аналогам, например, CH2(SCN)2. Алкилизоцианатосиланы R4-nSi(NCO) сходные по строению с изотиоцианатосиланами, фунгицидным действием вообще не обладают.
Изотиоцианатосиланы проявляют заметную фунгицидную активность и в паровой фазе. Так, диметилдиизотиоцианатосилан и диэтилдиизотиоцианато силан уже при концентрации в воздухе 0,2 г/л подавляют рост плесеней Cladosporium, Macrosporium и Tor Lila.
Фунгистатическая активность первичных, вторичных и третичных алифатических и гетероциклических аминов RR'2Si (CH2)nNR"R"' зависит от расстояния между атомами кремния и азота и является наибольшей в случае у-производных (п=3). Наиболее отчетливо это выражено у метилдибутилсилилпроизводных. В случае производных пиперидина, например, минимальная концентрация соединения, подавляющая рост Candida albicans 67/846, увеличивается от
мкг/мл при n=3 до 133 мкг/мл при n=2, а при n=1 никакого эффекта не наблюдается даже при концентрации 400 мкг/мл. Аналогичная картина имеет место при сравнении активности производных пирролидина, которые при n=3 в 10 раз активнее, чем при п=4 [8].
Метилдибутил(3-аминопропил) силан является наиболее сильным фунгистатиком в ряду аминов CH3R2Si(СН2)3NН2, активность которых в зависимости от природы заместителя R уменьшается в следующем порядке:
H9>C6H13>
>С3Н7>С3Н15>С7Н5>С2Н5>С8Н19>СН3
Метилдибутилпроизводное оказывается наиболее активным также в рядах производных диэтиламина, бутиламина, пирролидина, пиперидина и 2-фурфуриламина. Разветвление в бутильной группе приводит к понижению, активности, поэтому соответствующие метилдиизобутилпроизводные проявляют меньшую фунгистатическую активность.
В аналогичном ряду C2H5R2Si(СН2)3NН2
фунгистатическая активность уменьшается ' в другой последовательности
С3Н7>С5Н11> С4Н9> С2Н5
Среди соединений ряда R(C2H5)2Si(CH2)3NH2
наиболее активно диэтиламилпроизводноe
С5Н11>С4Н9>С3Н7>С2Н5>СН3
Фунгистатическая активность триалкил (3-аминопропил) силанов R3Si (СН2)3NН2, содержащих у атома кремния три одинаковых неразветвленных алкильных радикала, в зависимости от природы заместителя R уменьшается в ряду
H9> С3Н7> С5Н11 > С6Н13>С2Н5>СН3
В рядах соединений (СН3)3-n(C4H9)nSi(CH2)3N(С2Н5)2 и (C2H3)3-n(C2H5)nSi(CH2)3N(C2H5)2 с увеличением п (от 1 до 3 в первом случае и от 0 до 2 во втором) фунгистатическая активность по отношению к эпидермофитону и трихофитону увеличивается.
Фунгистатическая активность вторичных аминов ниже активности первичных аминов, но значительно превышает активность третичных аминов. Лишь метилдибутил (3-бутиламино-пропил) силан подавляет рост кандид несколько сильнее, чем метилдибутил (3-аминопропил) силан.
Фунгистатическая активность третичных аминов
CH3(C4H9)2Si(CH2)3NR2 в зависимости от строения органических радикалов,
связанных с атомом азота, уменьшается в следующем порядке:
(СН2)5> С2Н5> СН3> (СН2)4>
(СН2)6> (СН2)2О(СН2)2> С4Н9>
С3Н7. Однако производные дипропиламина и
пергидроазепина сильнее действуют на Trichophyton
gypseum 4/3, поэтому по
отношению к этому грибу ряд активности принимает следующий вид
С3Н7> (СН2)6>, С2Н5> СН3> (СН2)5>
(СН2)4> (СН2)2O(СН2)2>
С4Н9
Анализ полученных данных показывает, что из исследованных грибов наиболее устойчив к действию кремнийорганических аминов Candida albicans 67/846. Лучшими фунгистатиками по отношению к этому грибу являются метилдигексил (3-диэтпламинопропил) силан (6,7 мкг/мл), диэтиламил (3-аминопропил) силан (7,8 мкг/мл), метилдибутил (З-бутиламинопропил) силан (10,4 мкг/мл) и трибутил (3-амииопропил) силан (15,6 мкг/мл). Однако их активность не достигает активности антибиотика нистатина (3,5 мкг/мл) и 2-(ω-нитровинил) 5-нитрофурана (4,9 мкг/мл).
Ряд кремнийорганических аминов весьма эффективно подавляет рост Epidermophyton Kaufmann-Wolf 41. К ним относятся метилдибутил (3-аминопропил) силан (4,2 мкг/мл), метилдибутил [у-(2-фурфуриламино) пропил]силан (4,2 мкг/мл), 2-хлор-3-[у-(триэтоксисилил) пропиламино] бензо[в]тиофен-1,1-диоксид (4,2 мкг/мл), метилдибутил(3-бутиламинопропил) силан (5,2 мкг/мл). Их активность выше, чем нистатина (6,9 мкг/мл), и приближается к активности гризеофульвипа (2,6 мкг/мл).
Кремнийорганические амины эффективно подавляют рост Trichophyton gypseum 4/3. Сильнее нистатина (7,8 мкг/мл) действуют триэтил[у-(2-диэтиламиноэтилтио) пропил] силан (3,9 мкг/мл), 2-хлор-3-[у-(триэтокснсилил)пропиламино] бензо [в]тиофен-1,1-диоксид (4,2 мкг/мл) и трибутил (3-аминопропил) силан. Активность на уровне нистатина проявляют диэтиламил (3-аминопропил) силан (7,8 мкг/мл), метилдибутил (3-аминопропил) силан (8,3 мкг/мл) и этилдипропил (3-аминопропил) силан (8,3 мкг/мл) [8].
Фунгистатическая активность аминоалкилсиланов не коррелирует с их основностью и, по-видимому, в большей мере определяется их пространственной структурой. Об этом свидетельствуют большая активность узминов, понижение активности при замене n-бутильных групп у атома кремния изобутильными, меньшая активность третичных аминов и кремнийорганических ацетиленовых у аминов. Вместе с тем следует отметить, что активность соединений зависела от суммарного количества углеродных атомов, связанных с атомом кремния. Максимум активности наблюдался при С9 (метилдибутил-, диэтиламил-, трипропил) и С12 (трибутил-, этилдиамил-), а затем при С8 (этилдипропил). Аналогичные зависимости (вероятность активных соединений 75-85%) получены при кибернетическом анализе в режиме активного диалога исследователя с ЭВМ взаимосвязи структуры с фунгистатической активностью кремнийорганических аминов.