Материал: биохимия . гормоны - 2 часть
Липотропные гормоны (лтг, липотропины).
Среди гормонов передней доли гипофиза следует отметить липотропины, в частности β- и γ-ЛТГ. К биологическим свойствам β-липотропина относятся жиромобилизующее действие, кортикотропная, меланоцитстимулирующая и гипокальциемическая активность и инсулиноподобный эффект выражающийся в повышении скорости утилизации глюкозы в тканях. Липотропный эффект осуществляется через систему аденилатциклаза–цАМФ–протеинкиназа, завершающей стадией действия которой является фосфорилирование неактивной триацилглицерол-липазы. Этот фермент после активирования расщепляет нейтральные жиры на диацилглицерол и высшую жирную кислоту.
Перечисленные биологические свойства обусловлены не β-липотропином, оказавшимся лишенным гормональной активности, а продуктами его распада, образующимися при ограниченном протеолизе. Оказалось, что в ткани мозга и в промежуточной доле гипофиза синтезируются биологически активные пептиды, наделенные опиатоподобным действием. Приводим структуры некоторых из них:
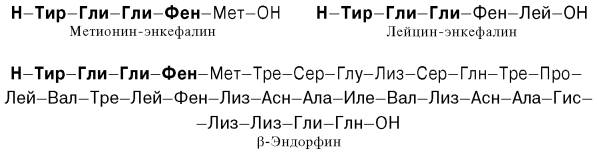
Общим типом структуры для всех трех соединений является тетрапептидная последовательность на N-конце.
β-эндорфин (31 АМК) образуется путем протеолиза из более крупного гипофизарного гормона β-липотропина (91 АМК); последний вместе с АКТГ образуется из общего предшественника – прогормона, названного проопиокортином, насчитывающим 134 аминокислотных остатка. Биосинтез и освобождение проопиокортина в передней доле гипофиза регулируется кортиколиберином гипоталамуса. В свою очередь из АКТГ и β-липотропина путем дальнейшего процессинга, в частности ограниченного протеолиза, образуются соответственно α- и β-меланоцитстимулирующие гормоны (α- и β-МСГ
Гормоны паращитовидных желёз
В паращитовидных железах образуется паратиреоидный гормон (паратгормон) и кальцитонин. Однако основное количество кальцитонина вырабатывается в щитовидной железе.
Паратгормон – это гормон белковой природы, который повышает содержание кальция (Са2+) и снижает концентрацию фосфата (Р) в крови. Действие паратгормона направлено на следующие ткани-мишени:
кости – гормон увеличивает выход Са2+ и Р из кости в кровь; тормозит синтез коллагена в остеобластах, увеличивает разрушение минеральной и органической части кости остеокластами и остеоцитами;
кишечник – увеличивает всасывание Са2+ и Р из кишечника в кровь;
почки – увеличивает реабсорбцию Са2+ из мочи в кровь, но увеличивает выведение Р с мочой.
Патология
Гиперпаратиреоз – повышенное образование паратгормона, возникающее при опухоли паращитовидных желёз. Так как Са2+ усиленно выходит из кости, то наблюдаются самопроизвольные переломы вследствие рассасывания костной ткани. Повышение концентрации Са2+ в крови приводит:
а) к окостенению внутренних органов, обызвествлению ушибов, кровоподтёков;
б) к понижению нервно-мышечной возбудимости, что проявляется как атрофия и слабость мышц, а также депрессией, нарушением памяти и внимания.
Избыток паратгормона резко увеличивает секрецию гастрина, что, в свою очередь, приводит к повышению секреции HCl и пепсина в желудке, поэтому при избытке паратгормона могут развиться язвы желудка.
Гипопаратиреоз – может наблюдаться после операций на щитовидной железе, когда по ошибке были удалены и паращитовидные железы, либо возникает у детей при инфекциях дыхательных путей. Такое состояние сопровождается снижением концентрации Са2+ в крови, что приводит к повышению нервно- мышечной возбудимости. У взрослых наблюдаются конвульсии, судороги, что характеризуется как тетания. У детей может возникнуть спазмофилия, т.е. состояние, когда ребенок во время плача внезапно синеет из-за спазма дыхательных мышц.
Кальцитонин – понижает концентрацию и Са2+, и Р в крови. Оказывает влияние на те же ткани-мишени, что и паратгормон, однако действие кальцитонина, в основном, противоположно эффектам паратгормона. Однако, как и паратгормон, кальцитонин увеличивает выведение Р с мочой.
Гормоны щитовидной железы
В щитовидной железе синтезируются тиреоидные гормоны – тироксин (Т4) и трииодтиронин (Т3). Для синтеза этих гормонов необходим иод, который активно захватывается из крови клетками фолликулов щитовидной железы. Тироксин и трииодтиронин являются производными аминокислоты тирозина. Тироксин содержит в своей молекуле 4 атома иода, в состав трииодтиронина входит 3 атома иода.
 В
клетках эпителия фолликулов щитовидной
железы находится белок тиреоглобулин.
Это гликопротеин, содержащий много
остатков аминокислоты тирозина (около
3 % от массы белка). Синтез тиреоидных
гормонов идет из тирозина и атомов иода
именно в составе молекулы тиреоглобулина
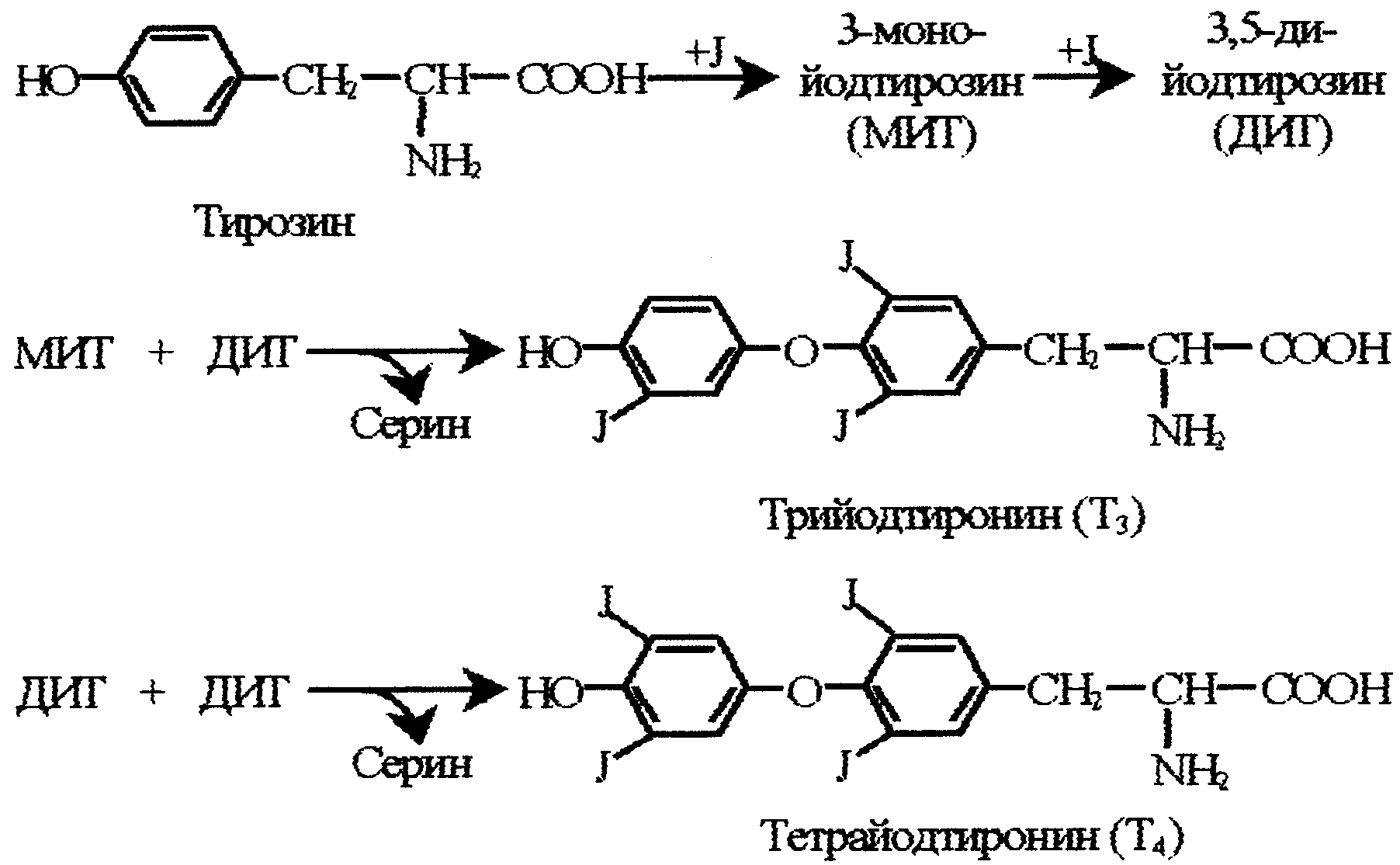
и включает 2 стадии. На апикальных
мембранах клеток фолликулов сначала
происходит иодирование тирозина с
образованием моноиодтирозина (МИТ) и
дииодтирозина (ДИТ). Следующим этапом
является конденсация МИТ и ДИТ с
образованием Т3
и Т4
(рис. 7).
В
клетках эпителия фолликулов щитовидной
железы находится белок тиреоглобулин.
Это гликопротеин, содержащий много
остатков аминокислоты тирозина (около
3 % от массы белка). Синтез тиреоидных
гормонов идет из тирозина и атомов иода
именно в составе молекулы тиреоглобулина
и включает 2 стадии. На апикальных
мембранах клеток фолликулов сначала
происходит иодирование тирозина с
образованием моноиодтирозина (МИТ) и
дииодтирозина (ДИТ). Следующим этапом
является конденсация МИТ и ДИТ с
образованием Т3
и Т4
(рис. 7).
Рис. 7. Схема синтеза тиреоидных гормонов
Такая иодированная молекула тиреоглобулина секретируется в просвет фолликула, в коллоид. Когда в щитовидную железу приходит сигнал в виде ТТГ (тиреотропного гормона), клетки фолликула захватывают капельки коллоида вместе с тиреоглобулином, ферменты лизосом протеазы гидролизуют белок до аминокислот, и готовые Т3 и Т4 поступают в кровь.
В крови тиреоидные гормоны связываются с белком- переносчиком и в таком виде транспортируются в ткани-мишени. Концентрация Т4 в крови в 10 раз больше, чем Т3, поэтому Т4 называют главной формой тиреоидных гормонов в крови. Но Т3 в 10 раз активнее, чем Т4.
Ткани-мишени для тиреоидных гормонов – это все ткани, кроме селезёнки и семенников.
В тканях-мишенях тиреоидные гормоны освобождаются от белка и поступают в клетку. В клетках 90 % Т4 теряет 1 атом иода и превращается в Т3. Таким образом, главной внутриклеточной формой гормона является Т3.
Действие тиреоидных гормонов на организм зависит от концентрации этих гормонов в крови: в физиологических дозах они оказывают анаболическое действие, в больших дозах – катаболическое.
При гипертиреозе (тиреотоксикоз, или Базедова болезнь) в организме образуется избыточное количество тироксина. Большие концентрации гормона действуют на митохондрии, которые являются «энергетическими станциями» клетки. В митохондриях находится ЦТД, т.е. цепь переносчиков, которая окисляет субстраты при помощи кислорода и в которой образуется энергия. В норме часть этой энергии запасается в виде АТФ, а часть идет на образование тепла для поддержания нормальной температуры тела. Поэтому одним из характерных признаков гипертиреоза является повышение температуры тела. Поскольку образование АТФ при этом заболевании снижается, то наблюдается сильная слабость, так как АТФ необходим для мышечного сокращения и поддержания тонуса мускулатуры. Дефицит АТФ в организме приводит к усиленному распаду белков, углеводов и жиров тела (катаболическое действие больших концентраций тироксина), что сопровождается резким общим похуданием.
Кроме перечисленных симптомов, при гипертиреозе наблюдаются: увеличение щитовидной железы (зоб), пучеглазие (экзофтальм), увеличение частоты сердечных сокращений (тахикардия), возбужденность, беспокойство, нервозность, плаксивость, бессонница, эмоциональная лабильность, потливость, кожа становится влажной и горячей.
Гипофункция щитовидной железы (гипотиреоз) у взрослых называется микседема. Развиваются слизеподобный отек тканей, ожирение, выпадение волос и зубов, апатия, сонливость, психическая инертность, снижение интереса и инициативы, гиперхолестеринемия, жировое перерождение печени, речь становится медленной и невнятной, мимика невыразительной, кожа - сухая, бледная и холодная, снижается температура тела.
Гипофункция щитовидной железы (гипотиреоз) у детей называется кретинизм (см. выше).
Особой формой гипотиреоза является эндемический зоб. Он возникает при недостаточном содержании йода в воде и пище. Компенсаторно разрастается ткань щитовидной железы, но при отсутствии иода это не приводит к увеличению выработки тиреоидных гормонов.
Гормоны поджелудочной железы.
Поджелудочная железа относится к железам со смешанной секрецией.
Внешнесекреторная функция ее заключается в синтезе ряда ключевых ферментов пищеварения, в частности амилазы, липазы, трипсина, химотрипсина, карбоксипептидазы и др., поступающих в кишечник с соком поджелудочной железы.
Внутрисекреторную функцию выполняют, как было установлено в 1902 г. Л.В. Соболевым, панкреатические островки (островки Лангерганса), состоящие из клеток разного типа и вырабатывающие гормоны противоположного действия. Так, α- (или А-) клетки продуцируют глюкагон, β- (или В-) клетки синтезируют инсулин, δ-(или D-) клетки вырабатывают соматостатин и F-клетки – малоизученный панкреатический полипептид.
Инсулин получивший свое название от наименования панкреатических островков (лат. insula – островок), был первым белком, первичная структура которого была раскрыта в 1954 г. Ф. Сэнджером. В чистом виде инсулин был получен в 1922 г. после его обнаружения в экстрактах панкреатических островков Ф. Бантингом и Ч. Бестом. Молекула инсулина, содержащая 51 аминокислотный остаток, состоит из двух полипептидных цепей, соединенных между собой в двух точках дисульфидными мостиками. В настоящее время принято обозначать цепью А инсулина 21-членный пептид и цепью В – пептид, содержащий 30 остатков аминокислот. Во многих лабораториях осуществлен химический синтез инсулина. Наиболее близким по своей структуре к инсулину человека является инсулин свиньи, у которого в цепи В вместо треонина в положении 30 содержится аланин. Существенных различий в аминокислотной последовательности в инсулине от разных животных нет. Инсулины различаются аминокислотным составом цепи А в положениях 8–10.
Биосинтез инсулина осуществляется в β-клетках панкреатических островков из своего предшественника проинсулина. Уже не только выяснена первичная структура проинсулина, но и осуществлен его химический синтез. Проинсулин представлен одной полипептидной цепью, содержащей 84 аминокислотных остатка; он лишен биологической, то есть гормональной, активности. Местом синтеза проинсулина считается фракция микросом β-клеток панкреатических островков; превращение неактивного проинсулина в активный инсулин (наиболее существенная часть синтеза) происходит при перемещении проинсулина от рибосом к секреторным гранулам путем частичного протеолиза (отщепление с С-конца полипептидной цепи пептида, содержащего 33 аминокислотных остатка и получившего наименование соединяющего пептида, или С-пептида). Длина и первичная структура С-пептида подвержена большим изменениям у разных видов животных, чем последовательность цепей А и В инсулина.
Исходным предшественником инсулина является препроинсулин, содержащий, помимо проинсулина, его так называемую лидерную, или сигнальную, последовательность на N-конце, состоящую из 23 остатков аминокислот; при образовании молекулы проинсулина этот сигнальный пептид отщепляется специальной пептидазой. Далее молекула проинсулина также подвергается частичному протеолизу, и под действием трипсиноподобной протеиназы отщепляются по две основные аминокислоты с N- и С-конца пептида С – соответственно дипептиды Aрг–Aрг и Лиз–Aрг.
Синтезированный из проинсулина инсулин может существовать в нескольких формах, различающихся по биологическим, иммунологическим и физико-химическим свойствам.
Различают две формы инсулина:
свободную, вступающую во взаимодействие с антителами, полученными к кристаллическому инсулину, и стимулирующую усвоение глюкозы мышечной и жировой тканями;
связанную, не реагирующую с антителами и активную только в отношении жировой ткани. Существование связанной формы инсулина доказано и установлена локализация ее в белковых фракциях сыворотки крови, в частности в области трансферринов и α-глобулинов.
Различают, кроме того, так называемую форму А инсулина, отличающуюся от двух предыдущих рядом физико-химических и биологических свойств, занимающую промежуточное положение и появляющуюся в ответ на быструю, срочную потребность организма в инсулине.
В физиологической регуляции синтеза инсулина доминирующую роль играет концентрация глюкозы в крови. Так, повышение содержания глюкозы в крови вызывает увеличение секреции инсулина в панкреатических островках, а снижение ее содержания, наоборот,– замедление секреции инсулина. Этот феномен контроля по типу обратной связи рассматривается как один из важнейших механизмов регуляции содержания глюкозы в крови. На секрецию инсулина оказывают влияние электролиты (особенно ионы кальция), аминокислоты, глюкогон и секретин.
Глюкоза действует в качестве сигнала для активирования аденилат-циклазы, а образовавшийся в этой системе цАМФ – в качестве сигнала для секреции инсулина.
При недостаточной секреции (точнее, недостаточном синтезе) инсулина развивается специфическое заболевание – сахарный диабет. Помимо клинически выявляемых симптомов (полиурия, полидипсия и полифагия), сахарный диабет характеризуется рядом специфических нарушений процессов обмена. Так, у больных развиваются гипергликемия (увеличение уровня глюкозы в крови) и гликозурия (выделение глюкозы с мочой, в которой в норме она отсутствует).
Клинические симптомы и метаболические нарушения при сахарном диабете могут быть объяснены не только отсутствием синтеза инсулина. При второй форме сахарного диабета, так называемой инсулинрезистентной, имеют место и молекулярные дефекты: в частности, нарушение структуры инсулина или нарушение ферментативного превращения проинсулина в инсулин. В основе развития этой формы диабета часто лежит потеря рецепторами клеток-мишеней способности соединяться с молекулой инсулина, синтез которого нарушен, или синтез мутантного рецептора.
Существовует специфический рецептор инсулина на внешней плазматической мембране почти всех клеток организма, а также образования инсулинрецепторного комплекса. Рецептор синтезируется в виде предшественника – полипептида (1382 аминокислотных остатка), который далее расщепляется на α-и β-субъединицы, то есть на гетеродимер (в формуле α2–β2), связанные дисульфидными связями. Оказалось, что если α-субъединицы почти целиком располагаются на внешней стороне биомембраны, выполняя функцию связывания инсулина клетки, то β-субъединицы представляют собой трансмембранный белок, выполняющий функцию преобразования сигнала. Концентрация рецепторов инсулина на поверхности достигает 20000 на клетку, и период их полужизни составляет 7–12 ч.
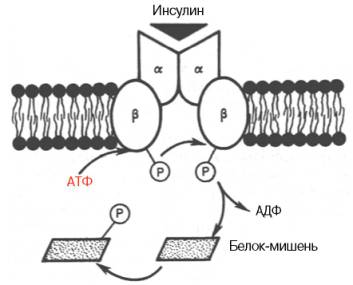
Инсулиновый рецептор (схема). Две α-цепи на наружной поверхности мембраны клетки и две трансмембранные β-цепи. Связывание инсулина с α-цепями запускает аутофосфорилирование остатков тирозина в β-цепях; активный тирозинкиназный домен затем участвует в фосфорилировании неактивных белков-мишеней в цитозоли.
Глюкагон
Глюкагон впервые был обнаружен в коммерческих препаратах инсулина еще в 1923 г., однако только в 1953 г. венгерский биохимик Ф. Штрауб получил этот гормон в гомогенном состоянии. Глюкагон синтезируется в основном в α-клетках панкреатических островков поджелудочной железы, а также в ряде клеток кишечника. Он представлен одной линейно расположенной полипептидной цепью, в состав которой входит 29 аминокислотных остатков.
Первичная структура глюкагонов человека и животных оказалась идентичной; исключение составляет только глюкагон индюка, у которого вместо аспарагина в положении 28 содержится серин. Особенностью структуры глюкагона является отсутствие дисульфидных связей и цистеина. Глюкагон образуется из своего предшественника проглюкагона, содержащего на С-конце полипептида дополнительный октапептид (8 остатков), отщепляемый в процессе постсинтетического протеолиза.
По биологическому действию глюкагон относятся к гипергликемическим факторам, вызывает увеличение концентрации глюкозы в крови главным образом за счет распада гликогена в печени. Органами-мишенями для глюкагона являются печень, миокард, жировая ткань. Биосинтез и секреция глюкагона контролируются главным образом концентрацией глюкозы по принципу обратной связи. На секрецию глюкагона оказывают влияние также инсулин и инсулиноподобные факторы роста.
В механизме действия глюкагона первичным является связывание со специфическими рецепторами мембран клеток, образовавшийся глюкагонрецепторный комплекс активирует аденилатциклазу и образование цАМФ. Последний активирует протеинкиназу, которая в свою очередь фосфорилирует киназу фосфорилазы и гликогенсинтазу. Фосфорилирование первого фермента способствует формированию активной гликогенфосфорилазы и соответственно распаду гликогена с образованием глюкозо-1-фосфата, в то время как фосфорилирование гликогенсинтазы сопровождается переходом ее в неактивную форму и соответственно блокированием синтеза гликогена.
Общим итогом действия глюкагона являются ускорение распада гликогена и торможение его синтеза в печени, что приводит к увеличению концентрации глюкозы в крови.
Глюкагон способствует образованию глюкозы из промежуточных продуктов обмена белков и жиров. Глюкагон стимулирует образование глюкозы из аминокислот путем индукции синтеза ферментов глюконеогенеза при участии цАМФ, в частности фосфоенолпируваткарбоксикиназы – ключевого фермента этого процесса.
Глюкагон тормозит гликолитический распад глюкозы до молочной кислоты, способствуя тем самым гипергликемии. Он активирует опосредованно через цАМФ липазу тканей, оказывая мощный липолитический эффект. Существуют и различия в физиологическом действии: глюкагон не повышает кровяного давления и не увеличивает частоту сердечных сокращений. Кроме панкреатического глюкагона существует еще кишечный глюкагон, синтезирующийся по всему пищеварительному тракту и поступающий в кровь.
Таким образом, панкреатические островки, синтезирующие два противоположного действия гормона – инсулин и глюкагон, выполняют ключевую роль в регуляции обмена веществ на молекулярном уровне.