Материал: Альонкіна К. В., Сотниченко Т. Д Хімія. Підготовка до ЗНО
тема 7. основи, солі, амфотеРні сПолуки
хімічні властивості основ
луги |
|
Нерозчинні гідроксиди |
Змінюють забарвлення індикаторів |
|
|
Взаємодіють із кислотами з утворенням солі й води (ре- |
Взаємодіють із кислотами з утворенням солі |
|
акція нейтралізації): |
|
й води (реакція нейтралізації): |
2KOH + H2SO4 → K2SO4 +2H2O |
|
Fe(OH)2 + H2SO4 → FeSO4 + 2H2O |
Взаємодіють із кислотними оксидами: |
|
Взаємодіють із кислотними оксидами (ангі- |
2NaOH + CO2 → Na2CO3 + H2O |
|
дридами сильних кислот): |
|
|
2Fe(OH)3 + 3SO3 → Fe2 (SO4 )3 + 3H2O |
Взаємодіють із амфотерними оксидами й гідроксидами: |
|
|
2NaOH +ZnO → Na2ZnO2 + H2O; |
|
|
KOH + Al(OH)3 → KAl(OH)4 |
|
|
Взаємодіють із солями, якщо виконується хоча б одна |
|
|
умова протікання реакцій обміну: |
|
|
2NaOH + CuSO4 → Cu(OH)2 ↓ + Na2SO4 ; |
|
|
NaOH + NaHCO3 → Na2CO3 + CO2 ↑ + H2O |
|
|
Гідроксиди лужних металів стійкі до нагрівання, гідро- |
При нагріванні розкладаються: |
|
ксиди лужноземельних металів розкладаються, але при |
2Fe(OH)3 t→Fe2O3 + 3H2O |
|
більш високій температурі, ніж нерозчинні гідроксиди: |
|
|
Ca(OH)2 t→CaO + H2O |
|
|
Добування основ |
||
луги |
|
Нерозчинні гідроксиди |
Електроліз водних розчинів солей: |
|
|
ел. струм |
|
|
2NaCl +2H2O →2NaOH +H2 +Cl2 |
|
|
Взаємодія металів з водою: |
|
|
2Na + 2H2O → 2NaOH + H2 |
|
|
Взаємодія оксидів з водою: |
|
|
Na2O + H2O →2NaOH; |
|
|
BaO + H2O → Ba(OH)2 |
|
|
Реакція обміну: |
Реакція обміну: |
|
Ba(OH)2 + K2SO4 → 2KOH + BaSO4 ↓ |
CuSO4 + 2NaOH → Cu(OH)2 ↓ + Na2SO4 |
|
СОлі
Солі — складні речовини, які складаються з йонів металічних елементів та кислотних залишків. Йони металічних елементів та кислотних залишків зв’язані один з одним відповідно до їхніх ва-
лентностей.
Назви солей складаються із двох слів: перше слово — назва металічного елемента (у називному відмінку), друге — назва кислотного залишку. Наприклад, цинк сульфід, натрій нітрат. Якщо металічний
50
www.e-ranok.com.ua
тема 7. основи, солі, амфотеРні сПолуки
елемент виявляє змінну валентність, то її обов’язково вказують у назві солі: купрум(ІІ) нітрат, ферум(ІІ) сульфат.
Формули солей складають аналогічно до формул оксидів, зрівнюючи число одиниць валентності металічногоелементатакислотногозалишку.Деякісолі,якішироковикористовуютьупобуті,окрімофіційних, мають ще й традиційні назви. Наприклад, натрій хлорид NaCl називають кухонною (кам’яною) сіллю, натрій карбонат Na2CO3 — це сода, калій карбонат K2CO3 — поташ.
Солі – електроліти, які дисоціюють у водних розчинах або розплавах на катіони металічних елементів та аніони кислотниз залишків.
Класифікація солей
Солі |
Кислі |
Середні |
Ознака |
Продукт неповного заміщення |
Складаються тільки |
|
атомів Гідрогену в кислоті атомом |
з атомів металічного |
|
металічного елемента |
елемента та кислот- |
|
|
них залишків |
якими речовинами |
Утворюються тільки багатооснов- |
Утворюються будь- |
утворюються |
ними кислотами |
якими кислотою та |
|
|
основою |
Приклади |
Натрій гідрогенсульфат |
Натрій сульфат |
й назви |
NaHSO4 ; |
Na2SO4 ; |
|
Калій дигідрогенфосфат |
Калій фосфат K3PO4 |
|
KH2PO4 |
|
Основні способи |
Взаємодія основ з кислотами: |
Взаємодія основ з |
добування |
KOH + H3PO4 → |
кислотами: |
|
→ KH2PO4 + H2O |
3КОН + Н3РО4 → |
|
Взаємодія солей з кислотами: |
К3РО4 + 3Н2О |
Na2SO4 + H2SO4 →
→2NaHSO4
Основні
Продукт неповного заміщення гідроксигруп основ на кислотний залишок
Утворюються тільки багатокислотними основами, не утворюються лугами
Купрум(ІІ) гідроксохлорид
Cu(OH)Cl;
Кальцій гідроксофосфат
Ca5 (PO4 )3 (OH)
Взаємодія основ з кислотами: Cu(OH)2 + HCl →
→ Cu(OH)Cl + H2O
Взаємодія солей з лугами: Fe2(SO4)3 + 2KOH →
→ 2Fe(OH)SO4 + K2SO4
хімічні властивості
 Дисоціація
Дисоціація
Термічне розкладання Взаємодіязметалами(керуючисьрядомактивності  З кислотними оксидами
З кислотними оксидами
З амфотерними оксидами
Зкислотами (склад продуктів залежить від молярних співвідношень вихідних речовин
Злугами або NH4OH (склад продуктів за-
лежить від молярних співвідношень вихідних речовин)
Солей між собою
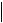 KCl ↔ K+ + Cl–
KCl ↔ K+ + Cl–
BaCO3 =t BaO + CO2
Hg(NO3)2 + Cu = Cu(NO3)2 + Hg
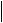 Na2CO3 + SiO2 =t Na2SiO3 + CO2↑
Na2CO3 + SiO2 =t Na2SiO3 + CO2↑
4KNO3 + 2Al2O3 =t 4KAlO2 + 4NO2↑ + O2↑ CuOHCl + HCl = CuCl2 + H2O;
Na2ZnO2 + 4HCl = 2NaCl + ZnCl2 + 2H2O
FeCl3 + NH4OH = FeOHCl2 + NH4Cl; MgCl2 + KOH = MgOHCl + KCl
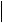 AgNO3 + Kl =Ag l ↓ + KNO3
AgNO3 + Kl =Ag l ↓ + KNO3
51
www.e-ranok.com.ua

тема 7. основи, солі, амфотеРні сПолуки |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Добування: |
|
|
|
|
|
|
|
|
Металу з неметалом |
Fe + S = FeS; 2Na + Cl2 = 2NaCl |
||||||||
Металу з кислотою |
Zn + 2HCl = ZnCl2 + H2↑ |
|
|||||||
Металу з лугом у розплавах |
Zn + 2NaOH = Na2ZnO2 + H2↑ |
|
|||||||
Металу з сіллю |
Fe + CuSO4 = FeSO4 + Cu |
|
|||||||
Неметалу з лугом |
3Cl2 + 6KOH =t 5KCl + KClO3 + 3H2O |
||||||||
Неметалу з сіллю |
Cl2 + 2Kl = I2 + 2KCl |
|
|
|
|||||
Основного оксиду з кислотою |
CaO + 2HCl = CaCl2 + H2O |
|
|||||||
Основи з кислотою |
Ba(OH)2 + H2SO4 = BaSO4↓ + 2H2O |
||||||||
Солі з кислотою |
CaCO3 + 2HNO3 = Ca(NO3)2 + CO2 + H2O |
||||||||
Основного оксиду з кислотним |
3MgO + P2O5 = Mg3(PO4)2 |
|
|||||||
Лугу з кислотним оксидом |
2KOH + Cl2O7 = 2KClO4 + H2O |
||||||||
Солі з лугом |
CuCl2 + 2KOH = Cu(OH)2↓ + 2KCl |
||||||||
Солі з кислотними оксидом |
CaCO |
3 |
+ SiO |
2 |
=t CaSiO |
3 |
+ CO |
↑ |
|
|
|
|
|
|
2 |
|
|||
Термічне розкладання солей |
2KClO3 =t 2KCl + 3O2↑ |
|
|
||||||
Солі з сіллю |
AgNO3 + KCl =AgCl↓ + KNO3 |
||||||||
АмфОтеРні ОКСиди тА гідРОКСиди
Таксамо,якіамфотернігідроксиди,амфотерніоксидивиявляютьтіжвластивості,щойзвичайніосновні оксидипривзаємодіїзкислотнимиречовинами.Привзаємодіїзосновнимиречовинамивонивступаютьуреакції як кислотні оксиди, тобто взаємодіють із основними оксидами й основами з утворенням солей.Амфотерні гідроксиди та відповідні їм кислоти й солі
Амфо |
Амфотерний гідроксид |
Відповідна йому кислота |
Кислотний залишок |
|||
|
|
|
|
|
|
|
терний |
|
|
|
|
формула |
|
оксид |
формула |
Назва |
формула |
Назва |
й валент |
Назва |
|
|
|
|
|
ність |
|
ZnО |
Zn(OH)2 |
цинк гідроксид |
H2ZnО2 |
Цинкатна |
ZnO |
|
цинкат |
|
|
|
|
|
II |
|
|
SnО |
Sn(OH)2 |
станум(ІІ) гідроксид |
H2SnО2 |
Станатна |
|
2 |
станат |
SnO |
|
||||||
|
|
|
|
|
II |
|
|
PbО |
Pb(OH)2 |
плюмбум(ІІ) гідроксид |
H2PbО2 |
Плюмбатна |
PbO |
2 |
плюмбат |
|
|||||||
|
|
|
|
|
II |
|
|
Al2O3 |
Al(OH)3 |
алюміній гідроксид |
H3AlО3 |
Алюмінатна |
AlO |
2 |
алюмінат |
|
|||||||
|
|
|
|
|
III |
|
|
|
|
|
|
|
|
3 |
|
Амфотерні сполуки
Амфотерними є сполуки, які можуть реагувати як з кислотами, так і з основами.
52
www.e-ranok.com.ua
тема 7. основи, солі, амфотеРні сПолуки
|
|
Взаємодія амфотерних оксидів |
||
Приклад |
З кислотами |
З основами |
||
ZnO, BeO |
ZnO + 2HCl = ZnCl2 + H2O |
ZnО + 2KOH спл → K2ZnO2 + H2O |
||
Cr2O3,Al2O3 |
Al2O3 + 3H2SO4 =Al2(SO4)3 +3H2O Al2O3 + 2NaOH спл → 2NaAlO2 + H2O |
|||
|
Амфотерні гідроксиди. хімічні властивості |
|||
1. Дисоціація (як кислоти і як |
Men+ + nOH– |
Me(OH)n = HnMeOn nH+ + MeOn–n |
||
основи) |
|
як основа |
як кислота |
|
2. Взаємодія з кислотами |
Zn(OH)2 + 2HNO3 = Zn(NO3)2 + 2H2O; |
|||
Cr(OH)3 + 3HCl = CrCl3 + 3H2O |
||||
|
|
|||
З лугами |
|
Zn(OH)2 + 2KOH= K2[Zn(OH)4] |
||
Способи одержання:
ZnSO4 + 2NaOH = Zn(OH)2↓ +Na2SO4
AlCl3 + 3NaOH =Al(OH)3↓ + 3NaCl
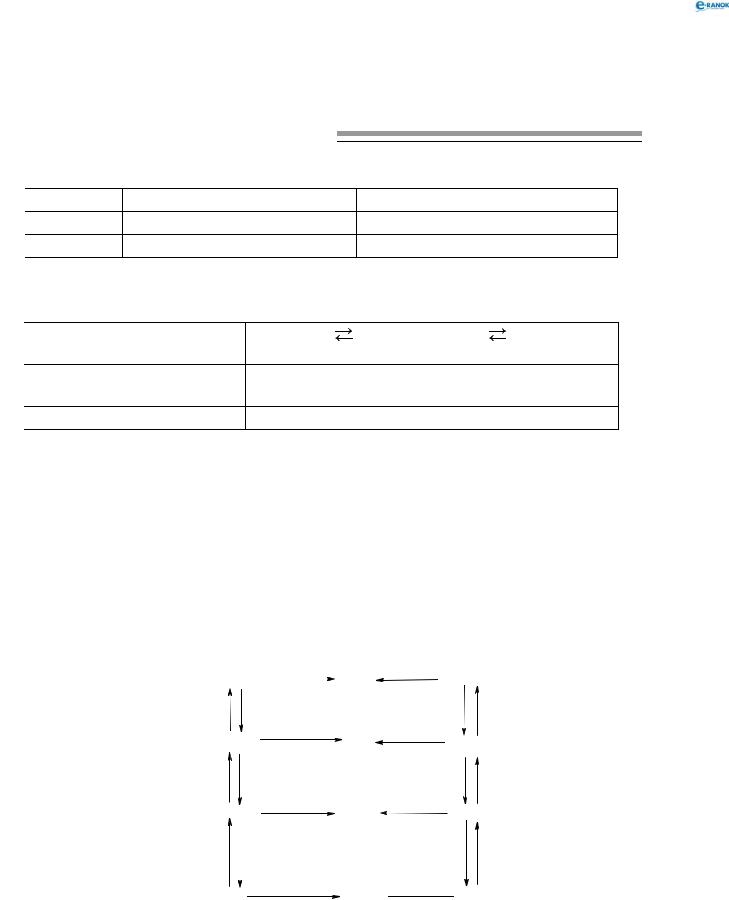
Генетичний зв’язок між класами неорганічних сполук
Взаємозв’язки між речовинами, які ґрунтуються на їх походженні і хімічних властивостях, називають генетичними зв’язками.
Генетичний зв’язок між класами сполук
Хімічні
елементи
Прості
речовини
Бінарні
сполукиоксиди
Гідрати
оксидів
Солі
Металічні |
|
|
|
|
Неметалічні |
Метали +Неметал |
(бінарніСолі |
+Метал |
Неметали |
||
+H2 + O2 |
|
сполуки) |
|
+ O2 |
|
|
|
|
|||
Основні |
|
Кислотний |
Солі |
Основний Кислотні |
|
оксиди |
|
||||
|
+ |
оксид |
|
+оксид |
оксиди |
+H2O |
|
+ H2O |
|||
Основи +Кислотнийоксид Солі
+Луг + Кислота
Солі |
+Сіль |
Солі |
|
|
+ Основнийоксид
 +Сіль
+Сіль
Кислоти
+Основи |
Кислота |
|
+ |
|
Солі |
Наводимо запис, який ілюструє взаємозв’язок між основою, сіллю, кислотою і кислотним оксидом:
→
Ca(OH)2 → CaCO3 ↔ CO2 ← H2CO3.
53
www.e-ranok.com.ua

тема 7. основи, солі, амфотеРні сПолуки
Приклади розв’язання задач
розв’язування задач на надлишок Задача 7.1. До розчину, який містить 20 г сульфату натрію, долили розчин, що містить 40 г нітрату
барію. Яка маса осаду утворилося?
Дано: |
|
|
|
Розв’язання: |
|
|
|
|
||
m (Na2SO4) = 20 г |
Аналізуючи умову задачі, бачимо що для обох солей, які реагують одна |
|||||||||
m (Ba(NO3)2) = 40 г з одною, зазначена певна маса. Це ознака того, що задача на надлишок, а він |
||||||||||
m (BaSO4↓) — ? |
не реагуватиме.Тому визначаємо, яка з вихідних речовин узята у надлишку. |
|||||||||
Для цього складаємо рівняння реакції: |
|
|
|
|
|
|
|
|
|
|
|
20 г |
40 г |
Х г |
|
|
|
|
|
|
|
|
Na2SO4 + Ba(NO3)2 = BaSO4 ↓ + 2NaNO3. |
|
|
|
||||||
|
142 г |
261 г |
233 г |
|
20 |
40 |
Na2SO4 |
|
Ba(NO3)2 |
|
|
|
|
|
|
|
. |
||||
Визначаємо кількісне співвідношення між реагентами |
|
142 |
= 261; |
0,14 |
< |
0,15 |
||||
Виходить, що Ba(NO3)2 взято в надлишку. Для розв’язування беремо Na2SO4: |
|
|
||||||||
|
20 |
Х |
20∙233 |
|
|
|
|
|
|
|
|
142 = |
233; X = |
142 |
|
= 32,8 г. |
|
|
|
|
|
Відповідь: m(BaSO4) = 32,8 г. |
|
|
|
|
|
|
|
|
|
|
виконайте контрольний тест
На його виконання відводиться 15 хвилин. Під час роботи над тестом не можна користуватися слов никами, підручниками, посібниками, довідниками тощо.
1. |
|
тест 14 (контрольний) |
|
||
Позначте назву елемента, що утворює амфотерні сполуки. |
|
||||
|
А Натрій |
В Карбон |
|||
|
Б Цнк |
|
Г Калій |
|
|
2. |
Позначте клас сполук, до якого відноситься речовина із складом NaCl. |
||||
|
А оксид |
В кислота |
|||
|
Б основа |
Г сіль |
|
||
3. |
Позначте пару солей, що будуть взаємодіяти одна з одною. |
|
|||
|
А аргентум нітрат та калій хлорид |
В алюміній хлорид та натрій сульфат |
|||
|
Б натрій хлорид, та калій нітрат |
Г кальцій хлорид та натрій нітрат |
|||
4. |
Установіть відповідність між реагентами та продуктами реакцій |
|
|||
|
А SO2 |
+ NaOH→ |
1 |
Na2SO4 |
+ H2O |
|
Б SO3 |
+ NaOH→ |
2 |
Na2SO3 |
+ H2O |
|
В SO2 |
+ 2NaOH→ |
3 |
NaHSO4 |
|
|
Г SO3 |
+ 2NaOH→ |
4 |
NaHSO3 |
|
5. |
Установіть генетичний ланцюг добування кальцій гідрогенкарбонату. |
||||
|
А кальцій оксид |
В кальцій |
|||
|
Б кальцій гідроген карбонат |
Г кальцій карбонат |
|||
6. Яку масу цинк сульфіду (г) можна добути при нагрівання 10 г цинку і 10 г сірки.
54
www.e-ranok.com.ua