Материал: Абсорбционные методы очистки отходящих газов
Из нейтрализатора часть суспензии выводят на центрифугу для отделения
кристаллогидратов солей магния. Обезвоживание солей производят в сушилках
барабанного типа с мазутной копкой. Безводные кристаллы обжигают во вращающихся
печах или печах кипящего слоя при 9000С, в печь добавляют кокс. При этом идет
реакция:
![]()
Концентрация ![]() в газе, выходящем из печи, 7 - 15%. Газ охлаждают, очищают от
пыли и сернокислотного тумана и направляют на переработку в серную кислоту.
в газе, выходящем из печи, 7 - 15%. Газ охлаждают, очищают от
пыли и сернокислотного тумана и направляют на переработку в серную кислоту.
Выгружаемый из печи продукт содержит 86,1% ![]() и 3,4%
и 3,4% ![]() . Его охлаждают до 1200С воздухом,
идущим на сгорание мазута в топках, после чего отправляют на абсорбцию.
. Его охлаждают до 1200С воздухом,
идущим на сгорание мазута в топках, после чего отправляют на абсорбцию.
Достоинства магнезитового метода: 1) возможность очищать горячие газы без предварительного охлаждения; 2) получение в качестве продукта рекуперации серной кислоты; 3) доступность и дешевизна хемосорбента; 4) высокая эффективность очистки.
Недостатки: 1) сложность технологической схемы; 2) неполное разложение
сульфата магния при обжиге; 3) значительные потери оксида магния при
регенерации.
3.2 Очистка газов от сероводорода
3.2.1 Вакуум - карбонатные методы
В этих методах сероводород поглощается из газов водным раствором
карбоната натрия или калия. Затем раствор регенерируют нагреванием под
вакуумом, охлаждают и снова возвращают на абсорбцию. В основе методов лежит
реакция:
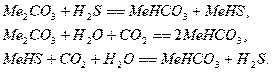
В следствие различной растворимости ![]() ,
, ![]() ,
, ![]() и
и ![]() для абсорбции применяют растворы
разной концентрации. Поташ лучше растворим в воде, поэтому применяются более
концентрированные его растворы, которые имеют высокую поглотительную
способность. Это позволяет уменьшит его расход, а также сократить расход пара
на регенерацию поташа и расход энергии на перекачивание раствора.
для абсорбции применяют растворы
разной концентрации. Поташ лучше растворим в воде, поэтому применяются более
концентрированные его растворы, которые имеют высокую поглотительную
способность. Это позволяет уменьшит его расход, а также сократить расход пара
на регенерацию поташа и расход энергии на перекачивание раствора.
Недостатком использования раствора поташа является их высокая стоимость. Исходя из этого, чаще используют содовый метод.
Если производится регенерация раствора без рекуперации сероводорода, то
раствор нагревают в регенераторе, а из него воздухом отдувают сероводород. При
этом некоторое количество сульфида натрия окисляется до тиосульфата, что
приводит к понижению концентрации абсорбирующей жидкости, поэтому периодически
ее заменяют свежей. Технологическая схема очистки газа от сероводорода вакуум -
карбонатном методом с получением из сероводорода серной кислоты приведена на
рис. 3.
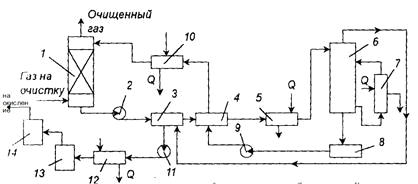
Рис. 3. Схема установки очистки газа от сероводорода вакуум - карбонатном
способом: 1 - абсорбер; 2, 9 - насосы; 3 - холодильник - конденсатор; 4 -
теплообменник; 5 - подогреватель; 6 - регенератор; 7 - циркуляционный
подогреватель; 10 - холодильник; 11 - вакуум - насос; 12 - холодильник; 13 -
печь; 14 - котел - утилизатор
После очистки газа в абсорбере раствор подают в холодильник -
конденсатор, где его подогревают за счет тепла конденсации паров, выделяющихся
при регенерации поглотительного раствора. Затем раствор проходит теплообменник
и подогреватель и поступает в регенератор. Раствор регенерирует кипячением под
вакуумом (15,6 кПа). Регенерированный раствор направляют в емкость, а затем
через теплообменник и холодильник - на орошение абсорбера. Выделяющиеся при
регенерации раствора пары сероводорода и воды отсасываются вакуумом - насосом
через конденсатор - холодильник, где конденсируется значительная часть паров
воды. Далее пары поступают в холодильник, а затем в печь для сжигания
сероводорода. Из печи газовая смесь, состоящая из диоксида серы, водяных паров,
кислорода и инертных газов, при 9000 С, а затем направляется на окисление в
контактный аппарат. После окисления газы направляют на абсорбцию для получения
серной кислоты.
3.2.2 Фосфатный процесс
Для абсорбции сероводорода фосфатным методом применяют растворы,
содержащие 40 -50% фосфата калия:
![]()
Из раствора сероводород удаляют кипячением при 107 - 1150С. Коррозии
кипятильников при этом не наблюдается. Растворы стабильны, не образуют
продуктов, ухудшающих их качество. Достоинством процесса является также
селективность раствора к сероводороду в присутствии ![]() .
.
3.2.3 Щелочно - гидрохиновый метод
Сущность метода в поглощении сероводорода щелочными растворами гидрохинона. При регенерации растворов выделяются элементарная сера и тиосульфата натрия. Гидрохинон является катализатором. Чем выше концентрация хинона в растворе, тем активнее раствор. Метод состоит из следующих стадий:
взаимодействие сероводорода с карбонатом натрия (содой)
![]()
окисление гид2росульфида натрия хиноном (окисленная форма гидрохинона)
![]()
![]()
![]()
регенерация соды
![]()
регенерация хинона
![]()
![]()
![]()
Последняя стадия осуществляется за счет кислорода, содержащегося в газе, и протекает параллельно с процессами поглощения и окисления сероводорода. Более полную регенерацию хинона проводят в регенераторах.
В процессе абсорбции протекает следующая побочная реакция:
![]()
Накопление в растворе ![]() и
и ![]() приводит к снижению его поглотительной способности вследствие
уменьшения концентрации карбоната натрия и снижения рН среды. Для поддержания
активности поглотительного раствора непрерывно добавляют свежие растворы соды и
гидрохинона. Для поддержания рН раствора в пределах 9 - 9,5 добавляют 42%-й
раствор едкого натрия.
приводит к снижению его поглотительной способности вследствие
уменьшения концентрации карбоната натрия и снижения рН среды. Для поддержания
активности поглотительного раствора непрерывно добавляют свежие растворы соды и
гидрохинона. Для поддержания рН раствора в пределах 9 - 9,5 добавляют 42%-й
раствор едкого натрия.
Абсорбцию сероводорода проводят в полом абсорбере с форсунками или плотности орошения 4,35 м3/ч на 1 м3 орошаемого объема. Раствор регенерируют, пропуская через него (барботаж) сжатый воздух. При этом происходит окисление гидрохинона до хинона и флотации выделившейся серы, которую в виде пены собирают на поверхности раствора. Одновременно здесь же происходит окисление части гидросульфида др тиосульфата. Серная пена собирается в пеносборнике, а затем поступает на вакуум - фильтр, где происходит ее отделение. Полученную серу плавят в автоклаве.
Метод позволяют очистить газ от начального содержания сероводорода в газе
0,185 г/м3 до 0,02 г/м3. степень очистки газа зависит от концентрации в нем
сероводорода, скорости движения газа в абсорбере и интенсивности орошения,
концентрации активных компонентов в растворе и его рН, температуры процесса, от
равномерности распределения раствора в абсорбере.
3.3 Очистка газов от оксидов азота
3.3.1 Абсорбция водой
При абсорбции диоксида азота водой в газовую фазу выделяется часть оксида
азота, скорость окисления которого при низких концентрациях мала:
![]()
Для утилизации оксидов можно использовать разбавленные растворы пероксида
водорода с получением азотной кислоты:
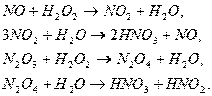
Основным фактором, определяющим экономику процесса, является расход пероксида водорода. Он приблизительно равен 6 кг на 1 т кислоты в сутки.
Разработан процесс очистки газов водой и циркулирующей ![]() . Физическая абсорбция оксидов азота
в азотной кислоте увеличивается с ростом концентрации кислоты и парциального
давления
. Физическая абсорбция оксидов азота
в азотной кислоте увеличивается с ростом концентрации кислоты и парциального
давления ![]() . Увеличение поверхности контакта
способствует протеканию процесса, так как на границе раздела фаз идет реакция
окисления NO в NO2. Для интенсификации процесса используют катализатор. Степень
очистки может достигать 97%.
. Увеличение поверхности контакта
способствует протеканию процесса, так как на границе раздела фаз идет реакция
окисления NO в NO2. Для интенсификации процесса используют катализатор. Степень
очистки может достигать 97%.
![]()
Уравнения для хемосорбции ![]() различными щелочными растворами или суспензиями представлены
ниже:
различными щелочными растворами или суспензиями представлены
ниже:
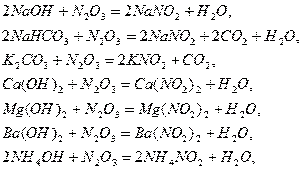
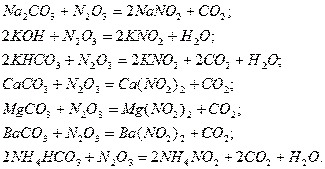
При абсорбции ![]() активность щелочных растворов убивает в такой
последовательности:
активность щелочных растворов убивает в такой
последовательности:
![]()
0,84 0,80 0,78 0,63 0,56 0,51 0,44 0,4
![]()
,40 0,39 0,35
Цифры под каждым из щелочных растворов показывают их активность
относительно раствора ![]() , активность которого условно принята за единицу. Данные
приведены для начальной концентрации растворов 100 г/л и времени проскока газа
10 мин. Активность щелочных растворов определяется начальным рН раствора.
Активность тем выше, чем выше этот показатель.
, активность которого условно принята за единицу. Данные
приведены для начальной концентрации растворов 100 г/л и времени проскока газа
10 мин. Активность щелочных растворов определяется начальным рН раствора.
Активность тем выше, чем выше этот показатель.
При абсорбции растворами аммиака образуются соединения с низкой
температурой разложения. Например, образующийся нитрит аммония ![]() при 560С полностью распадается:
при 560С полностью распадается:
![]()
3.3.3 Селективные абсорбенты
Для очистки газов от ![]() при отсутствии в газовой фазе кислорода могут быть
использованы растворы
при отсутствии в газовой фазе кислорода могут быть
использованы растворы ![]()
![]()
![]()
![]() для первых растворов протекают реакции с образованием
комплексов:
для первых растворов протекают реакции с образованием
комплексов:
![]()
При нагреве до 95 - 1000С комплекс ![]() распадается и
распадается и ![]() выделяется в чистом виде, а
восстановленный раствор вновь возвращают в производстве. Аналогично разлагается
и комплекс
выделяется в чистом виде, а
восстановленный раствор вновь возвращают в производстве. Аналогично разлагается
и комплекс ![]() .
.
Раствор ![]() является наиболее доступным и эффективным поглотителем. В
качестве абсорбента могут быть использованы и травильные растворы, содержащие
является наиболее доступным и эффективным поглотителем. В
качестве абсорбента могут быть использованы и травильные растворы, содержащие ![]() . Поглотительная способность раствора
зависит от концентрации
. Поглотительная способность раствора
зависит от концентрации ![]() в растворе, температуры и концентрации
в растворе, температуры и концентрации ![]() в газе. При температурах 20 - 250С
раствор может поглощать
в газе. При температурах 20 - 250С
раствор может поглощать ![]() даже при небольших концентрациях. Предел растворимости
оксидов азота соответствует соотношению
даже при небольших концентрациях. Предел растворимости
оксидов азота соответствует соотношению ![]() . Присутствие в растворе серной и
азотной кислот, солей и органических веществ снижает его поглотительную
способность. Однако наличие в растворе 0,5 - 1,5% (об.) серной кислоты
предохраняет
. Присутствие в растворе серной и
азотной кислот, солей и органических веществ снижает его поглотительную
способность. Однако наличие в растворе 0,5 - 1,5% (об.) серной кислоты
предохраняет ![]() от окисления кислородом воздуха до
от окисления кислородом воздуха до ![]() .
.
Использование растворов
![]() ,
, ![]() ,
, ![]() приводит к дефиксации азота:
приводит к дефиксации азота:
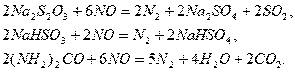
Таким же образом ![]() взаимодействует и с растворами
взаимодействует и с растворами ![]() ,
, ![]() ,
, ![]() .
.
При температуре выше 2000С ![]() взаимодействует с аммиаком по
реакции:
взаимодействует с аммиаком по
реакции:
![]() .
.
Серная кислота используется для поглощения ![]() и
и ![]() с образованием нитрозилсерной
кислоты:
с образованием нитрозилсерной
кислоты:
![]()
При нагревании нитрозилсерной кислоты или при разбавлении ее водой
происходит выделение оксидов азота:
![]()
Взаимодействие оксидов азота с жидкими сорбентами наиболее эффективно
протекает при 20 - 400С.
4 Технологический расчет аппаратов
. Масса поглощаемого вещества и расхода поглотителя
Пересчитаем исходные концентрации в относительные массовые доли:
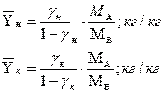
где:
![]() - мольная масса абсорбтива;
- мольная масса абсорбтива;
![]() - мольная масса инертного газа;
- мольная масса инертного газа;
Объемный расход инертного газа при рабочих условиях:
![]()
Массовый расход инертного газа:
![]()
![]()
где: ![]() - плотность инертного газа при 0 0C;
- плотность инертного газа при 0 0C;
Уравнение материального баланса:
![]()
Используя данные равновесия:
![]()
Отсюда минимальный расход поглотителя:
![]() , так как
, так как ![]() здесь
здесь
![]() концентрация абсорбтива в воде, равновесная с газом
начального состава; определяем из уравнения равновесной прямой:
концентрация абсорбтива в воде, равновесная с газом
начального состава; определяем из уравнения равновесной прямой:
![]() здесь
здесь
![]() - мольная масса воды
- мольная масса воды
![]() =>
=> ![]() , где
, где
![]() где
где ![]() ,
,
здесь Е-коэффициент Генри, П-давление среды.
Действительный расход:
![]()
Удельный расход поглотителя:
![]()