Материал: Абсорбционные методы очистки отходящих газов
Абсорбционные методы очистки отходящих газов
Содержание
Введение
Теоритические основы абсорбции
Растворы газов в жидкостях
Абсорбционные методы очистки отходящих газов от примесей кислого характера
.1 Очистка газов от диоксида серы
.1.1 Абсорбция водой
.1.2 Известняковые и известковые методы
.1.3 Магнезитовый метод
.2 Очистка газов от сероводорода
.2.1 Вакуум - карбонатные методы
.2.2 Фосфатный процесс
.2.3 Щелочно - гидрохиновый метод
.3 Очистка газов от оксидов азота
.3.1 Абсорбция водой
.3.2 Абсорбция щелочами
.3.3 Селективные абсорбенты
Технологический расчет аппаратов
Преимущества и недостатки абсорбционных методов очистки отходящих газов
Заключение
Список литературы
Введение
Многие технологические процессы на предприятиях металлургической, химической, нефтехимической промышленности, в ряде цехов машиностроительных заводов, на многих других производствах сопровождаются поступлением вредных газов и паров в атмосферный воздух. Активным загрязнителем атмосферного воздуха является транспорт, в первую очередь, автомобильный. Газовые загрязнения, как и аэрозольные, загрязняя атмосферный воздух, значительно ухудшают его качество, а в ряде случаев делают его непригодным для нахождения в нем людей. Санитарные нормы ограничивают концентрацию вредных паров и газов в воздухе населенных пунктов, однако эти требования не всегда соблюдаются. Это наносит значительный ущерб здоровью людей, проживающих в местностях, подверженных воздействию вредных газов и паров, ведению сельского хозяйства в данном районе, организации отдыха людей, приводит к повреждению архитектурных сооружений, памятников истории и культуры и т.д.
Под очисткой газового потока понимают отделение от него или превращения в безвредную форму загрязняющих веществ, выбрасываемых в атмосферу вместе с газовым потоком. Воздушными массами загрязнения могут переноситься на большие расстояния и существенно влиять на состояние атмосферы и здоровья человека.
Цель данной работы - рассмотреть и изучить абсорбционные методы очистки
отходящих газов.
1 Теоретические основы абсорбции
Абсорбцией называется перенос компонентов газовой смеси в объем соприкасающейся с ней конденсированной фазы. При абсорбции происходит избирательное поглощение одного или нескольких компонентов из газовой смеси жидкими поглотителями.
Вещество, которое содержится в газовой фазе и при абсорбции не переходит в жидкую фазу, называют газом-носителем, вещество, в котором происходит растворение абсорбируемых компонентов, называют растворителем (поглотителем или абсорбентом), вещество, которое содержится в газовой фазе и при абсорбции переходит в жидкую фазу, т.е. поглощаемый компонент, называют абсорбтивом, поглощаемое вещество в объеме поглотителя - абсорбатом. Абсорбат удерживаются в абсорбенте, равномерно распределяясь среди его молекул, вследствие растворения или химической реакции.
Процесс, завершающийся растворением абсорбата в поглотителе, называют физической абсорбцией. При физической абсорбции происходит физическое растворение абсорбируемого компонента в растворителе, при этом молекулы абсорбента и молекулы абсорбтива не вступают между собой в химическое взаимодействие.
Иногда растворяющийся газ вступает в химическую реакцию непосредственно с самим растворителем. Процесс, сопровождающийся химической реакцией между поглощаемым компонентом и абсорбентом, называют химической абсорбцией (хемосорбция). При хемосорбции абсорбируемый компонент вступает в химическую реакцию с поглотителем, образуя новые химические соединения в жидкой фазе.
Абсорбция представляет процесс химической технологии, включающей массоперенос между газообразным компонентом и жидким растворителем, осуществляемый в аппарате для контактирования газа с жидкостью. Аппараты, в которых осуществляют процесс абсорбции, называют абсорберы. Абсорбция - наиболее распространенный процесс очистки газовых смесей во многих отраслях, например, в химической промышленности.
Абсорбцию широко применяют для очистки выбросов от сероводорода, других
сернистых соединений, паров соляной, серной кислот, цианистых соединений,
органических веществ (фенола, формальдегида и др.).
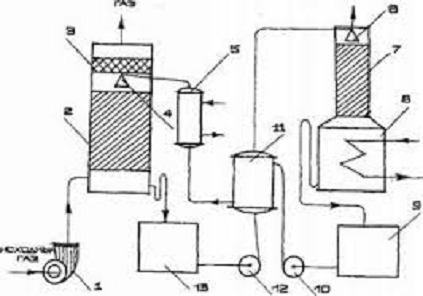
Рис. 1. Схема абсорбционной установки: 1 - вентилятор (газодувка);
2-абсорбер; 3-брызгоотбойник; 4,6-оросители; 5-холодильник; 7-десорбер; 8-куб
десорбера; 9,13-ёмкость для абсорбента; 10,12-насосы;
11-теплообменникрекуператор
Абсорбционная система может быть простой, в которой жидкость применяется только один раз и удаляется из системы без отделения абсорбированного загрязнения. В другом варианте загрязнение отделяют от абсорбирующей жидкости, выделяя её в чистом виде. Затем абсорбент вновь подают на стадию абсорбции, снова регенерируют и возвращают в систему.
Регенерацию поглотителей проводят физическими методами: повышением температуры, снижением давления либо сочетанием указанных параметров.
2 Растворы газов в жидкостях
Растворение газа в жидкости называют абсорбцией газа жидкостью. По своей природе и свойствам растворы газов в жидкости ничем не отличаются от других жидких растворов.
Влияние давления при не слишком высоких его значениях достаточно хорошо выражается законом Генри: при постоянной температуре растворимость газа в растворителе прямо пропорциональна давлению этого газа над раствором.
Как правило, растворение газов в воде происходит с выделением тепла и с
уменьшением объема, поэтому в соответствии с принципом Ле Шателье при повышении
температуры их растворимость снижается. Это иллюстрируют данные (табл. 1.) по
содержанию (в нормальных литрах) некоторых газов в 1 л воды при 760 мм рт. ст.:
Таблица 1
|
Газ |
0°C |
20°C |
60°C |
100°C |
|
Н2 |
0,021 |
0,018 |
0,016 |
0,016 |
|
CO2 |
1,713 |
0,88 |
0,36 |
- |
|
NH3 |
1176 |
702 |
- |
- |
При хемосорбции в качестве абсорбента используют водные растворы солей, органические вещества и водные суспензии различных веществ. При использовании воды абсорбируемый газ должен достаточно хорошо растворяться в ней при данной температуре в системе газ-жидкость. Для абсорбции газообразных загрязнителей с ограниченной растворимостью в воде, таких как SO2 или бензол, необходимы очень большие количества воды. Вода обладает высокой эффективностью при удалении кислых растворимых газов, таких как HCl, HF и SiF4 при использовании слабощелочной воды, для улавливания NH3 подкисленной водой. Газы с меньшей растворимостью, например SO2, Cl2 и H2S, легче абсорбируются не чистой водой, а щелочными растворами, в частности, разбавленным NaOH или водным раствором (суспензией) извести, т.е. в последнем случае более приемлема хемосорбция.
Нецелесообразно использовать воду для очистки выбросов с нерастворимыми в
ней органическими примесями. Подобные загрязнители как правило хорошо
поглощаются органическими жидкостями, среди которых могут использоваться как
абсорбенты высококипящие вещества, такие как этаноламины и тяжелые предельные
углеводороды (минеральные масла). Абсорбция органическим растворителем наиболее
эффективна для удаления органических газообразных загрязнителей, поскольку в
этом случае обеспечивается хорошая растворимость. В качестве органических
жидких абсорбентов применяются диметиланилин, моно-, ди- и триэтаноламин и
метилдиэтаноламин. Использование таких абсорбентов ограничено системами, не содержащими
твёрдых частиц, поскольку твердые вещества загрязняют органические жидкости.
3 Абсорбционные методы очистки отходящих газов от примесей кислого характера
3.1 Очистка газов от диоксида серы
3.1.1 Абсорбция водой
Абсорбция водой диоксида серы сопровождается реакцией:
![]()
![]()
Растворимость SO![]() в воде мала. Зависимость между общей концентрацией SO
в воде мала. Зависимость между общей концентрацией SO![]() а растворе и равновесным давлением
а растворе и равновесным давлением ![]() выражается формулой:
выражается формулой:
![]() ,
,
где ![]() - равновесное давление SO
- равновесное давление SO![]() ;
; ![]() - константа фазового равновесия для
SO
- константа фазового равновесия для
SO![]() , м
, м![]() *Па/кмоль; К - константа равновесия
реакции.
*Па/кмоль; К - константа равновесия
реакции.
При абсорбции SO![]() водой процесс лимитируется диффузионным сопротивлением со
стороны газа и жидкости. Он может быть проведен а абсорберах различной
конструкции. Для колонн с провальными и сетчатыми тарелками коэффициенты
массоотдачи могут быть определены из уравнений:
водой процесс лимитируется диффузионным сопротивлением со
стороны газа и жидкости. Он может быть проведен а абсорберах различной
конструкции. Для колонн с провальными и сетчатыми тарелками коэффициенты
массоотдачи могут быть определены из уравнений:
![]() ,
,
![]() ,
,
где ![]() и
и ![]() - диффузионные критерии Нуссельта для газа и жидкости;
- диффузионные критерии Нуссельта для газа и жидкости; ![]() и
и ![]() - диффузионные критерии Прандтля для
газа и жидкости;
- диффузионные критерии Прандтля для
газа и жидкости; ![]() и
и ![]() - критерии Рейнольдса для газа и жидкости;
- критерии Рейнольдса для газа и жидкости; ![]() и
и ![]() - коэффициенты массоотдачи со стороны
газа и жидкости, м/с;
- коэффициенты массоотдачи со стороны
газа и жидкости, м/с; ![]() - поверхностно-объемный диаметр пузырьков газа, м (
- поверхностно-объемный диаметр пузырьков газа, м (![]() ;
; ![]() и
и ![]() - коэффициенты молекулярной диффузии
SO
- коэффициенты молекулярной диффузии
SO![]() в газе и жидкости, м
в газе и жидкости, м![]() /с;
/с; ![]() и
и ![]() - кинематические коэффициенты
вязкости газа и жидкости, м
- кинематические коэффициенты
вязкости газа и жидкости, м![]() /с;
/с; ![]() и
и ![]() - скорость газа и жидкости а газожидкостном слое, м/с.
- скорость газа и жидкости а газожидкостном слое, м/с.
В связи с низкой растворимостью диоксида серы в воде для очистки
требуется большой ее расход и абсорберы с большими объемами. Удаление SO![]() из раствора ведут при нагревании его
до 100
из раствора ведут при нагревании его
до 100![]() С. Таким образом, проведение процесса
связано с большими энергозатратами.
С. Таким образом, проведение процесса
связано с большими энергозатратами.
На практике применяются известняк, мел, доломиты, мергели. Известь
получают обжигом карбонатных пород при температуре 1100 - 1300![]() С.
С.
Процесс абсорбции диоксида серы для известкового и известнякового методов
представляется в виде следующих стадий:
![]() ,
,
![]() ,
,
![]() ,
,
![]() ,
,
![]() ,
,
![]() ,
,
Протекание тех или иных реакций зависит от состава и рН суспензии. В
присутствии в растворе различных примесей процесс абсорбции значительно
усложняется. Например, действие небольших количеств ![]() повышает степень очистки и степень
использования известняка. При этом протекают следующие реакции:
повышает степень очистки и степень
использования известняка. При этом протекают следующие реакции:
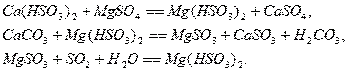
Для расчета равновесия при использовании солей кальция предложены эмпирические уравнения:
для системы
![]() :
:
![]()
для системы
![]() :
:
![]()
![]()
для системы
![]()
![]()
![]()
![]() .
.
3.1.3 Магнезитовый метод
Диоксид серы в этом случае поглощают оксид - гидрооксидом магния. В
процессе хемосорбции образуются кристаллогидраты сульфита магния, которые
сушат, а затем термически разлагают на ![]() -содержащий газ и оксид магния. Газ
перерабатывают в серную кислоту, а оксид магния возвращают на абсорбцию.
-содержащий газ и оксид магния. Газ
перерабатывают в серную кислоту, а оксид магния возвращают на абсорбцию.
В абсорбере протекают следующие реакции:
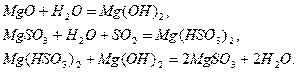
Растворимость сульфита магния в воде ограничена, избыток его в виде ![]() и
и ![]() выпадает в осадок. Технологическая
схема процесса представлена на рис. 2.
выпадает в осадок. Технологическая
схема процесса представлена на рис. 2.
Дымовые газы поступают в абсорбер Вентури, орошаемый циркулирующей
суспензией. Отношение Т:Ж в суспензии 1:10, рН суспензии на входе 6,8 - 7,5, а
на выходе из абсорбера 5,5 - 6. состав циркулирующей суспензии (в %):
![]()
![]()
![]() вода и примеси - 79,65.
вода и примеси - 79,65.
В абсорбере кроме сульфита образуется некоторое количество сульфата:
![]()
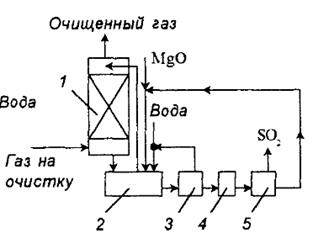
Рис. 2. схема установки очистки газа от диоксида серы суспензией оксида
магния: 1 - абсорбер; 2 - нейтрализатор; 3 - центрифуга; 4 - сушка; 5 - печь
Образование сульфата нежелательно, так как для его разложения необходима
более высокая температура (1200-13000С). При таких условиях получается
переобожженный ![]() , который имеет малую активность по отношению к
, который имеет малую активность по отношению к ![]() . Для устранения образования сульфата
необходимо использовать ингибиторы окисления или проводить процесс в абсорберах
при малом времени контакта газ - жидкость. Другой путь - производить обжиг
сульфата в присутствии восстановителей. В этом случае сульфат восстанавливается
в сульфит.
. Для устранения образования сульфата
необходимо использовать ингибиторы окисления или проводить процесс в абсорберах
при малом времени контакта газ - жидкость. Другой путь - производить обжиг
сульфата в присутствии восстановителей. В этом случае сульфат восстанавливается
в сульфит.