Материал: Molbiol_Misha
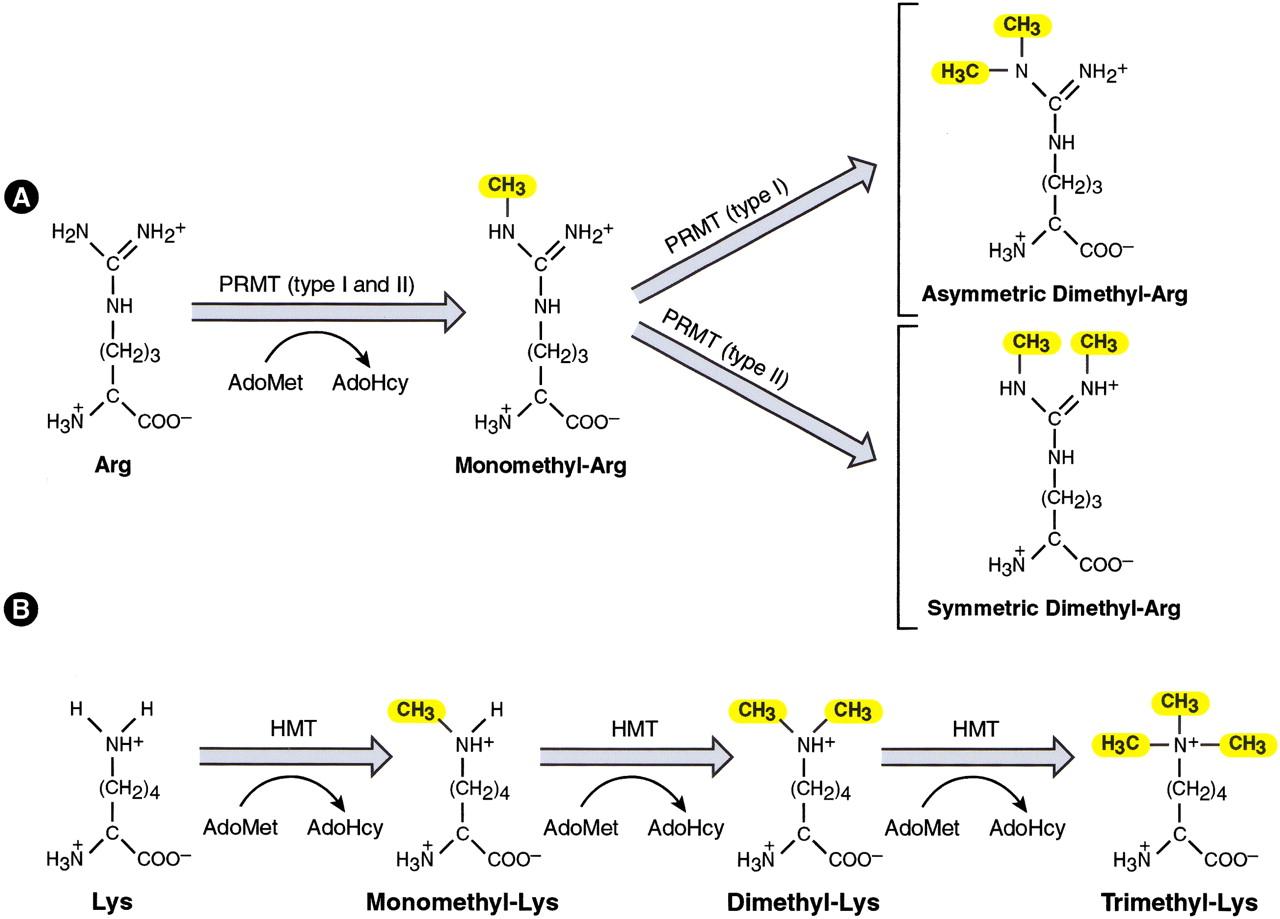
Метилирование лизина и аргинина:
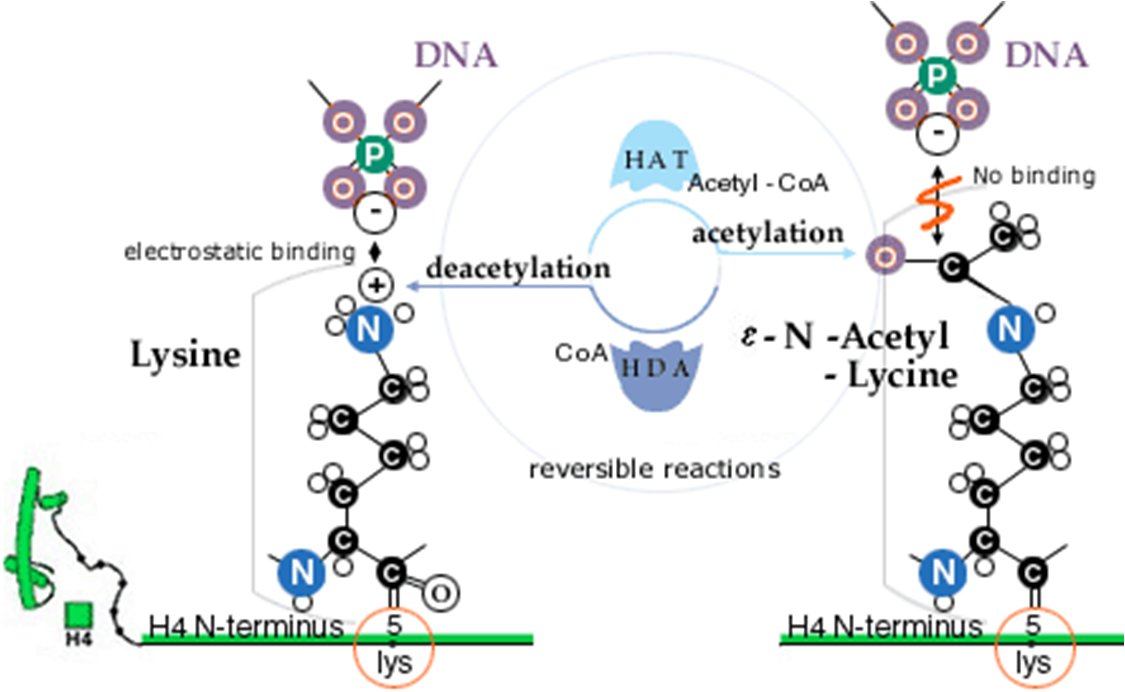
Убиквитинилирование и сумоилирование – присоединение к остаткам лизина коротких полиептидов (С-концевая аминокислота убиквитина или SUMO присоединяется ε-аминогруппе лизина). Убиквитин – короткий (76 аминокисл. остатков) полипептид. Крайне консервативен (всего три различия между убиквитином человека и дрожжей). SUMO (Small Ubiquitin Modifier) 98 аминокислотных остатков. Присоединение через изопептидную связь (амидная связь между не альфа-аминогруппой лизина гистонов и кабоксильной группой на С-конце пептидов).
Модификации гистонов могут:
1. прямо влиять на свойство октамера гистонов (например посредством
снижения заряда)
2. Выполнять сигнальную функцию, способствую привлечения различных
белков (ГИСТОНОВЫЙ КОД).
Важен не только тип модификации, но и количественные характеристики модификаций. Например, монометилирование и триметилирование лизина могут иметь прямо противоположные последствия.
В последние годы охарактеризовано много «вариантных» форм гистонов, некоторые из которых выполняют специальные функции. Примеры: H1 имеет варианты Н5 в эритроцитах птиц, варианты Н11-Н18 в мышиных клетках. Н2А: macro H2A имеет 64% гомологии с H2A, присутствует в неактивной копии Х хромосомы, Н2А.Х маркирует мишени для репарации. Н3 имеет вариантные формы CENP-A и Cid, встречающиеся в центромерах. Н3.3 – активный хроматин.
«Основные» и «вариантные» формы гистонов кодируются разными генами.
Следующий уровень компактизации – 30 нм фибрилла:
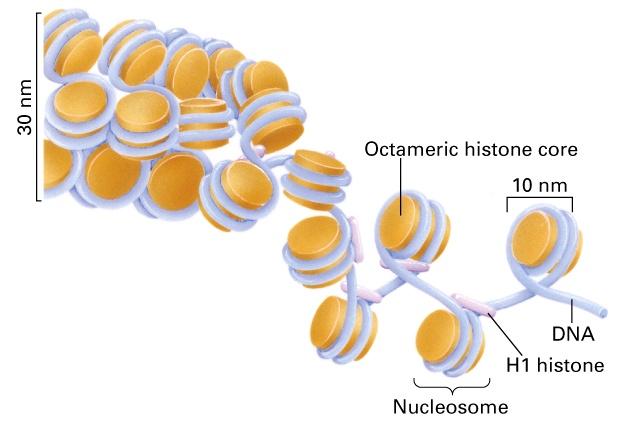
Последние исследования показали, что канонической 30 нм фибриллы просто не существует. В ядре присутствует набор разнообразных компактных хроматиновых фибрилл, толщина которых близка к 30 нм.
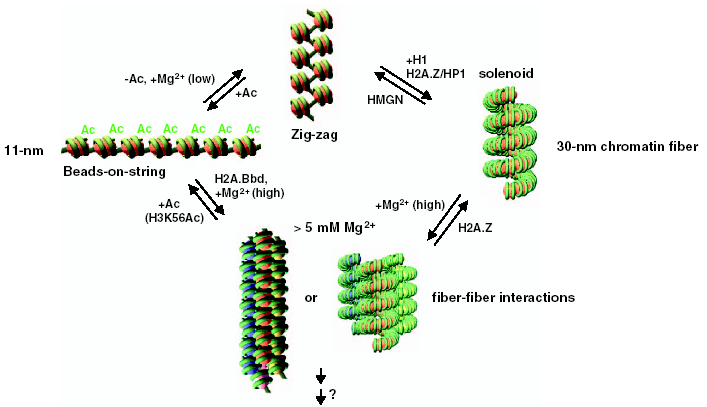
Существует целый ряд факторов, влияющих на степень конденсации хроматина, среди которых наиболее изучено ацетилирование гистонов: выявлено, что ацетилирование ведёт к эухроматинизации (т.е. открытию фибрилл, деконденсации). Распределение ацетилированных форм гистонов в протяженных доменах генома можно изучать с использованием метода иммунопреципитации хроматина (ChIP). Профиль ацетилирования гистонов в общих чертах совпадает с профилем чувствительности к ДНКазе I.
Важную сигнальную роль играет ацетилирование/метилирование гистона H3 по позиции К9 (лизин-9).
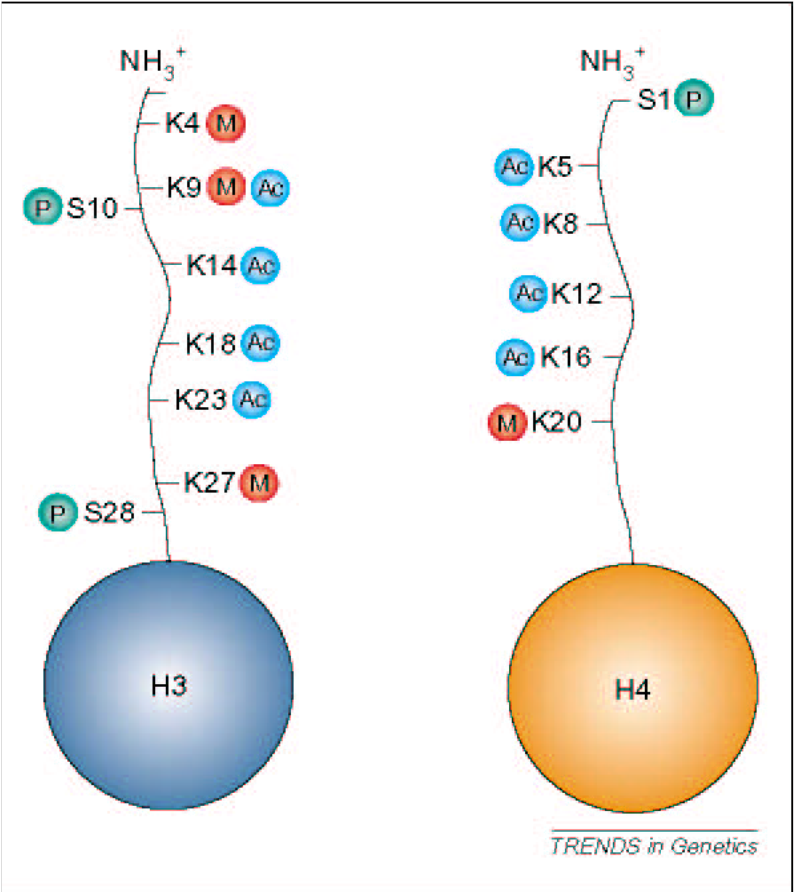
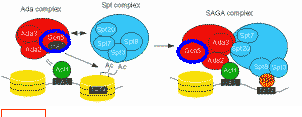
Ферменты, выполняющие модификации: гистонацетилазы, гистонметилазы, гистонфосфорилазы. Выполняющие удаление модификаций: гистондеацетилазы и тому подобное. В узнавании сигналов участвуют специфические белковые домены: бромодомен узнаёт ацетилирование К9 в Н3, а хромодомен – метилирование того же остатка. Ферменты, как правило, входят в состав мультисубъединичных комплексов. Например, в такие:
Суммарная информация по влиянию различных модификаций на активность хроматина:
-
Ацетилирование активизирует хроматин, как и метилирование аргинина.
-
Эффект метилирования лизина зависит от позиции.
-
Н3К4 триметилирование – связывание промоторов.
-
Н3К4 диметилирование – связывание энхансеров.
-
Н3К9 ди- и триметилирование ведет к образованию конститутивного гетерохроматина.
-
Н3К27 триметилирование ведет к образованию факультативного гетерохроматина.
Бромодомены (связывание с активным хроматином) содержат следующие белки:
1. RSC комплекс ремоделирования хроматина
2. TAF(II)250/CCG1 (белок, ассоциированный с TFIID)
3. коактиваторы транскрипции полимеразой II (p300)
4. некоторые транскрипционные факторы
Хромодомены (связывание с гистоном Н3, метилированным по К9 или К27, т.е. с неактивным хроматином) содержат эти белки:
1. HP1, Рс
2. Mi2 (AТФазная субъединица комплекса NURF сочетающего ремоделирующую хроматин и гистон-деацетилазную активности).
Ацетилирование Н3К9 может вызвать лавинообразную реакцию гиперацетилирования, благодаря активации НАТ (histone acetylase), имеющей бромодомен.
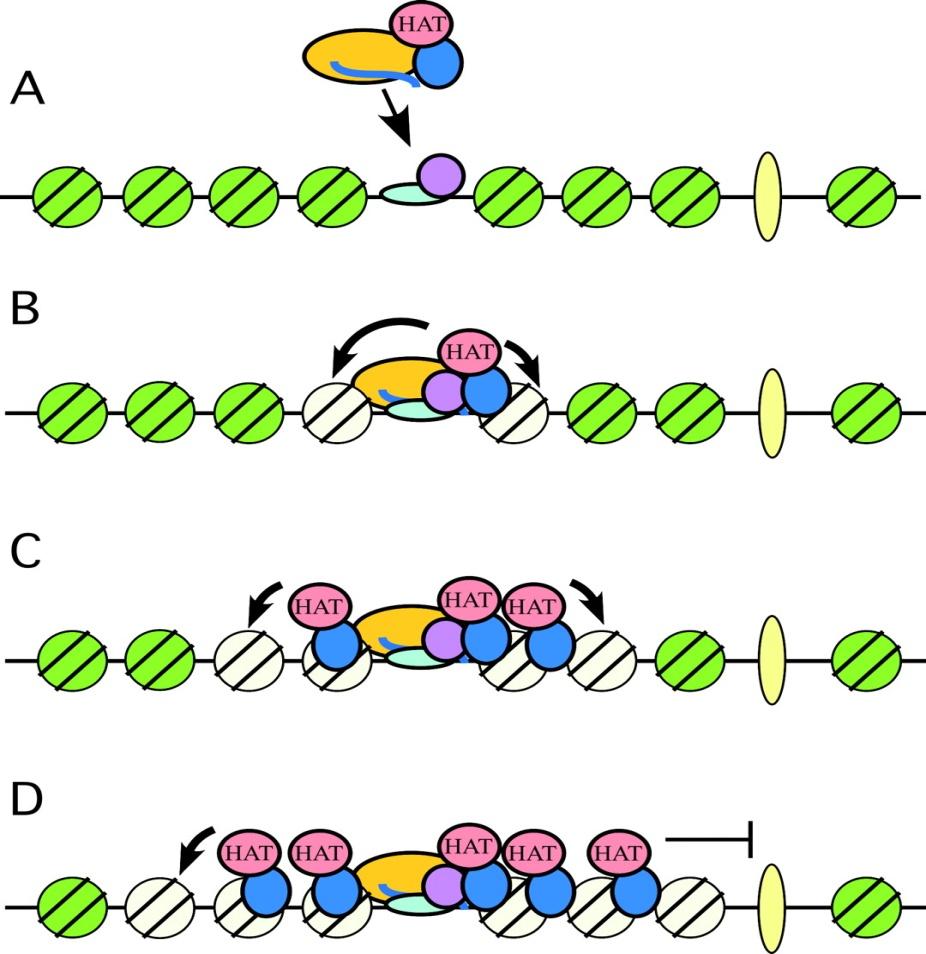
Создание неактивного хроматина инактивирует гены, как и метилирование ДНК (последнее, напомню, проиходит по CpG сайтам под действием ДНК-метилтрансферазы).
Неактивность хроматина не является конститутивным положением ДНК, а наоборот, требует создания. Важнейшими факторами в гетерохроматинизации являются элементы PEV-системы. PEV связан с упаковкой домена в конститутивный гетерохроматин. Существует целый ряд мутаций, подавляющих PEV (Suvars). Изучение соответствующих генов позволило идентифицировать ключевые белковые продукты, необходимые для поддержания компактной упаковки неактивных доменов. Важнейшими из них являются гистонметилазы и структурные белки гетерохроматина (HP1 у человека, Sir белки у дрожжей). Su(var)3-9 – SET-доменный белок, метилирующий Н3К9, что приводит к конденсации хроматина.
Репликационно-зависимая сборка нуклеосом:
В цитоплазме Н3-Н4 димеры подвергаются ацетилированию Hat1 (которая не участвует в ацетилирование собранных нуклеосом). Затем гетеродимеры транспортируются в ядро шаперонами CAF-1 и ASF-1 (комплексы с ним называются RCAF). Затем CAF1 привлекается PCNA в репликационную вилку, а ASF1 привлекается туда же CAF1. Здесь из гетеродимеров собирается тетрамер. Спустя некоторый лаг-период фермент HDAC1 деацетилирует гистоны. В течение лаг-периода комплекс не устойчив и главные формы гистонов могут быть заменены на варианты. Гетеродимеры Н2А-Н2В собираются в цитоплазме и переносятся в ядро при посредстве шаперона NAP1 (Nucleosome Assembly Protein 1). В ядре они связываются с уже собранными тетрамерами (H3-H4)2. Комплексы ремоделирования хроматина RCF and ACF обеспечивают регулярное распределение нуклеосом.
КАК ЭПИГЕНЕТИЧЕСКИЕ МОДИФИКАЦИИ ВОСПРОИЗВОДЯТСЯ ПОСЛЕ КЛЕТОЧНОГО ДЕЛЕНИЯ?
В случае неактивных доменов важную роль играет DNMT1.
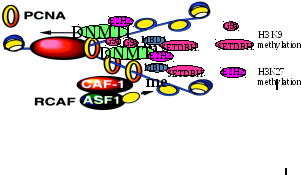
Билет № 7.
2. Редактирование РНК
Смотри второй вопрос первого билета.
Билет № 9.
1. Регуляция инициации репликации ДНК у E. coli. Структура участка старта репликации (origin, ori). Структурные переходы ДНК в районе старта репликации. Репликатор.
Пока нет ничего.
2. Активные и неактивные домены хроматина. Механизмы формирования
Смотри билет 6, вопрос 2.