Материал: Molbiol_Misha
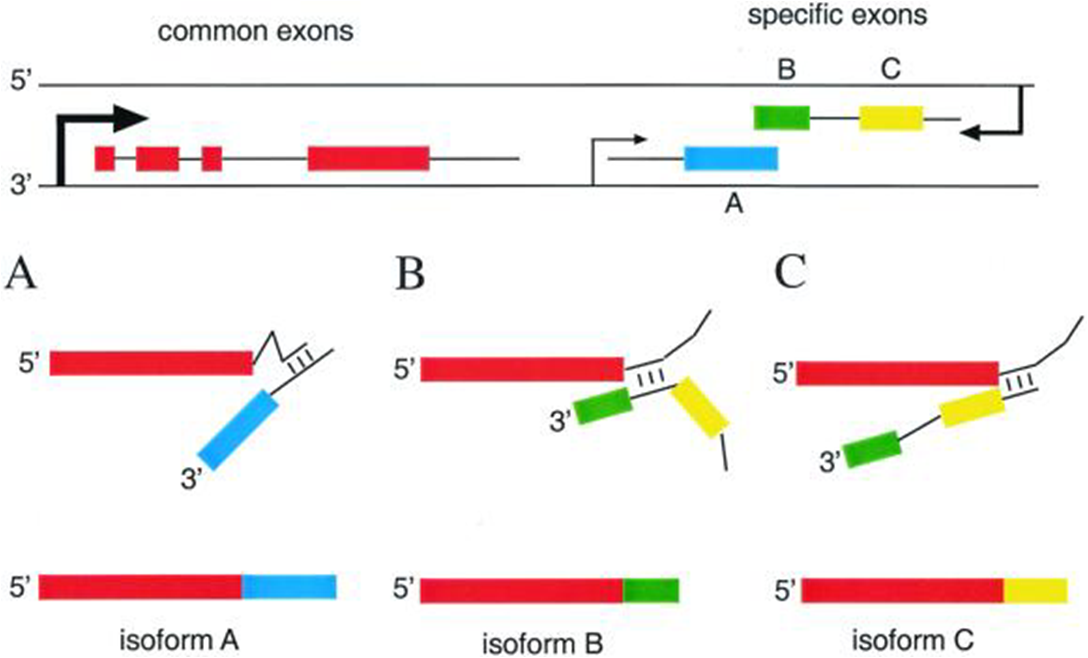
Многообразие мРНК, а следовательно и белков, кодируемых одним геном, существенно возрастает благодаря использованию альтернативных промоторов.
Резюме сплайсинга и прелюдия к остальному процессингу: в классической молекулярной биологии геном называли последовательность ДНК, кодирующую определенный белок. У высших эукариот такого рода ген формируется только на уровне мРНК.
Преобразования 5’ конца м РНК (присоединение 7-метилгуанина)
Cap: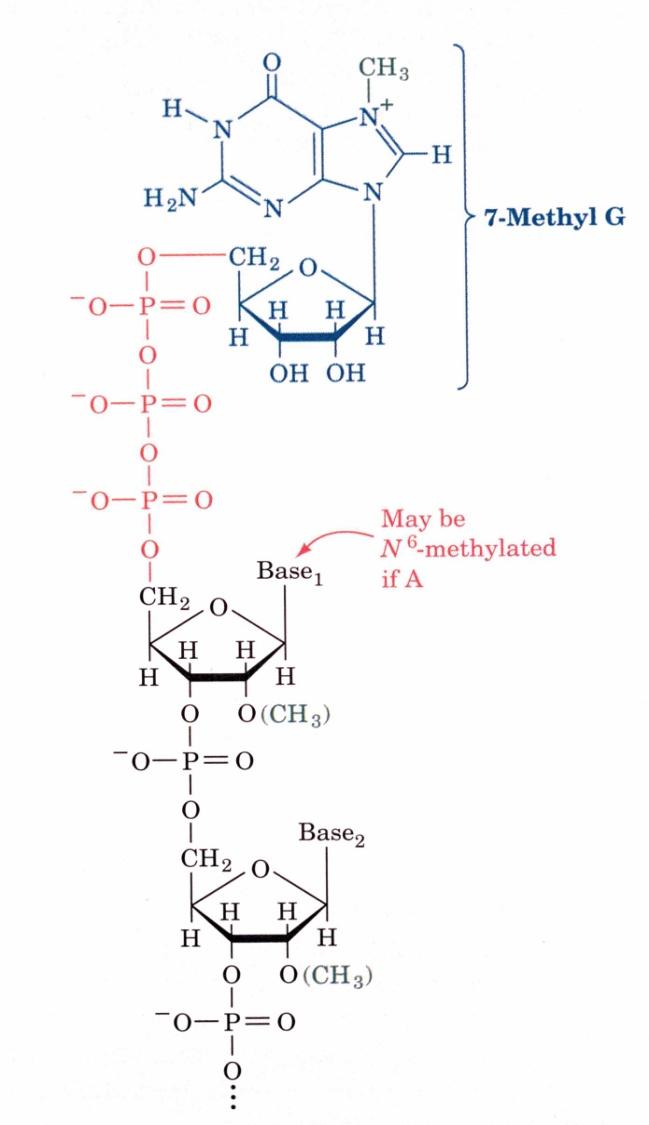
-
Защищает РНК от экзонуклеазного расщепления
-
Спсобствует трансляции
-
Способствует транспорту РНК из ядра в цитоплазму
-
5’ cap представляет собой «перевернутый» остаток гуанина, присоединенный к mRNA посредством 5’-5’ связи.
-
Гуанозин в составе Cap-структуры обычно метилирован.
-
Первый и второй нуклеотидные остатки в мРНК тоже часто метилируются по 2'-О-положению остатка рибозы.
Ферменты, участвующие в кэпировании: фосфогидролаза (РНК-трифосфатаза) отщепляет один из фосфатов на 5'-конце мРНК (остаётся два); гуанилитрансфераза использует ГТФ, чтобы присоединить к 5'-концу гуанин (побочный продукт – пирофосфат); гуанин-7-метилтрансфераза метилирует остаток гуанина по 7 положению, используя SAM – S-аденозилметионин. Далее могут последовать необязательные реакции: метилирование первого и второго остатков в цепи с помощью 2'-О-метилтрансферазы.
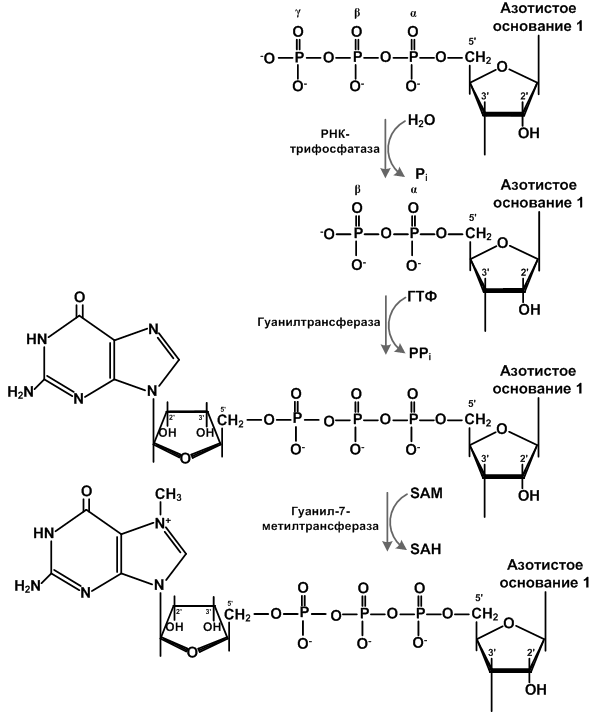
На 2013 год известны следующие типы кэпа:
-
кэп 0 (m7GpppNp, где N — любой нуклеотид) — это минимальная кэпирующая структура, которая представляет собой 7-метилгуанозин, соединённый 5',5'-трифосфатным мостиком с первым нуклеотидом РНК[1]. Кэп 0 распознаётся фактором инициации трансляции eIF4E;
-
кэп 1 (m7GpppNm2'-Op) отличается от кэпа 0 метилированием первого нуклеотида транскрипта по 2'-O положению рибозы;
-
кэп 2 (m7GpppNm2'-OpNm2'-Op) отличается от кэпа 0 метилированием первого и второго нуклеотидов транскрипта по 2'-O положению рибозы;
-
кэп 4 (m7GpppNm2'-OpNm2'-OpNm2'-OpNm2'-Op) соответственно;
-
2,2,7-триметилгуанозиновый кэп (m2,2,7GpppNp) характерен для малых ядерных РНК и служит сигналом к их транспорту и/или удержанию в ядре (Кугот, 2004 год).
Связь с транскрипцией
Кэпирование в процессе транскрипции обеспечивается тем, что соответствующие ферменты напрямую связываются с фосфорилированным C-концевым доменом большой субъединицы РНК-полимеразы II. Важно отметить, что не только транскрипция определяет ход кэпирования, но и успешность процесса кэпирования оказывает влияние на дальнейший ход транскрипции.
Кэп-структура стимулирует сплайсинг пре-мРНК как in vitro, так и in vivo, причём в большей степени стимулируется вырезание интрона ближайшего к 5'-концу транскрипта. Позитивное действие кэпа на сплайсинг объясняется следующим образом: сразу после присоединения кэпа к 5'-концу транскрипта с ним связывается кэп-связывающий комплекс CBC (англ. cap binding complex), который важен для последующих этапов процессинга пре-мРНК.
Наличие кэпа стимулирует эндопротеолитическое расщепление 3'-конца мРНК при полиаденилировании.
Полиаденилирование 3'-конца РНК.
-
Поли А «хвост» имеет размер 200-250 н.
-
Сигналом полиаденилирования является AAТAAA, за которым следует Г Т –богатая последовательность (23-24 пн) и Т богатая последовательность.
-
Транскрибирующая полимераза проходит через сигнал полиаденилирования, после чего РНК расщепляется и особый фермент синтезирует поли А.
Эндонуклеаза
расщепляет цепь РНК, а фермент
полиаденилат-полимераза использует
АТФ, чтобы сконструировать полиаденилатный
конец.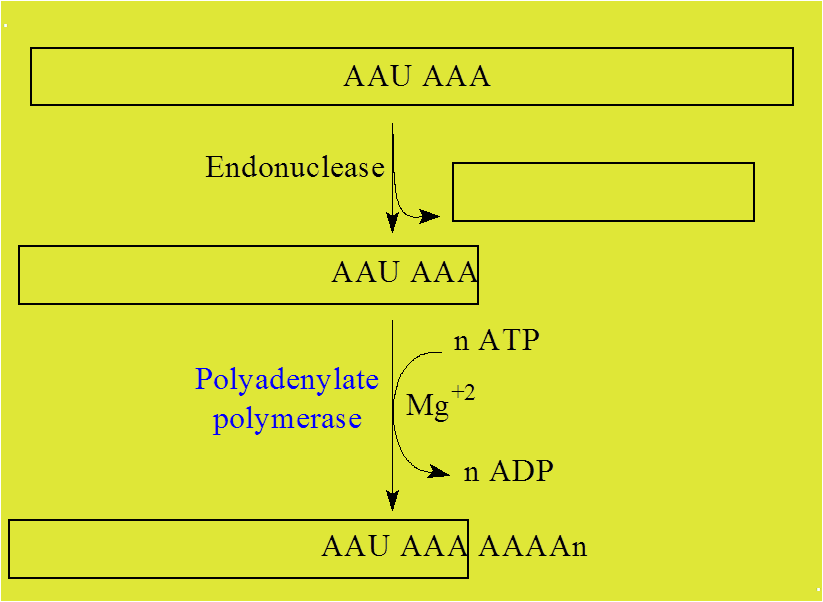
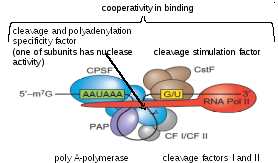
Ферменты, участвующие в «кэпировании» сплайсинге и полиаденилировании, рекрутируются фосфорилированным CTD-доменом РНК полимеразы II.
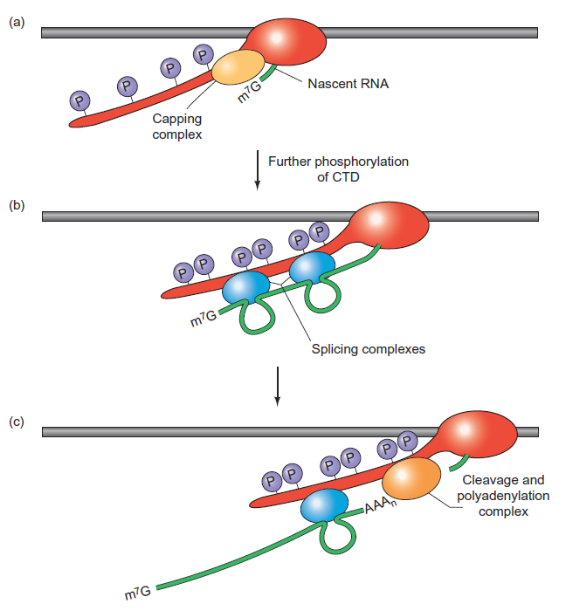
Терминация транскрипции происходит на расстоянии нескольких т.п.н. после сигнала полиаденилирования. Для терминации нужен разрыв в РНК, но не нужно само полиаденилирование. В синтезирующуюся после сигнала полиаденилировани молекулу РНК могут вноситься дополнительные разрывы (в глобиновых генах есть специальный элемент (CoTC – CoTranscriptional Clleavage), который автокатализирует разрыв, с сохранением фосфатной группы на 5’-конце. Разорванная РНК атакуется экзонуклеазой, которая, дойдя до РНК полимеразы, стимулирует ее диссоциацию от матрицы (cходство с ρ-зависимой терминацией у бактерий).
У трипаносом существует процесс уридилового редактирования кинетопластных РНК. Процесс редактирования осуществляется в направлении от 3’ конца РНК к 5’ концу при участии особых гидовых РНК, которые также кодируются геномом кинетопласта.
Другие виды редактирования
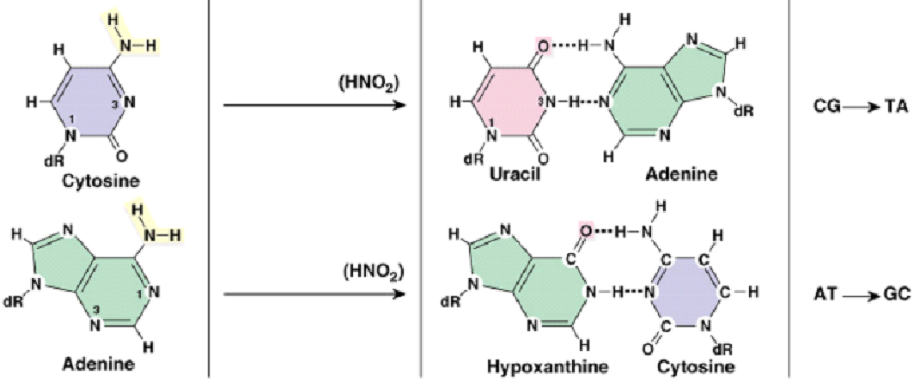
Дезаминирование аденина (превращение аденозина в инозин) – изменение смысла ряда кодонов так как A-T но I-C. Фермент adenosine deaminase acting on RNA (ADAR) (у человека три гена, кодирующих разные ADAR. Дезаминирование цитозина (превращение цитидина в уридин) фермент cytidine deaminase acting on RNA (CDAR).
Билет № 2.
2. Структура промотора РНК полимеразы II и основные этапы сборки пре-инициаторного комплекса.
У Арины в билетах.
Билет № 3.
1. Неканонические формы ДНК. Комплементарные пары оснований Уотсона-Крика и Хугстина. Триплексы.
Комплементарные пары оснований Уотсона-Крика:
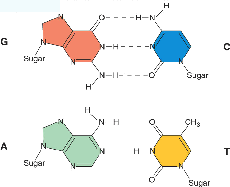
Также возможно такое спаривание:
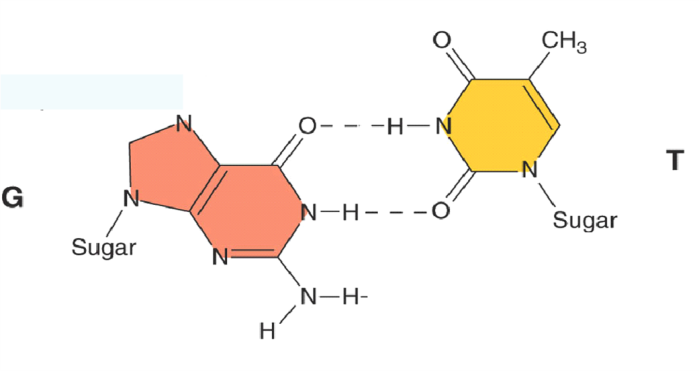
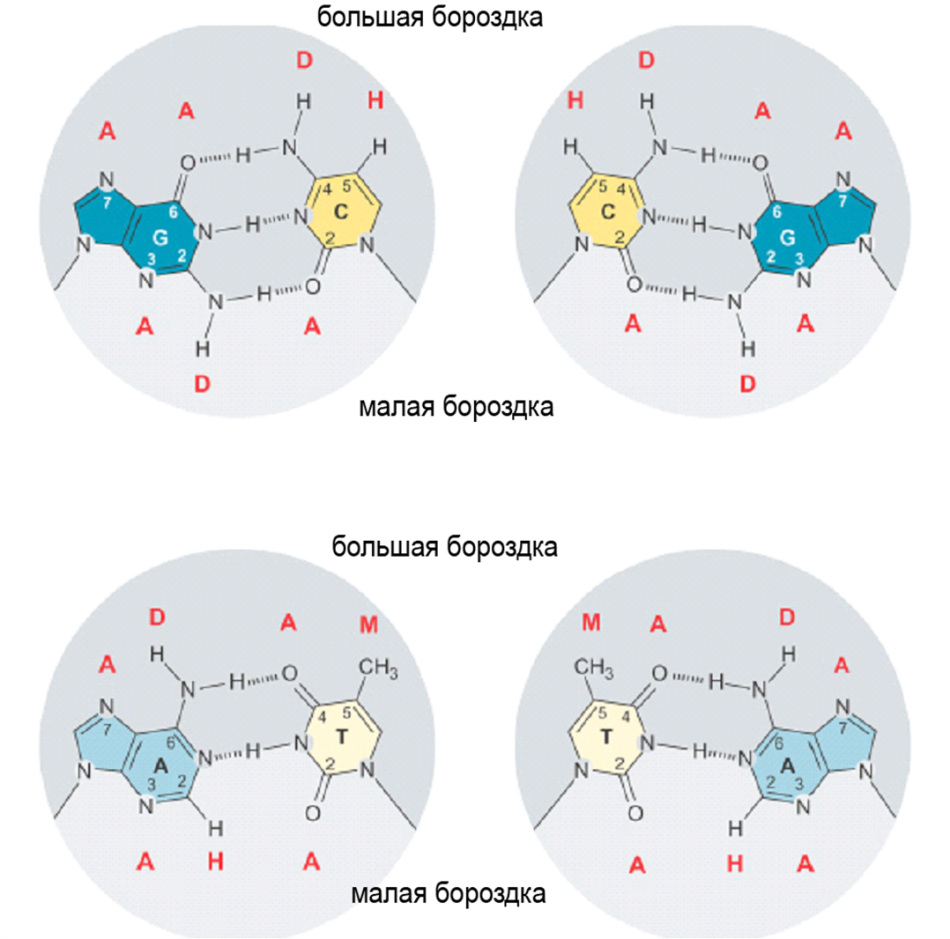
Параметры Уотсон-Криковских пар: расстояние между атомами сахара, связывающими основания (расстояние С1'-С1') в обоих случаях (AT и GC) равно 10,85 А. Угол между гликозильной связью (сахар-основание) и линией водородных связей – 51,5 град. ДНК по Уотсону-Крику – В-форма, антипараллельные цепи, есть малая и большая бороздки, шаг спирали – 33,2 А, 10 пар нуклеотидов на виток, отклонение плоскости оснований от горизонтальной равно -1,2 град. Спираль в В-форме правозакрученная. А-форма типична для двухцепочечной РНК и гибридов ДНК-РНК и имеет шаг спирали в 24,6 А, 10,7 п.н. на виток, отклонение от горизонтальной плоскости – 19 град. Спираль в А-форме правозакрученная (как и в В-форме). В Z-форме существует ДНК теломер, к примеру. В этой форме основания перевернуты, шаг спирали – 45,6 А, 12 п.н. на виток, спираль левозакрученная. Эту форму при определённых условиях может принимать ДНК с последовательностью поли dG/dC. Последовательности, способные образ. Z-форму, присутствуют в промоторах некоторых генов. Можно получить антитела к Z-форме, с помощью них было продемонстрировано, что такая форма есть в живой клетке. Во всех формах ДНК возможны разнообразные движения плоскости оснований друг относительно друга: вращения по разл. осям (z-twist, x-tilt, y-roll), смещения (z-rise, x-shift, y-slide), а также вращение оснований внтури одной пары: opening (sigma), propeller twist (omega), buckle (kappa), stogger (Sz), stretch (Sy), shear (Sx). В двухцепочечной ДНК Уотсон-Криковские пары замкнуты и не участвуют в узнавании лигандов, экспонированными остаются: в большую бороздку для пары АТ – метил тимина, кислород-4 тимина, водород аминогруппы аденина, азот-7 аденина; в малую для АТ – кислород-2 тимина, азот-3 аденина. Для ГЦ – в большую бороздку: водород цитозина, водород аминогруппы цитозина, кислород-6 и азот-7 гуанина, а в малую – кислород-2 цитозина, водород аминогруппы гуанина и азот-3 гуанина. Таким образом формируется специфичное сочетание атомов-доноров и акцепторов водородной связи (на рис. отмечены D и A, соответственно) для каждой последовательности, что и определяет взаимодействие ДНК с белками (обычно посредством остатков глутамина, серина, аспарагина, лизина и аргинина).
Хугстиновские пары – алтернативный вариант связывания нуклеотидов на комплементарных цепях нуклеиновых кислот ДНК и РНК, соединенных с помощью водородных связей не по каноническому Уотсон-Крику связыванию оснований. Пурины в Хугстиновских парах поворачиваются на 180 град. (находятся в син-ориентации). Хугстиновские пары наблюдаются редко, но для некоторых последовательностей ДНК, особенно в 5штрих-СА-3штрих и 5штрих-ТА-3-штрих динуклеотидах, они наблюдаются в равновесии с Уотсон-Криковскими парами.
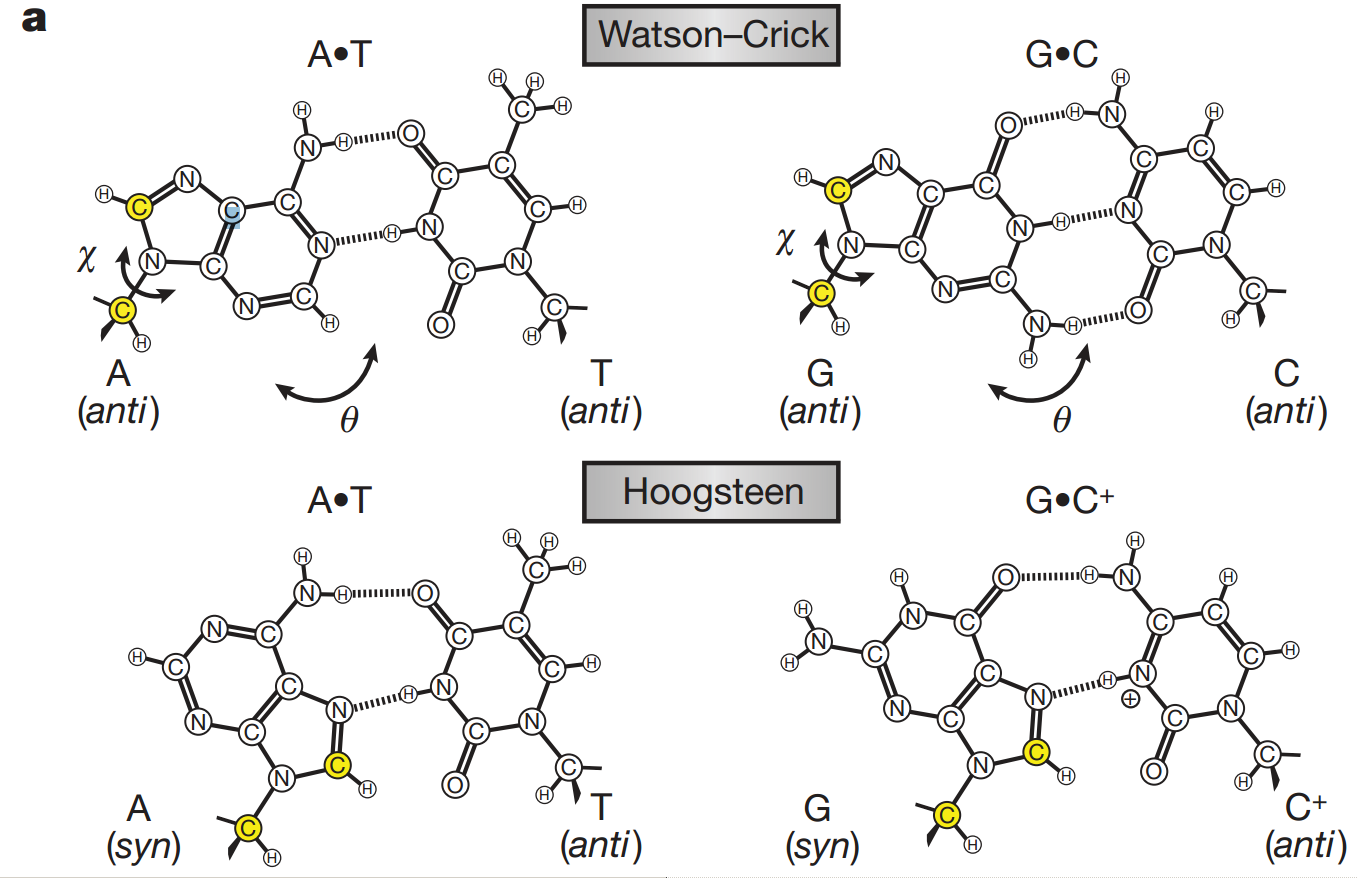
Отличия в параметрах: угол между гликозильными связями больше в Хугстиновских парах и составляет 80 град, расстояние С1штрих – С1-штрих меньше, всего 8,2 А. Хугстиновские пары стабилизируют триплексы ДНК: протонированный цитозин может формировать две водородные связи с гуанозином в ГЦ У-К паре, а тимидин формирует две водородные связи с аденозином в АТ У-К паре. За счёт этого может образовываться триплексная структура.
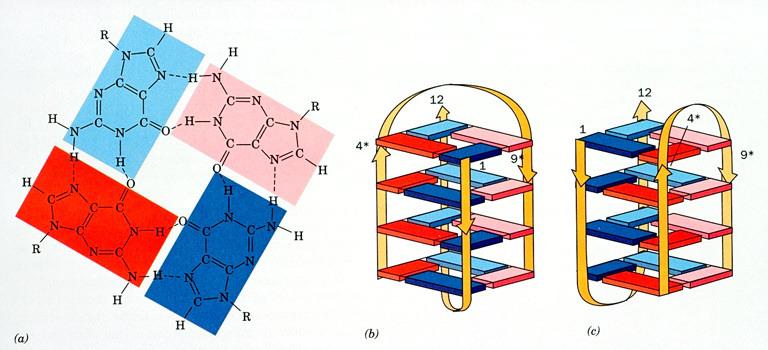
Квадруплекс ДНК также формируется за счёт Хугстиновских пар оснований и часто присутствует в теломерах, в том числе у человека.
2. Химические модификации гистонов нуклеосом. Вариантные формы гистонов. Понятие о «гистоновом коде». Активный и неактивный хроматин. Механизмы репрессии генов, обусловленные деацетилированием и метилированием гистонов.
Смотри билет 6, вопрос 2.
Билет № 4.
2. Расположение нуклеосом на молекуле ДНК. АТФ-зависимое «ремоделирование» хроматина.
Связывание гистонов с ДНК не является специфичным в отношении последовательности так как гистоны не не образуют водородных связей с азотистыми основаниями. Тем не менее, позиционирование нуклеосом на ДНК подчиняется определенным закономерностям. Существует две важных характеристики: СПЕЙСИНГ
ФАЙЗИНГ.
Секвенирование фрагментов ДНК, накрученных на нуклеосомные глобулы, позволило выявить последовательности ДНК предпочтительные и, наоборот, неудобные для посадки нуклеосом. Как изучали? После жесткой обработки стафилококковой нуклеазой, не деградированной остается только ДНК, связанная с нуклеосомными глобулами. Затем выделяли 145 п.н. фрагменты и секвенировали.
Некоторые последовательности ДНК являются предпочтительными для посадки нуклеосом в силу способности легко накручиваться на гистоновый октамер. Другие последовательности, напротив, вообще не могут накручиваться на гистоновый октамер.
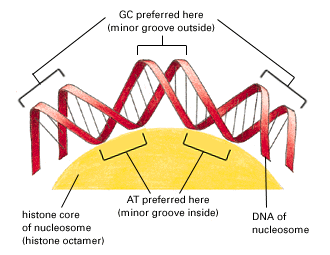
С учетом выявленных закономерностей разработано несколько компьютерных программ, позволяющих достаточно точно предсказать расположение нуклеосом на любой последовательности ДНК.
Жесткое позиционирование нуклеосом может препятствовать связыванию транскрипционных факторов. Присутствие нуклеосом на регуляторных последовательностях (например, на промоторах) может создать серьезные проблемы для работы регуляторных механизмов.Эти проблемы решаются при участии комплексов ремоделирования хроматина. Существует три основных группы комплексов ремоделирования хроматина: GROP, PROTOTIPE, ATPase. Пример GROP – Swi/Snf переносит нуклеосому на другой участок ДНК, а одна из PROTOTIPE, а именно NURF передвигает (sliding) нуклеосому от гена. Этот процесс требует затраты АТФ – swi2/snf2 передвигает нуклеосому на 50 п.н. на одну молекулу АТФ, другие ремоделирующие системы – по 10 п.н. на одну АТФ.
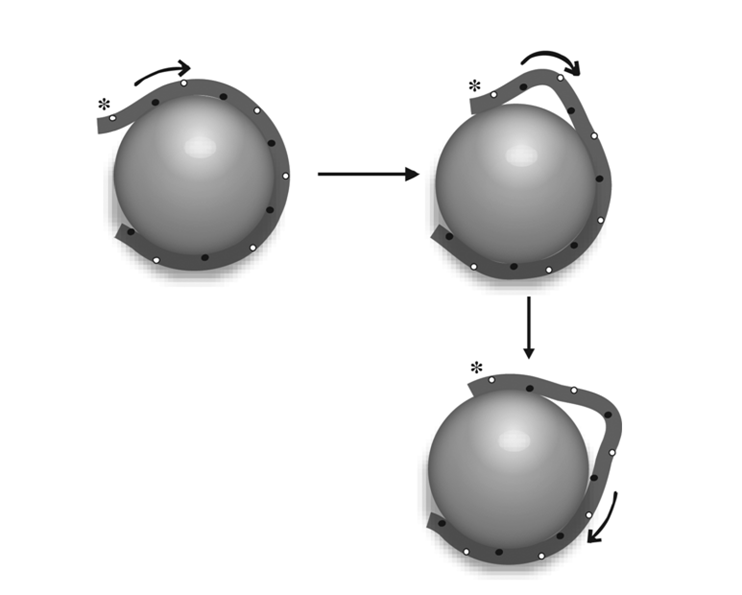
Некоторые участки генома (часто места локализации различных регуляторных последовательностей) всегда свободны от нуклеосом. Такие участки генома предпочтительно атакуются нуклеазами (участки гиперчувствительности к нуклеазам).
Билет № 6.
2. Нуклеосома как единица структурной организации хроматина. Октамер гистонов в составе нуклеосомы. Линкер и линкерные гистоны. 30 нм хроматиновая фибрилла.
Упаковка ДНК в клетке осуществляется в несколько этапов:
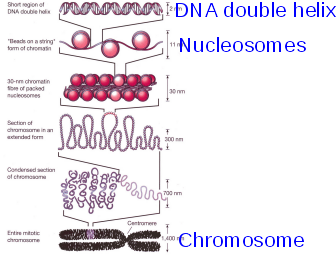
Компактизация ДНК в ядре осуществляется при посредстве сложного комплекса белков, среди которых принято выделять гистоны и негистоновые белки. Гистоны являются чрезвычайно консервативными белками. Выделяют 5 основных типов гистонов: Н1, Н2А, Н2В, Н3, Н4. Гистоны Н2А, Н2В, Н3, Н4 входят в состав минимальной нуклеосомы (так называемой “Core Particle”). По-этому их нередко называют «коровыми» гистонами. Н1 – линкерный гистон.
К открытию нуклеосом привели две группы экспериментов:
1. Электронная микроскопия препаратов хроматина в низкой ионной силе
2. Анализ продуктов расщепления хроматина стафилококковой нуклеазой
Нуклеосома является базовой структурной единицей первого уровня упаковки ДНК в хроматине. Она представляет собой белковую глобулу, или, точнее говоря некое подобие диска, на который намотан фрагмент ДНК протяженностью 146 п.н. (1,65 витка) Глобула состоит из восьми молекул гистонов: тетрамера (Н3)2-(Н4)2 и двух димеров Н2А-Н2В. Диаметр глобулы-диска составляет ~11 нм, а высота - ~ 5,7 нм.
Модульный принцип посторения нуклеосомнорго ядра отражает характер его сборки:
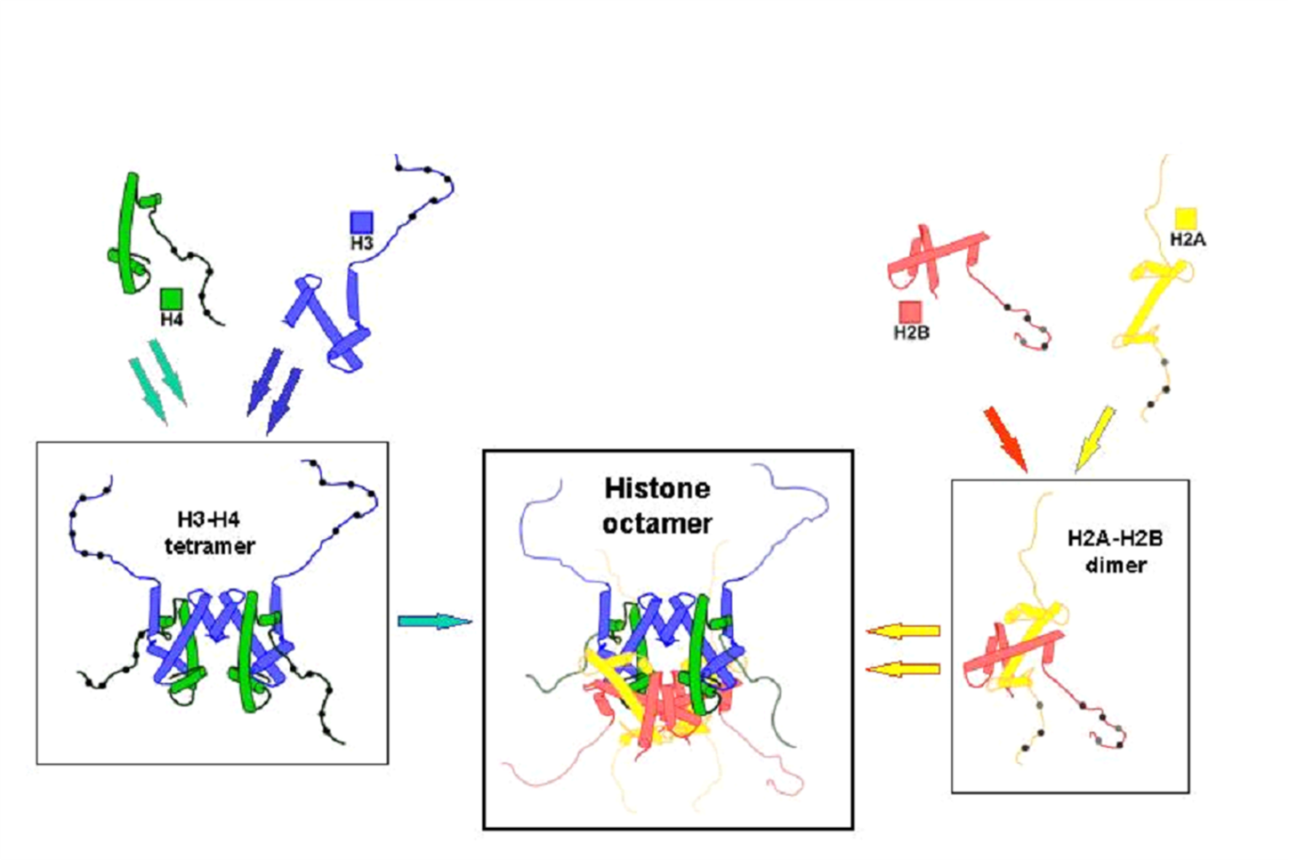
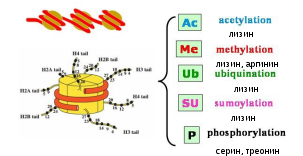 Нуклеосомные
частицы не являются вполне идентичными
благодаря модификациям гистонов и
наличию вариантных гистонов. N-концевые
фрагменты гистонов выходят за пределы
нуклеосомного ядра. На них находится
много мишеней для модификаций, имеющих
сигнальное значение. Плюс к рисунку:
полиАДФрибозилирование, которому
подвергается остаток глутаминовой
кислоты. В результате ацетилирования
Н4 гистона (лизина на N-конце) положительный
заряд лизина пропадает и связывание
ДНК не происходит.
Нуклеосомные
частицы не являются вполне идентичными
благодаря модификациям гистонов и
наличию вариантных гистонов. N-концевые
фрагменты гистонов выходят за пределы
нуклеосомного ядра. На них находится
много мишеней для модификаций, имеющих
сигнальное значение. Плюс к рисунку:
полиАДФрибозилирование, которому
подвергается остаток глутаминовой
кислоты. В результате ацетилирования
Н4 гистона (лизина на N-конце) положительный
заряд лизина пропадает и связывание
ДНК не происходит.