Материал: I. теория хим процессов

Кинетические закономерности.
–описывают, как и с какой скоростью превращаются в-ва.
Схема превращения показывает возможные пути превращения в реакционной среде; показывает реальные взаимодействия между компонентами – пути превращения – в реагирующей системе (представлена системой хим уравнений или графически:
Схема превращения необходима в предсказании и объяснении динамического изменения содержания веществ в реагирующей системе по мере протекания в ней хим. превращений.

Скорость превращения - кол-во i-го вещества, превращающегося в единицу времени в единице реакционного пространства.
Скорость реакции также определяют по изменению концентрации одного из компонентов во времени r = dC/dt – показывает связь между скоростью превращения и изменением концентрации в-ва только в закрытом сосуде, т.е. позволяет рассчитать скорость реакции в таком процессе, но не явл. ее определением.

Кинетическое уравнение или кинетическая модель реакции – зависимость скорости реакции от условий ее протекания.
r – константа р-ции, CА CВ – концентрации в-ств A, B в их стехиометрических коэффициентах
Порядок реакции: порядок реакции по i компоненту - показатель степени при концентрации i-го реагента в кинетическом уравнении, общий порядок реакции - сумма показателей степеней при концентрациях всех реагентов; для простых реакций молекулярность и порядок совпадают (несовпадение для: сложных реакций, гетерогенных реакций и для реакций с избытком)

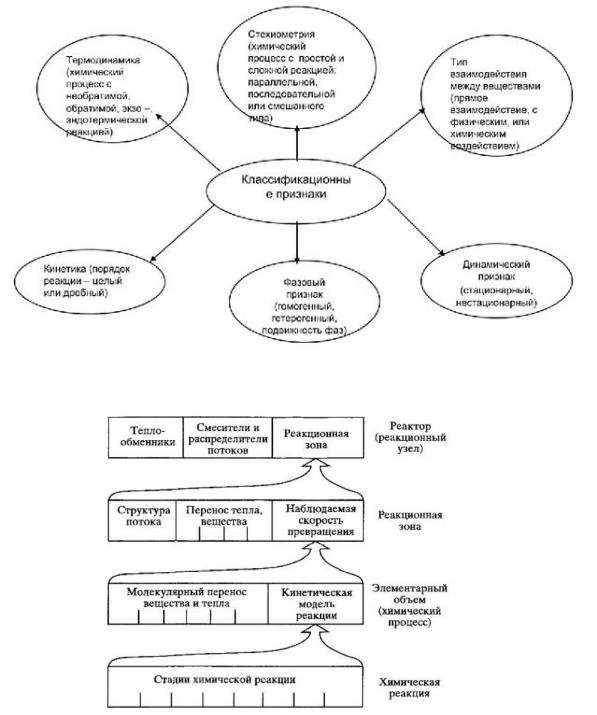
Химические процессы
Химический процесс - совокупность химической реакции и явлений переноса, таких как: диффузия и теплопроводность. На этой стадии кинетическая модель реакции является одной из составляющих процесса, причем объем, в котором рассматривается химический процесс, выбирается с такими условиями, чтобы закономерности его протекания не зависели от размера реактора. Например, это может быть процесс на отдельном зерне катализатора.
Классификация
Иерархическая структура построения математической модели в химическом реакторе