Материал: 9. Лекция. Антиоксидантная защита организма

На основе СОД и каталазы разработаны лекарственные препараты:
1)пероксинорм (препарат СОД из печени крупного рогатого скота);
2)эпурокс (СОД + каталаза);
3)редоксан (препарат СОД из эритроцитов человека).
II. линия антиоксидантной защиты (ГПО + ГР – глутатион-зависимые ферменты)
Глутатион – трипептид (глу – цис – гли). Свои восстановительные свойства глутатион проявляет за счёт SH-групп цистеина.
Глутатионпероксидаза (ГПО) не обладает строгой специфичностью. Фермент содержится во всех клетках: в мембранах и протоплазме. В активном центре содержит Se. ГПО способна разрушать гидроперекиси ЖК за счёт SH-групп глутатиона и образования дисульфидных мостиков:
|
ГПО |
|
|
RO OH + |
2G—SH |
ROH + H2O + G—S—S—G |
|
гидроперекись |
восстановленный |
оксикислота |
окисленный |
|
глутатион |
|
глутатион |
Помимо этого, ГПО обладает псевдокаталазной активностью и может разрушать пероксид водорода подобно каталазе. Необходимо отметить, что каталазную активность фермент проявляет при более низких концентрациях Н2О2, чем каталаза.
Восстановление |
окисленного |
глутатиона |
осуществляет |
глутатионредуктаза (ГР): |
|
|
|
|
ГР |
2G—SH + НАДФ+ |
|
G—S—S—G + НАДФН2 |
|||
окисленный глутатион |
(донор протонов) |
восстановленный |
|
глутатион
Источником НАДФН+Н+ является пентозофосфатный путь окисления глюкозы (печень и эритроциты). Реакцию, в которой генерируется НАДФН+Н+ катализирует фермент глюкозо-6-фосфатдегидрогеназа.
Помимо ГПО инактивацию гидроперекисей ЖК может осуществлять мембранный фермент глутатионтрансфераза, который входит в общую пероксидазную активность клетки.
III. линия антиоксидантной защиты
Церулоплазмин (ЦП) – белок плазмы крови и её основной антиоксидант. Является белком острой фазы при воспалении. В активном
центре содержит Cu2+. Другое название фермента – ферроксидаза, так как он окисляет Fe2+:
ЦП–Cu2+ + Fe2+ |
ЦП–Cu+ + Fe3+ |
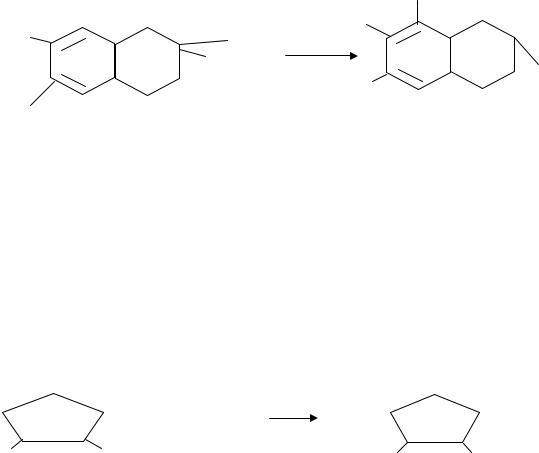
Церулоплазмин ингибирует ПОЛ на стадии разветвления цепи, так как окисляет Fe2+ - донор электронов.
В плазме церулоплазмин за счёт Cu2+ может проявлять свойства СОД. Трансферрин – плазменный белок, обеспечивающий связывание и
транспортировку Fe3+ в депо. Образуя координационные связи с атомом Fe3+, трансферрин работает по типу хелатора (комплексообразователя).
Неферментативная система регуляции ПОЛ
Природные антиоксиданты:
1. α-токоферол (витамин Е) – α-ТФ в больших количествах содержится в семенной жидкости и развивающихся клетках. Благодаря своей структуре погружается в мембрану и является мембранным антиокисдантом. В основе действия α-ТФ лежит взаимодействие с радикалами, образующимся в цепи окисления жирных кислот (RO2˙):
|
|
|
радикал вит Е (αТФ•) |
|||||
CH3 |
O |
CH |
3 |
|
О |
|||
|
|
║ |
H3С |
|
|
║ |
||
H3C |
CH3 |
|
|
|
|
|
|
|
|
|
|
|
CH3 |
||||
|
|
|
||||||
|
|
R + RO2• |
•О |
|
R |
|||
|
|
|
||||||
|
|
гидроперекисный |
|
|
+ ROOH |
|||
|
|
|
|
|
|
|||
НО |
|
радикал ЖК |
|
|
|
гидроперекись |
||
CH3 |
вит Е |
CH3 |
|
|
|
|
||
Радикалы α-ТФ˙ выталкиваются на поверхность мембраны. Два радикала способны к рекомбинации с образованием димеров нерадикальной природы. В мембранах α-ТФ сохраняется в постоянном количестве, хотя является витамином и в организме человека не синтезируется. Восстановление радикалов α-ТФ˙ осуществляет аскорбиновая кислота.
Подобно α-ТФ проявляют активность стероидные гормоны, убихиноны, витамин К и пуриновые основания.
2. аскорбиновая кислота (витамин С)
Суточная норма витамина-С составляет 70 мг.
|
O |
|
О |
||||||
O= |
|
|
|
CHOH-CH2OH + α-ТФ• |
α-ТФ+ О= |
|
|
|
CHOH-CH2OH |
|
|
|
|
|
|||||
OH |
|
|
OH |
•О |
|
ОН |
|||
|
|
|
|||||||
аскорбиновая кислота |
семидегидроаскорбиновая к-та |
||||||||
При восстановлении α-ТФ˙ аскорбиновая кислота отдаёт один из атомов водорода, переходя в семидегидроаскорбиновую кислоту (радикальная форма аскорбиновой кислоты). Это соединение является прооксидантом, так как может восстанавливать Fe3+ в Fe2+:

Две радикальные формы аскорбиновой кислоты могут взаимодействовать между собой с образованием восстановленной и полностью окисленной формы аскорбиновой кислоты.
Помимо этого, существует НАД-зависимая и глутатион-зависимая системы восстановления аскорбиновой кислоты, но их активность низкая.
3. амины
К природным антиоксидантам относятся различные амины, но они не являются истинными антиоксидантами.
Например, цистамин (SH–CH2–CH2–NH2) взаимодействует с МДА, а не со свободными радикалами, тем самым препятствуя реализации его повреждающего действия на биологически важные молекулы.
4. HS-соединения
Соединения, в состав которых входит SH-группа, являются инактиваторами гидроперекисных радикалов ЖК. К ним относятся глутатион и серосодержащие аминокислоты – метионин и цистеин. Наибольшее количество глутатиона содержится в печени и эритроцитах:
SH + ROO˙ |
ROOH |
+ |
S˙ |
||||
|
|
|
перекисный |
гидроперекись |
|
|
|
|
|
|
|
|
|||
|
|
|
радикал ЖК |
ЖК |
|
|
|
|
|
|
|
|
|
||
|
|
|
СН2 |
|
|
СН2 |
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
СН |
|
|
СН |
|||
NH2 |
|
|
COOH |
|
NH2 |
|
COOH |
цистеин |
|
|
радикал цистеина |
||||
Например, цистеин обезвреживает перекисный радикал ЖК, образуя менее агрессивное соединение гидроперекиси ЖК и радикал цистеина.
Две радикальные формы цистеина могут взаимодействолвать между собой с образованием нерадикального соединения – цистина:
S˙ |
+ |
S˙ |
|
S |
|
|
S |
|||
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
СН2 |
|
CH2 |
СН2 |
|
|
CH2 |
||||
|
|
|
|
|
|
|
|
|
|
|
СН |
CH |
|
СН |
|
CH |
|||||
NH2 |
COOH |
NH2 COOH |
NH2 COOH |
NH2 COOH |
||||||
|
|
радикалы цистеина |
|
|
цистин |
|||||
5. многоатомные спирты
Ловушками свободных радикалов являются многоатомные спирты (сорбит, ксилит, манит, а также альдегидоспирт – глюкоза). Они связывают свободные радикалы и АФК, включая гидроксильный радикал, за счёт своих ОН-групп. Например, введение 10 мл 40% раствора глюкозы обеспечивает нейтрализацию свободных R˙.

6. комплексообразователи
Комплексообразователи или хелаторы – способны образовывать координационные связи с ионами Fe2+/3+. В результате образуются комплексные соли. Примерами комплексообразователей являются ЭДТА (этилендиаминтетрауксусная кислота), ди- и трикарбоновые кислоты.
7. мембрана сама является структурным антиоксидантом. Структура мембраны такова, что она препятствует вхождению катализатора ПОЛ и контакта интактной мембраны с продуктами ПОЛ. На мембране находятся мембранные глутатион-зависимые ферменты – Глутатион-S-трансфераза; α- токоферол, восстанавливаемый витамином С.
комплексообразователь |
каталаза |
глутатион, глутатионзависимые ферменты |
||||
ē |
|
|
|
|
|
|
О2 |
О2• |
Н2О2 |
НО• |
|
ROO• |
ROOH |
КО |
|
|
|
|
|
|
блокаторы КО |
СОД |
|
многоатомные |
αТФ, |
|
|
(аллопуринол) |
|
|
спирты, |
|
вит.С |
|
|
|
|
HS-соединения |
|
|
|
Синтетические антиоксиданты
1. Существуют синтетические антирадикальные органические вещества, которые выступают в роли конкурента субстратов ПОЛ (ЖК). Обозначим их как InH.
У ингибитора связь с протоном очень лабильна и гораздо слабее, чем у α-углеродного атома в молекуле ненасыщенной ЖК. Энергия, необходимая для разрыва связи In–H равна 40 – 60 ккал/моль. Энергия, необходимая для разрыва связи С–Н в молекуле жирной кислоты равна 70 – 90 ккал/моль. Поэтому реакция InH с RO2˙ идёт легче, чем с RH.
RO2˙ + InH + RH |
ROOH + In˙ + RH |
интактная ЖК |
гидроперекись ЖК |
Образовавшийся радикал ингибитора (In˙) малоактивен и не способен инициировать новые цепи окисления жирных кислот, так как не обладает достаточным запасом энергии для разрыва связи С–Н.
Как правило, радикалы ингибиторов взаимодействуют друг с другом с
образованием нерадикальных димеров: In˙ + In˙ |
In—In |
|
Радикалы ингибиторов также могут взаимодействовать с RO2˙с образованием |
||
перекисных продуктов нерадикального характера: In˙ + RO2˙ |
ROOIn |
|
2. К синтетическим антиоксидантам относятся такие |
органические |
|
вещества, как ионол (дитретбутилфенол) и дибунол (на его основе готовят лекарственный препарат – линимент дибунола).
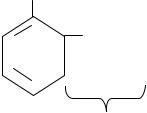
СН3 |
ОН СН3 |
экранированный гидроксил |
||||||
|
|
|
|
|
|
|
|
|
Н3С–С |
|
׀ |
|
С |
–СН3 |
(связь О-Н очень слабая) |
||
|
||||||||
|
|
|
|
|
|
|
|
|
Н3С |
|
|
СН3 |
|
||||
третбутиловая группировка
ионол
Экранированная НО-группа, которая принимает на себя атаку свободных радикалов, окружённая с двух сторон гидрофобными метильными группами, защищающими мембрану.
В организме человека ионол оказывает меньшую активность чем α- токоферол, так как строение молекулы ионола не позволяет погружаться в мембрану в отличие от α-токоферола и ионол более гидрофобен. Ионол используется для наружного применения, чаще всего при ожогах.