Материал: 9. Лекция. Антиоксидантная защита организма

АНТИОКСИДАНТНАЯ ЗАЩИТА
Повреждающие механизмы ПОЛ
Различают первичный и вторичный повреждающий механизмы ПОЛ.
I. Первичный механизм ПОЛ связан с непосредственным действием свободных радикалов или продуктов ПОЛ на клетку.
В результате действие первичного механизма идет деструкция полиненасыщенных жирных кислот (ПНЖК), входящих в состав мембранных фосфолипидов. Из «срезанных хвостов» ПНЖК, имеющих двойную связь, образуются промежуточные продукты ПОЛ: оксикислоты, этилен, кетоны, альдегиды. Из «срезанных хвостов», имеющих две и более двойные связи, образуется вторичный продукт ПОЛ – малоновый диальдегид (МДА).
МДА имеет две реакционно-способные альдегидные группы. Легко взаимодействует с белками, липидами, белково-липидными комплексами, образуя внутри- и межмолекулярные сшивки путём образования ковалентных связей по остаткам аминогрупп (радикалы лизина и концевые аминогруппы белков, аминогруппы фосфатидэтаноламинов).
Полимеризация белков, липидов и белково-липидных комплексов
Полимеризация белков, липидов и белково-липидных комплексов с образование Шиффовых оснований (третичный – конечный продукт ПОЛ). Уровень оснований Шиффа является информативным критерием, отражающим интенсивность ПОЛ.
Реакции образования внутри- и межмолекулярных сшивок можно представить следующим образом:
а) образование внутримолекулярной сшивки в молекуле белка:
|
NH2 |
O = C – H |
|
N = CH |
|
|
׀ |
|
׀ |
Pr |
+ |
CH2 |
Pr |
CH2 |
|
NH2 |
׀ |
2Н2О |
׀ |
белок |
|
O = C – H |
|
N = CH |
|
|
МДА |
связь прочная ковалентная, |
|
образовалось Шиффово основание
В результате ограничивается способность молекулы белка к изменению конформации, что приводит к утрате функции белка.

б) образование межмолекулярной сшивки между молекулами белков:
H |
H |
H |
H |
׀ |
׀ |
׀ |
׀ |
Pr-N H2 + O = C – CH2 – C = O + H2 N-Pr |
Pr-N=C-CH2-C=N-Pr |
||
|
-2H2O |
образовался димер, |
|
состоящий из 2-х остатков белковых молекул
в) образование межмолекулярных сшивок между молекулами фосфотидилэтаноламинов:
ФЭА-N H2 + O=CН–CH2–CН=O + H2 N-ФЭА |
ФЭА-N=CН-CH2-CН=N-ФЭА |
2H2O |
липофусцин |
В результате возрастает микровязкость мембраны, снижается её текучесть, что приводит к изменению функции мембраны. При старении организма этот процесс приводит к образованию ксантоматозных бляшек вследствие накопления липофусцина.
Полимерные белок-липидные комплексы стабильны и легко обнаруживаются флюориметрическими методами.
Все эти изменения приводят к нарушению функции ферментов, ассоциированных в мембране, и мембранных рецепторов. Образование комплексов делает мембрану ригидной (невосприимчивой к внешним сигналам), так как конформационные изменения белковых молекул (ферментов, транспортных систем, рецепторов), лежащие в основе биохимического ответа клетки на внешнее воздействие, осуществляются с трудом.
д) образование межмолекулярных белок-липидных сшивок:
Pr-NH2 + O=CH – CH2 – C=O + H2N-ФЭА |
Pr-N=CH-CH2-C=N-ФЭА |
2H2O
Окисление аминокислот и белков, содержащих сульфгидрильные группы
SH-группы входят в состав цистеина и метионина и выступают в качестве восстановителей, взаимодействуя со свободными радикалами:
Pr —SH + RO2˙→PrS˙ + ROOH (гидроперекись ЖК)
Образующиеся радикальные формы очень неустойчивы и легко взаимодействуют друг с другом:
PrS˙ + PrS˙ → Pr —S—S—Pr
В результате такого взаимодействия образуются неполярные ковалентные связи (дисульфидные мостики). Такой тип взаимодействия характерен для радикалов свободных аминокислот.
Радикалы аминокислот также могут подвергаться окислению молекулярным кислородом:
PrS˙ + О2 + Н+ → PrSOOH (белковые сульфопроизводные)
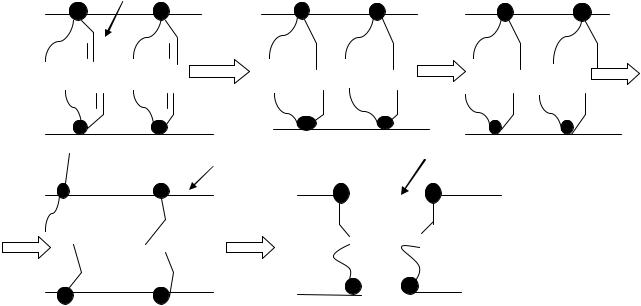
Разрыв гликозидных связей в полисахаридах
Под действием свободных радикалов осуществляется окисление и разрыв гликозидных связей, что приводит к деструкции полисахаридов.
Деструкция и разрушение нуклеопротеинов
Деструкция и разрушение нуклеопротеинов осуществляется: а) по азотистому основанию; б) по углеводному компоненту; в) по белковой части.
В результате деструкции нуклеопротеинов клетка утрачивает генетическую информацию.
II. Вторичный повреждающий механизм ПОЛ
Является следствием первичного свободно-радикального повреждения химической структуры биологически важных молекул.
1.Повышение проницаемости биомембран
Врезультате атаки НО˙ у α-углеродного атома молекулы ненасыщенной жирной кислоты, входящей в состав фосфолипидов биологических мембран, появляется перекисная группировка: сначала - ОО˙, затем - ООН.
Перекисная группа гидрофильна и выталкивается и выталкивается на поверхность мембраны вместе с жирной кислотой, на которой находится. На
поверхности мембраны имеется фермент фосфолипаза А2, которая «выстригает» радикалы ненасыщенных ЖК из фосфолипидов с образованием ОН-групп. Фосфолипиды, утратившие остатки ЖК, превращаются в лизофосфатиды. В результате в мембране появляются ОН-группы, образующие гидрофильные поры. Таким образом, мембрана превращается в «решето» и нарушается её главное свойство – избирательная проницаемость.
OH• атака
ОО• |
ОО• |
ООН |
ООН |
ОО• |
ОО• |
ООН |
ООН |
фосфолипаза А2 |
|
гидрофильная пора |
|
OOH |
ОН ОН |
OOH |
ОН ОН |
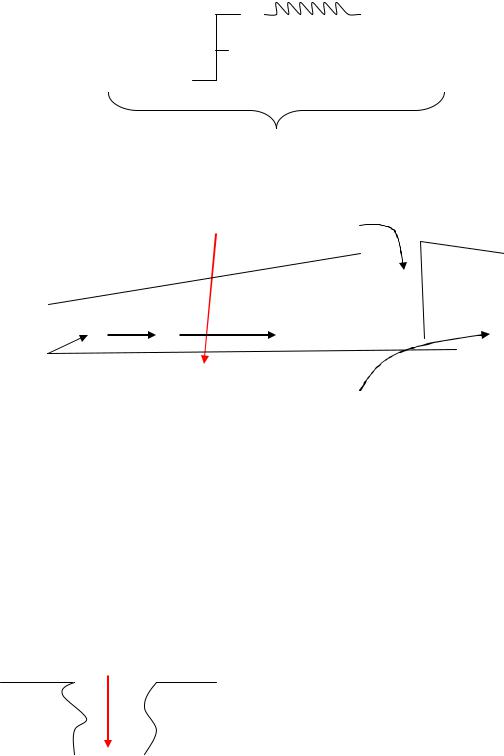
Повышение проницаемости биомембран – образование гидрофильных пор
О |
ЖК |
ОН
R – O
ФЛ
Лизофосфатид
Снижение процессов окислительного фосфорилирования.
за счёт протонов создается ΔμН |
|
|
|
|
|
|
||
|
|
Н● |
Н+ |
|
ΔμН |
|||
|
|
|
||||||
|
|
|
|
|
|
|
|
|
Н+ |
мембрана |
|
|
|
|
|
в норме |
|
|
|
|
|
|
|
|
АТФ-азный канал |
|
|
ē |
ē |
|
|
● |
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
SН2 |
через пору |
О2 |
АТФ-аза |
|||||
|
ОН- |
ОН- |
|
|
|
ОН- |
||
В физиологических условиях митохондриальная мембрана непроницаема для протонов и ΔμН+ = 0,2В, а Н+ проникают во внутреннюю митохондриальную мембрану по каналу АТФ-синтетазы. При повышении интенсивности ПОЛ и появлении в мембране гидрофильных пор, Н+ имеют возможность возвращаться в мембрану через эти поры, минуя канал АТФсинтетазы. В результате меняется величина ΔμН+. Окисление субстратов в дыхательной цепи не прекращается, но идёт в холостую, так как АТФ не синтезируется. Из-за разобщения окислительного фосфорилирования.
Кроме ионов водорода через гидрофильные каналы проходят Na+. Это приводит к нарушению симпорта аминокислот и глюкозы, которые
проникают в клетку с ионами натрия.
Na+, Ca2+
ОН НО
В результате работы Na+/Ca2+- обменника усиливается поступление в клетку ионов Са2+, при этом активируются Са-зависимые гидролазы, разрушающие собственные структуры клетки.
Также меняется активность мембранных ферментов, меняется микровязкость мембран, конформация рецепторов и нарушается их взаимодействие с лигандами.
Система регуляции ПОЛ
Существуют ферментативные и неферментативные системы регуляции ПОЛ.
Ферментативная система регуляции
Ферментативная система регуляции включает три линии защиты:
1)супероксиддисмутаза (СОД) + каталаза;
2)глутатионпероксидаза (ГПО) + глутатионредуктаза (ГР);
3)церулоплазмин + трансферин.
I. линия антиоксидантной защиты (СОД+катазаза)
СОД - содержится в клетках любого происхождения, считается мембранным ферментом. В активном центре содержится ион Сu2+ или Mn2+ (митохондриальная СОД). Существует также Zn2+-содержащая СОД. Фермент обладает высокой активностью – 1 молекула фермента способна обеспечивать дисмутацию (одновременное окисление и восстановление) 4,8 × 106 молекул супероксид-анион-радикала в минуту.
Каталитическую активность фермента обеспечивает Cu2+, выполняющий роль и акцептора, и донора электрона:
1) Е – Сu2+ + О2• |
→ Е – Сu1+ + О2 |
||
фермент |
ē |
принимает |
|
|
|
СОД переносит ē – это окисление. |
|
|
|
|
2Н+ |
2) Е – Сu1+ + О2• |
Е – Сu2+ + Н2О2 |
||
отдает |
ē |
|
в присутствии протонов, которые берутся из среды |
Дисмутация – это окисление и восстановление, происходящие |
|||
одновременно. |
|
|
|
Суммарно СОД обеспечивает образование Н2О2 и О2● |
|||
|
2Н+ |
|
|
О2• + О2• |
|
Н2О2 + О2 |
|
СОД
Каталаза – антиперекисный фермент. Фермент представляет собой олигомерный белок (тетрамер), содержащий атом Fe2+/3+. Каталаза обладает очень высокой активностью и работает при высокой концентрации пероксида водорода. Одна молекула фермента обеспечивает расщепление 5 × 106 молекул Н2О2 в минуту:
2Н2О2 |
каталаза |
2Н2О + О2 |