Материал: 7_Флуоресцентная спектросокпия белков
Флуоресцентная спектроскопия макромолекул: белки
АННОТАЦИЯ
Работа посвящена изучению флуоресцентной спектроскопии белков. Были сняты и проанализированы спектры флуоресценции белка (бычьего сывороточного альбумина), триптофана и тирозина, растворённых в калий-фосфотном буфере и растворе гидроксида натрия. Спектры флуоресценции БСА и триптофана схожи между собой. Триптофан и БСА проявил pH зависимость.
ВВЕДЕНИЕ
Люминесценция - испускание фотонов из электронно-возбужденных состояний - делится на два типа в зависимости от природы основного и возбужденного состояний.
Флуоресценция - это испускание, происходящее при возвращении спаренного электрона на более низкую орбиталь. Такие переходы квантовомеханически "разрешены", а типичные величины скоростей испускания для них ~108 с-1. Высокие значения скоростей испускания приводят к временам затухания флуоресценции~10-8 с (10 нс). Квантовый выход флуоресценции — это отношение числа испущенных фотонов к числу поглощенных.
Фосфоресценция - это испускание, происходящее при переходе между состояниями различной мультиплетности, как правило, из возбужденного триплетного состояния в синглетное основное. Такие переходы не разрешены, и константы скорости испускания малы. Типичный диапазон времени затухания фосфоресценции — от миллисекунд до секунд, что главным образом зависит от вклада других процессов дезактивации.
Флуоресцентные свойства объекта обычно характеризуют спектрами испускания и возбуждения. Спектр испускания флуоресценции — это зависимость интенсивности флуоресценции от длины волны (в нанометрах) или волнового числа (в см-1). Спектры испускания зависят как от химической структуры флуорофора, так и от растворителя, в котором он растворен. Спектр возбуждения - это зависимость интенсивности люминесценции при определенной длине волны от длины волны возбуждения. Для большинства флуорофоров квантовые выходы и спектры испускания не зависят от длины волны возбуждающего света. Следовательно, спектр возбуждения флуорофора обычно совпадает с его спектром поглощения. Даже при идеальных условиях для такого совпадения необходимо присутствие единственного флуорофора, а также отсутствие осложняющих факторов, таких, как нелинейность, связанная с большой оптической плотностью образца.
Поглощение и испускание света хорошо иллюстрирует диаграмма уровней энергии, предложенная Яблонским. Основное, первое и второе электронные состояния обозначают S0, S, и S2 соответственно. Каждый из этих уровней энергии может состоять из множества колебательных энергетических уровней, обозначаемых 0, 1, 2 и т. д. Переходы между различными электронными уровнями обозначают вертикальными линиями. Такое представление используется, чтобы наглядно показать мгновенную природу поглощения света. Этот процесс происходит примерно за 10-15 с, время, слишком короткое для заметного смещения ядер (принцип Франка - Кондона). Из-за большой разности энергий между уровнями S0 и S1 ни у каких флуорофоров состояние S1 не может быть заселено термическим путем. За поглощением света обычно следует несколько других процессов. Возбуждение флуорофора, как правило, происходит до некоторого высшего колебательного уровня состояний (S1 либо S2). За некоторыми редкими исключениями, для молекул в конденсированной фазе характерна быстрая релаксация на самый нижний колебательный уровень состояния S1. Этот процесс называется внутренней конверсией и происходит большей частью за 10-12 с. Поскольку типичные времена затухания флуоресценции близки к 10-8 с, внутренняя конверсия обычно полностью заканчивается до процесса испускания. Следовательно, испускание флуоресценции чаще всего осуществляется из термически равновесного возбужденного состояния. Термическое равновесие достигается за время порядка 10-12 с. Молекулы в состоянии S1 могут также подвергаться конверсии в первое триплетное состояние Т1. Испускание из Т1 (фосфоресценция), обычно сдвинуто в сторону больших длин волн по сравнению с флуоресценцией. Переход из S1 в Т1 называется интеркомбинационной конверсией.
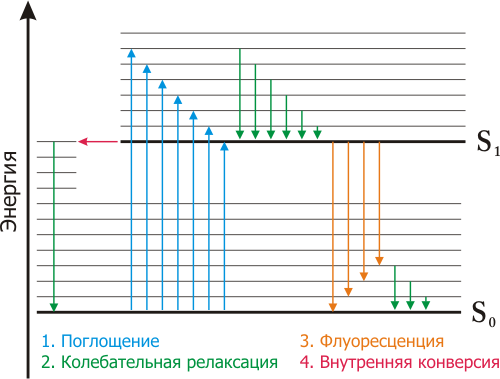
Рис. 1 - диаграмма Яблонского
Флуоресценция молекул имеет следующие характеристики:
1. Стоксов сдвиг
Как правило, всегда наблюдается сдвиг испускания относительно поглощения в сторону больших длин волн, т.е. потеря энергии (исключение — атомы в газовой фазе). Потери энергии между возбуждением и испусканием неизменно наблюдаются для флуоресцирующих молекул в растворах. Одной из основных причин возникновения стоксова сдвига является быстрая релаксация на нижний колебательный уровень состояния S1. К тому же обычно происходит переход на возбужденные колебательные уровни состояния S0, что приводит к дополнительной потере колебательной энергии. Вдобавок к этому стоксов сдвиг может быть еще более увеличен благодаря влияниям растворителя на флуорофоры и реакциям в возбужденных состояниях.
2. Независимость спектра испускания от длины волны возбуждения
Спектр испускания флуоресценции обычно не зависит от длины волны возбуждения. При возбуждении на высшие электронные и колебательные уровни избыток энергии быстро расходуется, переводя флуорофор на самый нижний колебательный уровень состояния S1. Эта релаксации происходит за время порядка 10-12 с и является результатом сильного перекрывания множества состояний с примерно равными энергиями. Благодаря такой быстрой релаксации длина волны возбуждения обычно не влияет на спектр испускания. Кроме того, возбуждение на красном крае спектра поглощения часто ведет к сдвигу флуоресценции в длинноволновую область. Этот сдвиг обусловлен тем, что возбуждение на красном краю спектра избирательно возможно для тех флуорофоров, которые наиболее сильно взаимодействуют с растворителем.
3. Правило зеркальной симметрии
Обычно спектр испускания флуоресценции представляет собой зеркальное отражение спектра поглощения, точнее, того поглощения, которое соответствует переходу из S0 в S1. Для многих молекул различное распределение электронов в состояниях S0 и S1 существенно не влияет на эти уровни энергии. Согласно принципу Франка - Кондона, все электронные переходы происходят без изменения межъядерного расстояния. В результате, если данная вероятность перехода (фактор Франка - Кондона) между нулевым и вторым колебательными уровнями максимальна при поглощении, соответствующий переход будет наиболее вероятен также и в испускании.
Факторы, влияющие на спектры испускания белков:
Трехмерная структура
Связывание белков с субстратами и другими макромолекулами
Вся флуоресценция белка обусловлена наличием остатков триптофана, тирозина и фенилаланина, если известно, что белок не содержит особых флуоресцирующих компонентов.
При уменьшении полярности растворителя λmax в спектре флуоресценции триптофана смещается в область более коротких длин волн и интенсивность при λmax возрастает:
а) Если λmax смещена в область более коротких длин волн, когда белок находится в полярном растворителе, триптофан должен находиться внутри молекулы в неполярном окружении;
б) Если λmax смещена в область более коротких длин волн, когда белок находится в неполярной среде, то либо триптофан расположен на поверхности белка, либо он попадает на поверхность в результате конформационного перехода, индуцированного растворителем.
Если вещество, известное как тушитель (т. е. оно тушит флуоресценцию свободной аминокислоты), например, йодид, нитрат или ионы цезия, тушит флуоресценцию триптофана или тирозина, то эти аминокислоты должны быть на поверхности белка. Если тушения не происходит, этому имеется несколько причин:
а) Аминокислота находится внутри молекулы;
б) Аминокислота находится в полости, размеры которой слишком малы, чтобы туда вошел тушитель;
в) Аминокислота находится в сильно заряженном участке, и заряд может отталкивать тушитель.
Флуоресцентная спектроскопия - эффективный метод исследования динамических процессов в растворах, представляющих интерес для биологов. Такая возможность связана в первую очередь с временем жизни возбужденных состояний. Вследствие принципа Франка - Кондона абсорбционная спектроскопия может дать информацию только об усредненных характеристиках основного состояния молекул, поглотивших свет. Поскольку только те молекулы растворителя, которые непосредственно соседствуют с поглощающими частицами, будут влиять на их спектр поглощения, абсорбционная спектроскопия может дать информацию лишь о некоторой средней сольватной оболочке растворителя, соседствующей с хромофором, и не отражает молекулярную динамику. В противоположность этому параметры флуоресцентной спектроскопии являются чувствительными функциями всех процессов, протекающих за время жизни возбужденного состояния, причем в этих процессах могут участвовать молекулы, находящиеся в момент возбуждения на расстояниях до 100 А от флуорофора. Хотя может показаться, что 10 нс - слишком короткий промежуток времени, фактически это большое время по сравнению с временем движения малых молекул в жидком растворе. Вращательная диффузия связанных с белками и мембранами флуорофоров также укладывается в этот временной диапазон.
Материалы и методы
Измерение флуоресценции исследуемых растворов осуществляется с помощью спектрофлуориметра. Прибор снабжён монохроматорами для выделения отдельной длины волны как возбуждающего, так и испускаемого света. Флуоресценция попадает на фотоумножители и затем количественно измеряется с помощью соответствующих электронных устройств. Схема использованной установки представлена на рисунке 2.
1

Были приготовлены растворы триптофана (210-5 М), тирозина (10-4 М), БСА (10-5 М) в двух средах – растворе NaOH и фосфатном буфере. Условия регистрации флуоресценции растворов: диапазон съемки – 285-450 нм для возб = 275 нм, 305-450 нм для возб = 295 нм, шаг -1 нм, спектральная ширина щелей – 4 нм.
РЕЗУЛЬТАТЫ
Были сняты спектры флуоресценции триптофана (210-5 М), тирозина (10-4 М), белка (10-5 М) при двух длинах волн возбуждения – 275 и 295 нм и в двух средах – растворе NaOH и фосфатном буфере.
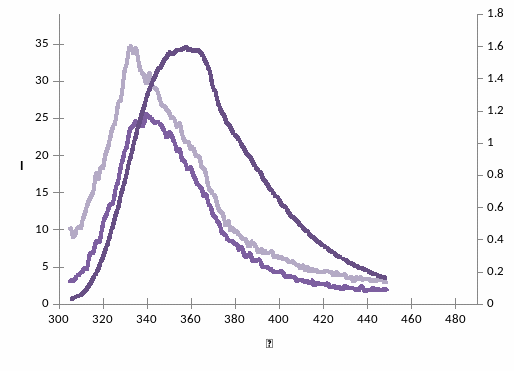
Рис. 2 – спектры флуоресценции растворов NAOH при длине волны возбуждения возб = 295 нм
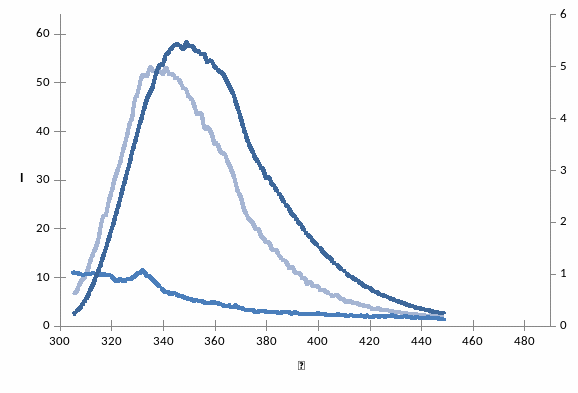
Рис. 3 – спектры флуоресценции растворов, приготовленных в фосфатном буфере при длине волны возбуждения возб = 295 нм
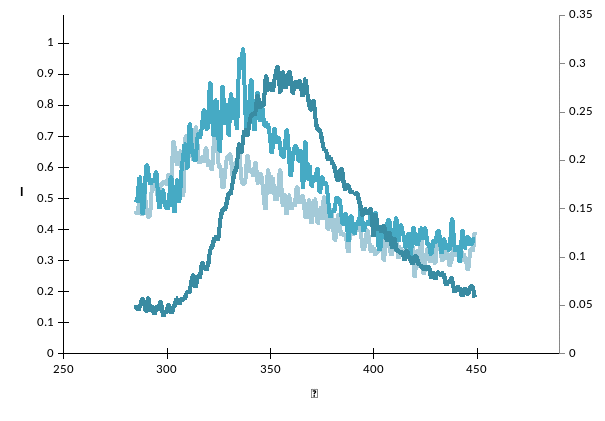
Рис. 4 – спектры флуоресценции растворов NAOH при длине волны возбуждения возб = 275 нм
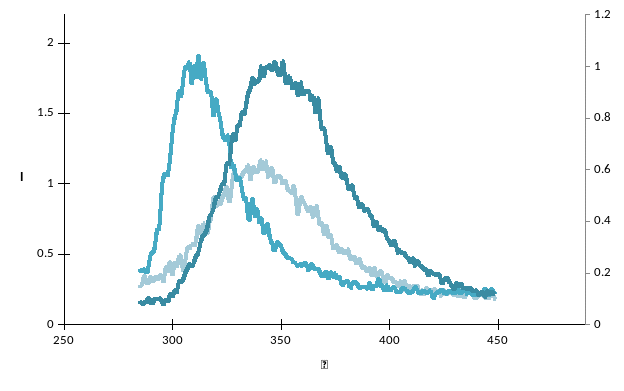
Рис. 5 – спектры флуоресценции растворов, приготовленных в фосфатном буфере при длине волны возбуждения возб = 275 нм
Таблица 1 — максимумы интенсивности флуоресценции триптофана (210-5 М), тирозина (10-4 М), белка (10-5 М) при двух длинах волн возбуждения – 275 и 295 нм и в двух средах – растворе NaOH и фосфатном буфере.
№ |
Образец |
Растворитель |
Спектр испускания |
||
возб, нм |
max, нм |
Imax, о.е |
|||
1 |
Триптофан |
NaOH |
275 |
354 |
0,912907 |
2 |
295 |
358 |
34,5374 |
||
3 |
Буфер |
275 |
351 |
1,86752 |
|
4 |
295 |
349 |
58,2136 |
||
5 |
Тирозин |
NaOH |
275 |
337 |
0,313376 |
6 |
295 |
340 |
1,17796 |
||
7 |
Буфер |
275 |
312 |
1,04004 |
|
8 |
295 |
332 |
1,06641 |
||
9 |
БСА |
NaOH |
275 |
314 |
0,234086 |
10 |
295 |
332 |
1,58962 |
||
11 |
Буфер |
275 |
341 |
0,635225 |
|
12 |
295 |
335 |
4,9806 |
||
ВЫВОДЫ
Спектры флуоресценции БСА и триптофана схожи между собой. Известно, что флуоресценция белка определяется в основном люминесценцией триптофана, поэтому формы спектров практически не отличаются.
Триптофан проявил pH зависимость. Возможно, это происходит ввиду повышения диссоциации фенольного кольца, ввиду чего произошло перераспределение зарядов на молекуле, что повлекло за собой уменьшение флуоресцентных свойств. В случае с БСА также наблюдается pH зависимость. Это может быть объяснено чувствительностью триптофана к pH т.к. именно флуоресценция триптофана оказывает основное влияние на флуоресцентные свойства белка.
Значение максимума интенсивности флуоресценции для раствора тирозина в буфере и гидроксиде натрия и раствора белка в гидроксиде натрия смещено в коротковолновую область. Это объясняется наличием дополнительного источника излучения, а именно комбинационным рассеянием света.