Материал: 6. Лекция. Обмен холестерола, желчных кислот и кетоновых тел
Третья стадия характеризуется циклизацией сквалена под действием циклазы в ланостерин. Затем в ходе двадцати последовательных реакций ланостерин превращается в ХС.
Регуляция биосинтеза ХС
Регуляторным ферментом биосинтеза ХС является ГМГ-КоА-редуктаза.
Различают метаболическую и гормональную регуляцию.
Метаболическая регуляция
Скорость синтеза ГМГ-КоА-редуктазы в печени подвержена суточным колебаниям. Максимум приходиться на полночь, минимум – на утренние часы.
Впечени скорость синтеза ХС регулируется по механизму отрицательной обратной связи. Это значит, что ХС как конечный продукт синтеза ингибирует активность ГМГ-КоА-редуктазы. Помимо этого, пищевой ХС угнетает синтез эндогенного ХС de novo.
Вэнтероцитах хенодезоксихолевая кислота также подавляет синтез эндогенного ХСа (de novo), поэтому можно считать, что в энтероцитах синтез ХС регулируется преимущественно концентрацией жёлчных кислот.
Гормональная регуляция
На активность ГМГ-КоА-редуктазы влияют гормоны: инсулин, Т3 и Т4,
повышающие активность фермента; глюкагон и глюкокортикоиды – снижают активность. Гормональная регуляция осуществляется по механизму ковалентной модификации – фосфорилирование/дефосфорилирование. Регуляторный фермент
– ГМГ-КоА-редуктаза активен в дефосфорилированной форме.
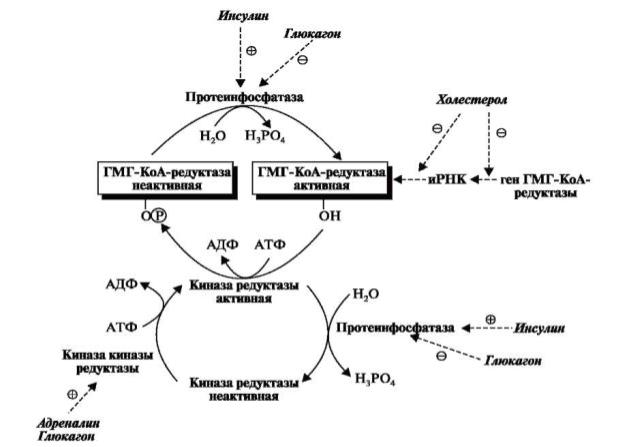
Инсулин, Т3 и Т4 активируют протеинфосфатазу, которая катализирует дефосфорилирование ГМГ-КоА-редуктазы и, таким образом, стимулирует синтез ХС. Кроме того, инсулин поддерживает ГМГ-КоА-редуктазу в дефосфорилированной форме за счёт перевода киназы ГМГ-КоА-редуктазы в дефосфорилированную, то есть неактивную форму.
Глюкагон активирует протеинкиназу, которая катализирует фосфорилирование белков, в том числе и ингибитора протеинфосфатазы, переводя его в активную
форму. В результате блокируется активность регулируемого фермента ГМГ-КоА-
редуктазы и, как следствие, синтез ХС.
Кроме того, глюкагон поддерживает ГМГ-КоА-редуктазу в фосфорилированной неактивной форме с помощью киназы ГМГ-КоА-редуктазы, которая активна в фосфорилированной форме.
Регуляция синтеза ХС
Катаболизм ХС
В клетках животных тканей нет ферментов, которые могли бы катализировать окисление ХС с разрывом стеринового кольца, не говоря уже об окислении до СО2 и Н2О. И, тем не менее, ХС в организме подвергается катаболизму с образованием различных продуктов, содержащих неразорванное стериновое кольцо, и отличающихся друг от друга не только химическими, но и физиологическими особенностями. В надпочечниках и плаценте из ХС образуются кортикоидные гормоны. В половых железах из ХС синтезируются стероидные гормоны. В печени катаболизм ХС протекает с образованием жёлчных кислот.
Образование жёлчных кислот
Первичные жёлчные кислоты образуются из ХС в печени. Среди жёлчных кислот в количественном отношении преобладает холевая кислота. Холевая и дезоксихолевая кислоты имеют общего предшественника, образующегося из ХС
–7-α-гидроксихолестерол.
Первым этапом образования жёлчных кислот является 7-α-гидроксилирование.
Реакция является скорость-лимитирующим звеном всего процесса. Реакция протекает с участием О2, НАДФН++Н+, цитохрома Р-450 и витамина С,
катализирует процесс фермент – 7-α-гидроксилаза.
7-α-гидроксилаза – это монооксигеназа, как и остальные ферменты последующих стадий гидроксилирования. При недостатке витамина С образование жёлчных кислот на стадии 7-α-гидроксилирования тормозится, что приводит к накоплению ХСа и развитию атеросклероза.
Путь биосинтеза жёлчных кислот разветвляется на ранней стадии. Одна из ветвей приводит к образованию холевой кислоты, имеющей дополнительную ОН-группу в двенадцатом положении, другая – к образованию хенодезоксихолевой кислоты
(при отсутствии ОН-группы в двенадцатом положении).
Холевая и хенодезоксихолевая – это первичные жёлчные кислоты. По сравнению с ХС они обладают выраженными гидрофильными свойствами. В норме жёлчные кислоты поступают в состав желчи в виде конъюгатов с глицином и таурином. В
основе конъюгации лежит образование пептидной связи между НОО С-группой жёлчной кислоты и NH2-группой глицина (NH2 – CH2 – COOH) или таурина (NH2
–CH2 – CH2 –SO3H).
Врезультате конъюгации образуются гликохолевая, таурохолевая,
гликохенодезоксихолевая, таурохенодезоксихолевая кислоты. Конъюгации подвергается 90% жёлчных кислот. Конъюгированные жёлчные кислоты являются более гидрофильными соединениями, чем соли жёлчных кислот. У
человека соотношение конъюгатов жёлчных кислот с глицином и таурином в норме составляет 3/1, так как количество таурина ограничено.
Поскольку жёлчь содержит значительное количество ионов Na и К и имеет щелочную реакцию, то принято рассматривать жёлчные кислоты и их конъюгаты в форме солей, откуда и возникает термин «жёлчные соли».
Затем, соли жёлчных кислот выделяются в составе желчи из жёлчного пузыря в просвет двенадцатиперстной кишки. Выполнив свою функцию, около 95% солей жёлчных кислот в подвздошной кишке всасываются и через воротную вену возвращаются в печень и повторно используются в эмульгировании жиров. Этот путь жёлчных кислот называют энтерогепатической циркуляцией. Каждая молекула жёлчной кислоты проходит этот путь 6-8 раз.
В кишечнике часть первичных жёлчных кислот (≈5%, в том числе и конъюгированные) под действием кишечных бактерий подвергаются деконъюгации и 7-α-дегидроксилированию, в результате чего образуются вторичные жёлчные кислоты: из холевой – дезоксихолевая, из хенодезоксихолевой – литохолевая.
Дезоксихолевая кислота всасывается в кишечнике, попадает в печень и там превращается в первичную – холевую кислоту. Литохолевая кислота плохо растворима в воде и не всасывается в кишечнике, а выводится в составе фекалий.
За сутки из организма выводится 500-600 мг жёлчных кислот. Путь выведения жёлчных кислот является и основным путём выведения ХСа из организма.
Гормональная регуляция
Тиреоидные гормоны индуцируют синтез 7-α-гидроксилазы и контролируют его активность. Эстрогены в детородном возрасте репрессируют синтез 7-α-
гидроксилазы. Такое влияние эстрогенов на синтез жёлчных кислот объясняет тот факт, что у женщин после менопаузы желчнокаменная болезнь встречается в
3-4 раза чаще, чем у мужчин. Гормональная регуляция осуществляется с помощью ковалентной модификации по механизму фосфорилирование/дефосфори-лирование. 7-α-гидроксилаза активна в фосфорилированной форме. Процесс фосфорилирования и дефосфорилирования контролируют тиреоидные гормоны через тирозинкиназу и тирозинфосфатазу, а
те, в свою очередь, активируют протенкиназу и протенфосфатазу.
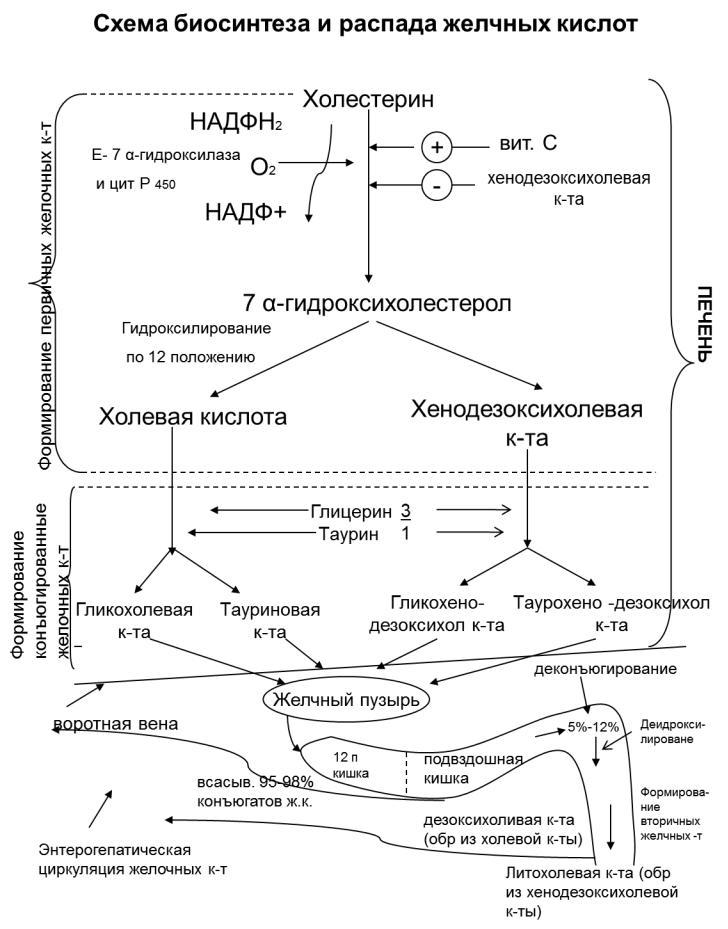
Образование и распад жёлчных кислот