Материал: 6. Лекция. Обмен холестерола, желчных кислот и кетоновых тел

ОБМЕН ХС И ЖЁЛЧНЫХ КИСЛОТ
ХС относится к группе стероидов. Эти соединения имеют в своей структуре циклопентанпергидрофенантреновое ядро. Среди стероидов выделяют соединения стеринов (или стеролов). Характерным для них является наличие НО-
группы в третьем положении и боковой цепи в семнадцатом положении.
ХС (холестерол) – производное стеринов, представляющее собой мононенасыщенный спирт (рис. 18).
Кольцевая структура ХСа отличается значительной жёсткостью, но боковая цепь довольно подвижна. Наличие в третьем положении кольца А ОН-группы позволяет отнести ХС к полярным липидам, способным образовывать сложные эфиры с жирными кислотами.
Образование эфиров ХСа
1. В цитоплазме клеток, в эндоплазматическом ретикулуме происходит этерификация ХСа под действием ацилхолестеролацилтрансферазы (АХАТ).
Этерификация ХСа в эндоплазматическом ретикулуме
2. В плазме крови этерификация ХСа, входящего в состав ЛПВП происходит под действием лецитинхолестеролацилтрансферазы (ЛХАТ). ЛХАТ синтезируется в гепатоцитах, а затем секретируется в кровоток, где образует прочный комплекс с ЛПВП. Источником жирной кислоты для этерификации является лецитин, входящий в состав ЛПВП. В молекуле лецитина ЛХАТ отщепляет молекулу ненасыщенной жирной кислоты во втором положении и присоединяет её к НО-группе ХС. В результате образуется сложный эфир ХСа и жирной кислоты и лизолецитин.
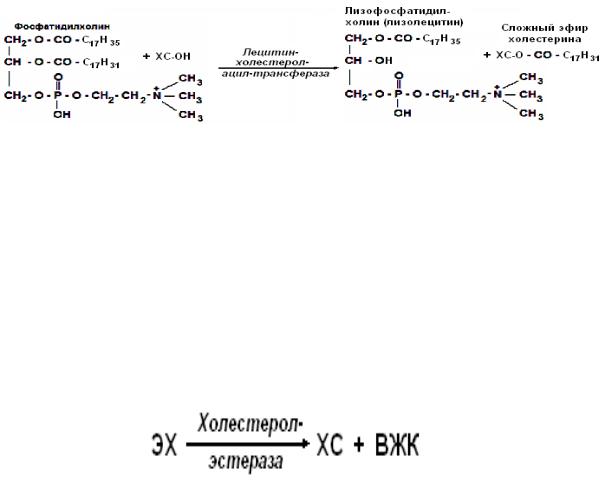
ЭХС преобладают в крови и находятся, в основном, в составе ЛПВП, в
лейкоцитах, миндалинах и лимфоузлах, а также в цитоплазме клеток надпочечников и гепатоцитов. Небольшое количество эфиров ХСа содержит эпидермис, жировая ткань и клетки кишечника (около 10% от общего содержания ХСа). Следовые количества эфиров ХСа находятся в нервной ткани. При патологических состояниях эфиры ХСа накапливаются в нервной ткани.
Эфиры ХСа рассматриваются как запасная форма ХСа. В лизосомах клеток имеется фермент холестеролэстераза, который в зависимости от условий и потребности клетки расщепляет эфиры ХСа на ХС и жирные кислоты.
С возрастом в плазме крови, коже, соединительной и жировой тканях, во внутренней оболочке сосудов происходит увеличение содержания ХСа,
преимущественно за счёт накопления его эфиров, образованных с олеиновой и линолевой жирными кислотами.
В целом, в организме млекопитающих свободный ХС преобладает над эфирами ХСа. Свободный ХС локализован в клеточных мембранах, миелиновых оболочках, эритроцитах, адипоцитах, желчи, в клетках слизистой кишечника (80-
90% свободного ХСа). В клетке свободный ХС распределяется следующим образом:
больше всего – в мембранах
меньше – в митохондриях
еще меньше – в ядрах
и меньше всего – в клеточной жидкости.
Втеле взрослого человека содержится около 210-250 г ХС. Метаболизм ХС в различных тканях протекает с различной скоростью, в связи с чем, выделяют несколько пулов ХСа:
1. Быстро обменивающийся пул (в течение 30 суток). Это ХС печени, эпителия кишечника, плазмы (в составе ЛП) и других паренхиматозных органов. Этот пул составляет около 30 грамм из общего количества ХСа.
2. Медленно обменивающийся пул (в течение нескольких месяцев). Это ХС жировой ткани. На него приходится около 50 г от общего количества ХС.
3. Очень медленно обменивающийся пул (в течение года). Это – ХС, который содержится в головном и спинном мозге, в соединительной ткани. На него приходится 60 г из 140 г общего ХС.
Особое значение имеет быстро обменивающийся пул ХС:
1.ХС печени окисляется в жёлчные кислоты (в сутки 0,5 г);
2.синтез стероидных гормонов (0,1 г в сутки);
3.избыток ХС удаляется в виде вторичных жёлчных кислот (0,5 г в сутки) с фекалиями;
4.ХС удаляется со слущенным эпителием кишечника, кожи и секретом сальных желёз (0,1 г в сутки).
Итак, ежесуточно расход ХС составляет 1,2 г. Восполнение фонда ХС идёт за
счёт:
1)синтеза de novo (0,8 г в сутки);
2)экзогенного ХС, поступающего с пищей (0,4 г в сутки).
Вплазме крови взрослого человека уровень ХСа составляет 3,9 – 6,0 ммоль/л (их них 70% - эфиры ХСа (норма = 2,5-4,9 ммоль/л) и 30% свободный ХС (норма =
1,4-1,6 ммоль/л)). С возрастом уровень ХС повышается.
У новорождённых уровень ХС составляет 1,9 ммоль/л. У детей ХС необходим для клеточного деления и построения новых цитоплазматических мембран.
Нарушение процесса поступления ХС нарушает психическое и физическое развитие ребёнка.
С возрастом замедляется процесс окисления и выведения ХС, что сопровождается накоплением ХС в мембранах и изменяет физико-химических свойств последних. Такое явление получило название «холестериноз».
Атеросклероз можно рассматривать как его осложнение.
У пожилых людей уровень ХС составляет 6,0 ммоль/л и выше. Увеличение уровня ХС выше 6,7 ммоль/л называется гиперхолестеролемией, а уменьшение ниже 3,9 ммоль/л гипохолестеролемией. Гиперхолестеролемия является фактором риска развития ИБС и других заболеваниях, связанных с атеросклерозом. Отложение ХС на стенках сосудов приводит к атеросклерозу, а в жёлчном пузыре к образованию жёлчных камней.
Биосинтез ХС
Способностью синтезировать ХС обладают все клетки животных и человека, за исключением зрелых эритроцитов. В значительных количествах ХС синтезируется в печени (50-70%), в стенке слизистой тонкой кишки (15-
20%) и коже (около 5%). Гепатоциты и клетки слизистой тонкой кишки синтезируют ХС не только для своих нужд, но и на экспорт. Биосинтез ХС можно разделить на 3 стадии:
1)биосинтез мевалоновой кислоты;
2)образование из мевалоната сквалена;
3)циклизация сквалена и образование ХС.
Биосинтез мевалоновой кислоты
Реакция протекает в цитоплазме, в аэробных условиях, после приёма пищи,
богатой углеводами. Основным субстратом биосинтеза ХС является ацетил-КоА,
преимущественно углеводного происхождения и ацетил-КоА, образованный из аминокислот.
3,5-дигидрокси, 3-метилвалериановая (мевалоновая кислота)
Ацетил-КоА попадает в цитоплазму при помощи цитратного челночного механизма. В биосинтезе мевалоновой кислоты имеются реакции восстановления, что требует присутствия НАДФН++Н+. Источниками последнего являются: пентозофосфатный путь окисления глюкозы, окислительное декарбоксилирование малата в пируват, декарбоксилирование изоцитрата в α-
кетоглутарат. Далее протекают следующие реакции.
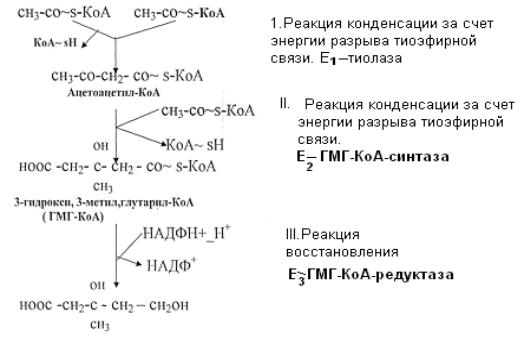
1.Реакция конденсации двух молекул ацетил-КоА за счёт энергии разрыва тиоэфирной связи с образованием ацетоацетил-КоА. Катализирует процесс фермент – тиолаза.
2.Реакция конденсации ацетоацетил-КоА с ацетил-КоА. Источником энергии также служит разрыв тиоэфирной связи. Реакция протекает с участием воды,
катализирует процесс фермент – ГМГ-КоА-синтаза. В результате образуется 3-
гидрокси-3-метилглутарил-КоА (ГМГ-КоА).
3. Реакция восстановления ГМГ-КоА в мевалоновую кислоту. Источником протонов является НАДФН++Н+. Катализирует реакцию ГМГ-КоА-редуктаза.
Второй стадией биосинтеза ХСа является образование сквалена. Процесс протекает с затратой 3-х молекул АТФ.