Материал: 3995
36
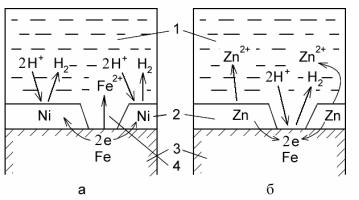
Рис.8. Схема коррозии металла в кислом растворе при нарушении металлических покрытий: а - катодного, б - анодного;
1– раствор, 2 – покрытие, 3 – основной металл, 4 – дефект в покрытии
Анодное покрытие, даже при его повреждении, продолжает защищать металл изделия (рис. 8б).
Гальванические покрытия
Гальванические покрытия – это покрытия изделий из металлических и неметаллических материалов, получаемые в процессе электролитического осаждения металла на их поверхности, т.е. электролиза. Хромирование и никелирование фурнитуры в мебельной промышленности, в лесном и автомобильном хозяйствах, в лесоинженерном деле проводят с помощью электролиза, получая противокоррозионные гальванические покрытия для защиты оборудования, механизмов и транспорта от коррозионных разрушений.
Электролиз представляет собой процесс раздельного окисления и восстановления на электродах, протекающий под действием постоянного электрического тока. Электролитические процессы осуществляются в электролизерах или электролитических ваннах. Изделие, на которое необходимо нанести слой защитного металлического покрытия подключают к катоду, а анодом является графитовый электрод или электрод из того, металла, который служит покрытием. Катодная и анодная пластины помещаются в соответствующий раствор электролита, содержащий ионы металла, служащего защитным покрытием.
Например, при нанесении цинкового покрытия на изделие из стали, протекают следующие процессы по схеме:
37
Диссоциации электролита ZnSO4 Zn2+ + SO42– Миграция катионов (Zn2+) к катоду, а анионов (SO42–) к аноду
КАТОД (-): |
АНОД графитовый (+): |
Zn2+ |
SO42– |
на катоде - реакция восстановления |
на аноде – реакция окисления воды |
2 Zn2+ + 2e = Zn0 |
2H2O – 4e = O2 + 4H+ |
металл (Zn)осаждается на поверхности электрода
Суммарный процесс электролиза выражается следующим уравнением:
электролиз
ZnSO4 2H2O Zn0 O2 2H2 SO4 .
Законы М. Фарадея, установленные в 1833 г. позволяют рассчитывать массу осаждаемого металла, время электролиза и необходимую силу.
I закон Фарадея
Масса выделяющегося на электроде вещества пропорциональна количеству электричества, протекающего через электролизер.
m K I t = K Q |
(14) |
где m – масса вещества на электроде, г; I - сила тока, А; t |
– время протекания |
тока через электролизер, с; Q = I t – количество электричества; K – электрохимический эквивалент, равный отношению химического эквивалента к числу Фарадея (F 96500 Кл/моль).
II закон Фарадея
Для выделения на электроде 1 моль любого вещества необходимо затратить одно и то же количество электричества, равное F=96500 Кл/моль – постоянная Фарадея.
Обобщенный вид первого и второго законов Фарадея выглядит так:
m |
Э |
I t |
(15) |
|
F |
||||
|
|
|
Определение толщины покрытия
Толщина гальванопокрытия во многих случаях является решающим признаком качества покрытия, технические и экономические требования к которому установлены ГОСТ 9.302-88. Следует учитывать, что толщина покрытия на изделиях, особенно профилированных, неодинакова в различных точках поверхности, поэтому необходимо измерение не только средней толщины покрытия, но и минимальной толщины на определенных участках детали.
Методы контроля толщины покрытий по степени воздействия на объект подразделяют на две группы: разрушающие и неразрушающие.
38
Разрушающие методы контроля толщины покрытий приводят к разрушению целостности не только покрытия, но и самого изделия. Они делятся на химические и физические. К химическим методам относят метод стравливания, методы капли и струи, кулонометрический метод.
Метод стравливания является наиболее простым и удобным, и позволяет определять среднюю толщину нанесенного покрытия по изменению массы при растворении покрытия в травильном электролите, который не действует на металл основы.
В методе капли травильный раствор (HCl, H2SO4) наносят по каплям на поверхность покрытия из капельницы с внутренним диаметром капилляра 1,5- 2,0 мм и выдерживают в течение определенных промежутков времени до полного растворения покрытия. Метод капли позволяет определять локальную толщину покрытия на любом участке поверхности изделия, однако имеет высокую относительную погрешность до 30 %.
Методы струи определяют толщину однослойных и многослойных покрытий на поверхности, площадью не менее 0,3 мкм. Методы основаны на растворении покрытия под действие струи электролита, вытекающей с определенной скоростью.
Металлографический метод основан на измерении толщины однослойных и многослойных покрытий на поперечном шлифе с помощью металлографического микроскопа при увеличениях до 1000 раз для покрытий толщиной менее 20 мкм и до 200 раз для покрытий толщиной более 20 мкм. Разновидностью металлографического метода является оптический, основанный на измерении при помощи металлографического микроскопа длины уступа, образованного краем покрытия с основным металлом. Метод применим для измерения покрытий толщиной 1-40 мкм с коэффициентом отражения не менее 0,3. Погрешность метода 10 %.
Из неразрушающих методов контроля наибольшее распространение получили электромагнитные методы, метод измерения масс, метод прямого измерения.
Электромагнитные методы основаны на изменении силы отрыва постоянного магнита от контролируемой поверхности в зависимости от толщины покрытия (магнитоотрывной); регистрации изменений напряжённости магнитного поля в цепи электромагнита постоянного тока в
39
зависимости от толщины покрытия (магнитостатический); определении магнитного сопротивления участка цепи соответствующего изменению толщины покрытия (магнитоиндукционный).
Метод прямого измерения заключается в измерении размеров детали до и после нанесения покрытия с помощью микрометра или оптиметра.
Гравиметрический метод предусматривает непосредственное взвешивание и измерение покрываемой поверхности образца или изделия до и после электроосаждения. Средняя толщина покрытия представляет собой отношение объема нанесенного покрытия к площади поверхности покрытого изделия. Изза трудностей измерения площади поверхности покрываемых изделий гравиметрический метод применяют для определения средней толщины гальванопокрытия на небольших деталях простого профиля.
Реактивы и оборудование
1.Электролизер.
2.Металлические электроды (медные, цинковые пластины).
3.Внешний источник тока.
4.Потенциометр или амперметр.
5.Соединительные проводники.
6.Набор растворов электролитов.
7.Аналитические весы.
Экспериментальная часть
Порядок выполнения работы
В данной работе для получения медного гальванического покрытия используется установка, представленная на рис. 9. Перед сбором установки необходимо определить массу катодной пластины, m1, и ее площадь, S, записать в таблицу 14. Для этого, катодную пластину отсоединяют и взвешивают на аналитических весах. Площадь катодной пластины определяют геометрически. Затем собирают установку для чего в электролизер наливают раствор соли меди (CuSO4) с концентрацией 0,1 моль/л объемом 300-400 мл. В раствор помещают исследуемые металлические пластины, таким образом, чтобы они были максимально покрыты раствором электролита. Одна из пластин служит катодом (К) и будет покрыта металлом, ионы которого присутствуют в растворе, а также тем металлом, из которого сделана анодная пластина (А). Электроды необходимо соединить проводниками с источником
40
постоянного тока, последовательно соединив с амперметром. Составленную схему установки необходимо показать преподавателю или лаборанту.
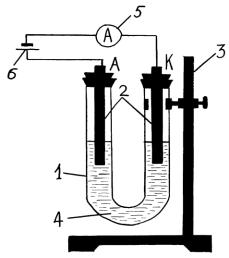
Рис. 9. Схема установки для электролитического нанесения покрытий:
1 - электролизер;
2 - электроды (металлические пластины);
3 - штатив;
4 - раствор электролита;
5 - амперметр;
6 - внешний источник тока
Силу тока и время проведения электролиза определяет преподаватель, так чтобы время электролиза составило не менее 30 мин. После этого, включают источника тока и засекают время электролиза. В течение времени осуществления электролиза студенты наблюдают за явлениями, происходящими на электродах, и записывают уравнения электрохимических процессов на электродах. После этого, проводят расчет теоретических значений массы, m3, и толщины покрытия, пользуясь законом Фарадея и уравнением 15. Результаты расчетов записывают в таблицу 14.
Таблица 14 Результаты определения толщины гальванического покрытия
гравиметрическим методом
Материал катодной пластины |
Состав раствора для нанесения покрытия |
Сила тока, А |
Время электролиза, мин |
Масса катодной пластины, г |
Толщина покрытия, см |
Погрешность, % |
|||
|
|
|
|
|
|||||
Без |
Эксперим., |
Теоретич., |
|
|
|||||
покрытия, |
после |
по закону |
|
|
|||||
m1 |
нанесения |
Фарадея, |
Эксперим. |
Теоретич. |
|||||
|
покрытия, |
m3 |
|||||||
|
|
|
|||||||
|
m2 |
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
По истечении времени электролиза источник тока отключают, катодную пластину извлекают, промывают дистиллированной водой, аккуратно высушивают фильтровальной бумагой и оставляют на 5 мин. до полного