Материал: 1488
связанных с изменением термодинамических параметров); p V – работа по преодолению внешнего давления, необходимая для удержания системы в состоянии механического равновесия, или работа расширения. Для многих систем она единственный вид работы, поэтому A = 0 и A = p∆V.
С |
V2 |
|
A pdV , тогда A pdV , |
||
V1 |
||
|
||
здесь d – мгновенное изменение; δ – бесконечно малая величина; индекс 1 |
||
– начальное, а ндекс 2 – конечное состояния системы. |
||
Первый закон термодинамики – это постулат. Известны следующие вивалентныхформулировки закона:
1. Закон сохранен я энергии в применении его к термодинамическим процессам является одним из выражений первого закона термодина-
мики: |
зол рованной с стеме о щий запас энергии сохраняется посто- |
|||||||||||
янным. |
|
|
|
|
|
|
|
|
|
|
|
|
2. Энерг я переход т из одного вида (формы) в другой в строго эк- |
||||||||||||
|
|
кол |
чествах. |
|
|
|
|
|
||||
3. Вечный дв гатель первого рода невозможен: получить работу, не |
||||||||||||
затрачивая энерг |
ю, нельзя. |
|
|
|
|
|||||||
|
|
|
|
|
|
А |
||||||
Пусть система переходит из состояния 1 в состояние 2. При этом |
||||||||||||
система поглощаетбтеплоту Q, которая расходуется на изменение внут- |
||||||||||||
ренней |
энергии |
системы |
∆U и совершение |
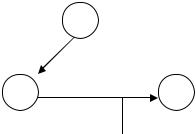
работы А (рис. 1). |
||||||||
Q = ∆U + A |
или |
Q = dU + A. |
Д |
|||||||||
Это математическое |
выражение |
|||||||||||
|
|
Q |
||||||||||
|
|
|
|
|
|
|
|
|
|
|||
первого закона термодинамики. |
|
|
|
|
||||||||
Рассмотрим изохорный про- |
|
|
|
|
||||||||
цесс (V = const): |
|
|
|
1 |
|
2 |
||||||
Qv dU pdV |
|
|
|
|||||||||
. |
|
|
|
∆U, A |
|
|||||||
Если |
V = const, |
то dV = 0, |
|
И |
||||||||
|
|
|
|
|||||||||
тогда |
pdV = 0 |
и, следователь- |
Рис. 1. Схема, иллюстрирующая |
|||||||||
но, QV dU; QV |
U2 |
U1 |
; |
|||||||||
первый закон термодинамики |
||||||||||||
|
|
|
|
|
|
|
|
|||||
Q U , или |
|
|
U . |
|
|
|
|
|
||||
QV |
|
|
|
|
|
|||||||
V |
|
|
|
|
|
|
|
|
|
|
|
|
11
Тепловой эффект реакции при изохорном процессе равен изменению внутренней энергии системы.
Рассмотрим изобарный процесс (р = const):
Qp dU pdV , |
или |
Qp (U2 U1) ( pV2 pV1) , |
|||
или |
Qp |
(U2 pV2 ) (U1 pV1). |
|||
Так как U pV H |
– это энтальпия системы, тогда |
||||
СибАДИ |
|||||
H2 U2 pV2 , H1 |
U1 pV1 |
или |
|
Qp H2 H1 и |
|
|
|
Qp H или |
Q |
p H . |
|
В зобарном процессе тепловой эффект реакции равен изменению |
|||||
энтальпии. |
|
|
|
|
|
Замен м выражен е H U p V на выражение Qp Qv pdV. огласно уравнен ю Клайперона – Менделеева, p V nRT , тогда
Qp Qv nRT ,
где n – зменен е ч сла молей газообразных веществ, участвующих в реакции.
Для конденс рованных систем Qр = QV.
Теплоёмкость – это количество тепла, необходимое для нагревания данного количества вещества на один градус. Удельная и молярная теплоёмкость – это отношение количества теплоты Q, поглощённое одним граммом (Суд – удельная) или одним молем (См – молярная) вещества к повышению температуры (∆T = T2 – T1), которым сопровождается его нагревание.
Единицы измерения теплоемкости: [Cуд] = |
ж/г·К, [Cм] = Дж/моль·К. |
||||||||||||
Средняя теплоемкость |
|
|
определяется как |
|
|
||||||||
|
|
|
|
|
C |
|
Q |
|
Q . |
|
|
|
|
|
|
|
|
|
T T |
|
|
|
|||||
|
|
|
|
|
|
T |
|
|
|
||||
|
|
|
|
|
|
|
2 |
1 |
|
|
|
|
|
Истинная теплоемкость определяется как |
|
|
|
||||||||||
|
|
|
|
C lim |
Q |
Q . |
|
|
|||||
|
|
|
|
T |
|
|
|||||||
|
|
|
|
|
T2 |
T1 |
dT |
|
|
|
|||
При p = const Cp |
Qp |
|
; |
|
при |
V = const |
CV |
Qv |
. |
||||
dT |
|
dT |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||
Разница между теплоемкостью при изобарных и теплоемкостью при изохорных условиях равна газовой постоянной R и описывается уравнением Майера Cр – CV = R.
Теплоемкость зависит от температуры. Зависимость C = f(T) выражается эмпирическими уравнениями, найденными опытным путём. Они
имеют вид
C = a + bT = cT2 + dT3 или C = a + bT + c'T-2,
12
где a, b, c, d, c'– коэффициенты, получаемые после обработки экспериментальных данных; они приведены в справочниках.
2.3. Термохимия
Термохимия – раздел термодинамики, который изучает тепловые |
|||
С |
|
|
|
Q понима- |
|||
эффекты процессов. В термохимии под тепловым эффектом |
|||
ют теплоту, которая выделяется или поглощается в результате процесса, протекающего при постоянном р или V, причём температура исходных веществ продуктов реакции одинакова, а полезная работа равна нулю
( A и= 0).
Закон Гесса – это основной закон термохимии. Формулировка закона: тепловой эффект процесса не зависит от числа и характера промежу-
точных стад й, а определяется только начальным и конечным состоянием |
|
системы. |
б |
|
|
Услов е пр менен я закона Гесса: закон применим только к тепло- |
|
вым эффектам процесса, т.е. к условиям, когда процесс протекает при р = const ли V = const. Закон применим не только к химическим реакциям, но и к любым другимАфизико-химическим процессам.
Термодинамическое о основание закона Гесса заключается в сле-
дующем. Установлено, что QV = ∆U, а QP = ∆Н. Так как внутренняя энергия U и энтальпия H являются функциями состояния системы, т. е. не за-
висят от пути процесса, то Q и Q не будут зависеть от промежуточных
стадий, а определяются только начальным и конечным состояниями системы.
Практическое значение закона Гесса заключается в следующем. За-
затруднено.
V PД
кон позволяет рассчитывать тепловые эффекты процессов, не проводя экспериментов, а также тепловые эффекты неосуществимых процессов и процессов, для которых определение тепловогоИэффекта опытным путём
Уравнение химической реакции с указанием теплового эффекта называется термохимическим уравнением. С термохимическими уравнениями можно обращаться так же, как и с алгебраическими уравнениями (складывать, умножать, делить).
Первое следствие из закона Гесса: тепловой эффект Q обратной ре-
акции равен по величине и противоположен по знаку тепловому эффекту прямой реакции.
aA + bB = cC + dD + Q ;
cC + dD = aA + bB – Q .
13
Второе следствие из закона Гесса: тепловой эффект реакции равен сумме энтальпий (теплот) образования продуктов реакций минус сумма энтальпий (теплот) образования исходных веществ.
H 0 |
298 |
H 0 f ,298(продуктов реакции) H 0 f ,298(исходных |
веществ), |
||||||
здесь индекс f – от лат. foramentum – образование. |
|
|
|||||||
С |
|
|
|
|
|||||
|
|
|
Например, для реакции aA + bB = cC + dD |
|
|||||
|
|
|
∆H0298 = [с∆H0f,298(С) + d∆H0f,298(D) – (a∆H0f,298(А) + b∆H0f,298(В)]. |
||||||
|
|
При сумм рован |
обязательно учитываются стехиометрические |
||||||
коэффиц енты уравнен я реакции. |
|
|
|||||||
если |
|
|
|||||||
|
|
Для расчета тепловых эффектов используются стандартные теплоты |
|||||||
образован я веществ. Стандартной теплотой (энтальпией) образования |
|||||||||
|
|
|
0 |
|
|
|
0 |
|
|
вещества (∆H f,298 |
|
|
∆H 298) называется изменение энтальпии при обра- |
||||||
зовании одного моля вещества из простых веществ, находящихся при |
|||||||||
стандартных услов ях. Стандартная энтальпия простого вещества равна |
|||||||||
нулю. |
|
|
|
|
|
|
|
||
|
|
Напр мер, |
|
вещество получено по реакции, выраженной термо- |
|||||
химическ м уравнен ем |
|
|
|||||||
|
|
|
Ca(тв) |
+ C(граф т) + 1,5O2(газ) = CaCO3(тв) |
+ 1207,7 Дж/моль, |
||||
|
|
|
|
|
|
А |
|
||
его стандартная теплота о разования равна |
|
|
|||||||
|
|
|
|
|
|
|
0 |
|
|
|
|
|
б∆H f,298(CaCO3) = – 1207,7 Дж/моль. |
|
|||||
|
|
Третье следствие из закона Гесса: тепловой эффект реакции равен |
|||||||
сумме теплот сгорания исходных веществ минус сумма теплот сгорания |
|||||||||
продуктов реакции. |
|
|
|
|
|||||
H |
0 |
H |
0 |
|
|
|
0 |
|
|
|
298 |
с,298(исходных веществ) H |
с,298(продуктов реакции), |
||||||
здесь индекс с – от лат. combustum – сгорание. |
|
|
|||||||
|
|
|
Например, для реакции aA + bB = cC + dD |
|
|||||
|
|
|
|
|
|
|
И |
||
|
|
|
∆H0298 = a∆H0с,298(А) + b∆H0с,298(В) – с∆H0с,298(С) – d∆H0с,298(D). |
||||||
|
|
|
|
|
|
|
|
0 |
0 |
|
|
Стандартная теплота сгоранияДвещества (∆H с,298, ∆H сгор) – это |
|||||||
уменьшение энтальпии в реакции сгорания одного моля простого вещест- |
|||||||||
ва или соединения до соответствующих окисленных форм элементов. |
|||||||||
|
|
Соединения, состоящие из углерода и водорода (например, топливо), |
|||||||
сгорают до CO2 |
и H2O. Стандартные теплоты сгорания и образования при- |
||||||||
ведены в справочных таблицах термодинамических величин.
Закон Кирхгофа устанавливает зависимость теплового эффекта реакции от температуры. Формулировка закона: температурный коэффициент теплового эффекта реакции равен изменению теплоемкости в результате процесса.
Уравнение Кирхгофа для изобарного процесса (р = const)
14

|
|
|
|
|
d H |
|
Cp , |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
dT |
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
где |
Cp Cp (продуктов) Cp (исходных |
|
веществ) . |
|||||||||||||||
|
В зависимости от знака ∆Cр |
тепловой эффект реакции (процесса) с |
||||||||||||||||
ростом температуры может увеличиваться или уменьшаться. |
||||||||||||||||||
1. |
Если ∆Cp > 0, то с ростом температуры ∆H увеличивается. |
|||||||||||||||||
2. |
Если ∆Cp < 0, то с ростом температуры ∆H уменьшается. |
|||||||||||||||||
3. |
Если ∆Cp = 0, то тепловой эффект не зависит от температуры. |
|||||||||||||||||
|
Про нтегр руем уравнение Кирхгоффа d∆H = ∆CрdT. |
|||||||||||||||||
|
Пусть теплоемкость Ср не зависит от температуры, т. е. ∆Ср = const, |
|||||||||||||||||
что допуст мо в небольшом интервале температур. |
|
|
|
|
|
|
|
|
||||||||||
С |
|
T2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
H2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
d H Cp dT , H2 H1 Cp (T2 T1 ). |
|||||||||||||||
|
|
H1 |
T1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
Отсюда выведем формулу для вычисления теплового эффекта: |
|||||||||||||||||
и∆H2 = ∆H1 + ∆Cр(T2 – T1) . |
|
|
|
|
|
|
|
|
||||||||||
|
Пусть теплоемкость ∆Cр является функцией от температуры, то есть |
|||||||||||||||||
∆Cp = f(T). Эта зав с мость выражается уравнением |
|
|
|
|
|
|
|
|||||||||||
|
Cp = a + bT + cT² |
или Cp = a + bT + |
|
|
|
|
2 |
. |
||||||||||
|
c T |
|
||||||||||||||||
|
В общембвиде изменение теплоемкости равно |
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
2 |
. |
|
|
|
||
|
|
|
∆Cp = ∆a + ∆bT + ∆cT² + c T |
|
|
|
|
|
|
|||||||||
|
Подставим это выражение в уравнение Кирхгофа, тогда |
|||||||||||||||||
|
|
|
d∆HТ = (∆a + ∆bT + ∆cT² +∆ |
|
|
|
|
2 |
)dT. |
|||||||||
|
|
|
c T |
|
|
|||||||||||||
|
|
|
А |
|
|
|
|
|
|
|||||||||
|
Возьмем неопределённый интеграл и получим выражение |
|||||||||||||||||
|
H |
|
aT |
b T 2 c T 3 c |
|
H |
|
. |
|
|
|
|||||||
|
T |
|
|
|
|
|
||||||||||||
|
|
|
2 |
|
3 |
T |
|
|
|
0 |
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
Полученное уравнение показывает зависимость теплового эффекта |
|||||||||||||||||
|
|
|
|
|
|
Д |
||||||||||||
|
|
|
|
|
|
|
|
И |
||||||||||
реакции от температуры. В нем ∆H0 – постоянная интегрирования, определяемая как значение теплового эффекта при одной из температур.
Уравнение Кирхгофа для изохорного процесса (V = const) d U
dT
2.4. Второй закон термодинамики
Самопроизвольные (спонтанные) процессы описываются следую-
щими характеристиками:
1. Все природные самопроизвольные процессы протекают в одном направлении, т. е. имеют одностороннее направление. Например, тепло от
15