Материал: 1150
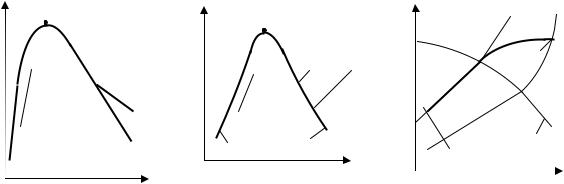
Изотермический процесс (Т = const), происходящий полностью в области насыщенного пара, совпадает с изобарным процессом в зоне насыщения. Изотермический процесс, начинающийся в области насыщения и заканчивающийся в зоне перегрева, изображен в диаграммах на рис. 1.8 линией 1-2.
Количество теплоты, участвующее в изотермическом процессе 1 2, может быть найдено графически, как площадь под кривой в Т s- диаграмме или по выражению
q1-2 = T(s2 – s1).
Энтропия влажного пара определяется по h s-диаграмме или формуле
sX = s' + rx/TS,
где s' – энтропия кипящей воды; ТS – температура насыщенного пара при данном давлении.
p |
К |
|
|
T |
|
|
|
К |
h |
|
|
p1 |
p2 |
||
|
|
|
|
|
|
|
|
|
t1 |
= t2 |
|||||
|
|
|
|
|
|
|
|
|
|
|
h2 |
|
|
||
|
1 |
|
|
|
|
|
|
р1 р2 |
|
|
|
2 |
|||
|
|
|
|
|
|
|
|
|
|
|
|||||
р1 |
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|||
|
2 |
|
|
|
h1 |
1 |
|
|
|||||||
р2 |
|
|
|
|
|
|
|||||||||
|
|
|
|
|
х1 |
|
|
|
|
|
|
|
|||
х1 |
|
|
|
|
|
|
|
|
|
х = 1 |
|||||
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
х = 0 |
х = 1 |
|
|
|
|||||||
|
х = 0 |
х = 1 |
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
s |
|
|
х1 |
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
s |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
а) |
|
|
|
б) |
|
|
в) |
|
|||||
|
|
Рис. 1.8. Изотермические процессы для водяного пара: |
|
||||||||||||
|
|
а – р -диаграмма, б – Т–s-диаграмма; в – h–s-диаграмма |
|
||||||||||||
Энтропия перегретого пара находится по h s-диаграмме или по таблицам термодинамических свойств воды и водяного пара.
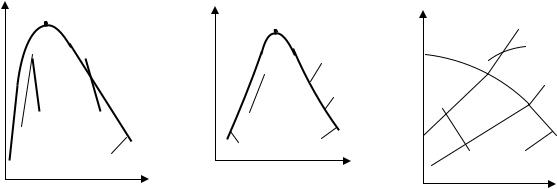
Адиабатный процесс (dq = 0). Примеры изображения адиабатных процессов водяного пара в диаграммах приведены на рис. 1.9.
Адиабата 1 2 полностью расположена в области влажного пара, а адиабата 3 4 начинается в области перегретого пара и заканчивается в зоне насыщения.
Уравнение адиабаты водяного пара описывается зависимостью
15
р К = const,
где к – показатель адиабаты ( к = 1,135 влажный насыщенный пар, к = 1,3 – перегретый пар).
p
р1
р2
К |
|
|
|
T |
|
К |
|
|
|
|
h |
|
|
|
p1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
1 |
3 |
|
|
|
|
|
|
3 р1 |
h3 |
3 |
|
t3 |
||||
|
|
Т3 |
|
1 |
|
|
|
|
p2 |
|||||||
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
Т1 |
|
|
|
|
|
р2 |
h1 |
1 |
|
|||
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
Т2 |
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
х1 2 |
|
|
|
|
|
|
|
|
||||
2 |
4 |
|
|
4 |
|
h4 |
|
|
|
|
||||||
|
|
4 |
|
|||||||||||||
х1 |
|
|
|
|
х = 0 |
х = 1 |
|
|
|
|||||||
х = 0 |
х = 1 |
|
h2 |
|
х1 |
х = 1 |
||||||||||
|
|
|
|
|
|
|
s |
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
s |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
а) |
|
|
|
|
|
б) |
|
|
|
|
|
|
в) |
|
||
|
Рис. 1.9. Адиабатные процессы для водяного пара: |
|
||||||||||||||
а – р- -диаграмма, б – Т–s-диаграмма; в – h–s-диаграмма |
|
|||||||||||||||
Работа адиабатного процесса равна
l1-2 = h1 – h2; l3-4 = h3 – h4.
1.2. Определение параметров воды и водяного пара по таблицам
Водяной пар, широко используемый в теплотехнике в качестве рабочего вещества, относится к реальным газам. В реальных газах, в отличие от идеальных, заметно влияние сил взаимодействия между молекулами. Известные уравнения состояния для водяного пара и для воды достаточно сложны, что инженерами непосредственно не используются, а в практике инженерных теплотехнических расчетов применяются таблицы и диаграммы воды и водяного пара, составленные по этим уравнениям.
Выполнение настоящей работы позволит студентам научиться определять по таблицам воды и водяного пара их термодинамические параметры.
1.2.1. Цель и задачи работы
Целью работы является ознакомление студентов с методикой определения параметров воды и водяного пара (реального газа) по таблицам. При этом решаются следующие задачи:
16
а) изучаются термодинамические таблицы воды и водяного пара; б) определяются параметры реального газа;
в) строится по найденным параметрам Т s-диаграмма.
1.2.2. Проведение работы
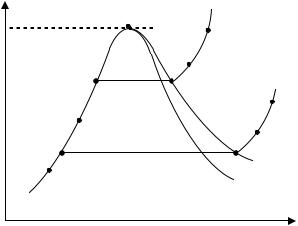
Используя таблицы термодинамических свойств воды и водяного пара [7] и приложение, требуется определить параметры воды и водяного пара при заданных давлениях р1 и р2 (табл. 1.1) и построить в масштабе Т s-диаграмму (рис. 1.10). Нанести на диаграмму критическую точку К; линии кипящей воды х = 0, сухого насыщенного пара х = 1, постоянных давлениях р1 и р2 и линию постоянной степени су-
хости х = const.
T |
ТК |
|
|
К |
2в р2 |
Перегретый |
|
|
|
|
|
|
|
||||
|
Жидкость |
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
р2 |
|
2б |
|
пар |
Рис. |
1.10. |
Т s-диаграмма |
|||||||||
|
|
2' |
|
|
р1 |
|
воды и водяного пара: х = 0 |
||||||||||
|
|
|
2" |
|
|||||||||||||
|
2a |
|
|
|
|
|
1в |
|
– линия кипящей |
жидко- |
|||||||
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
сти; х = 1 – линия сухого |
||||||||
|
|
|
|
|
|
|
|
|
|
||||||||
|
1' |
|
|
р1 |
1" |
1б |
|
насыщенного пара; К – кри- |
|||||||||
|
1a |
|
|
|
|
|
|
|
х = 1 |
|
тическая точка; х – степень |
||||||
|
х = 0 |
|
Влажный |
|
х = const |
|
сухости пара |
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
пар |
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
s |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Таблица 1.1 |
||
|
|
Исходные данные к построению Т s-диаграммы |
|
|
|
|
|||||||||||
|
(значения р1 и р2 |
даны в МПа; х – безразмерная величина) |
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Исх. |
|
|
|
|
|
|
|
|
Варианты |
|
|
|
|
|
|
|
|
дан. |
1 |
2 |
|
3 |
|
|
4 |
5 |
6 |
7 |
|
8 |
|
9 |
|
10 |
|
р1 |
0,01 |
0,02 |
|
0,03 |
|
0,04 |
0,05 |
0,06 |
0,07 |
|
0,08 |
|
0,09 |
|
0,02 |
||
р2 |
0,5 |
1,0 |
|
1,5 |
|
2,0 |
2,5 |
3,0 |
3,5 |
|
4,0 |
|
4,5 |
|
5,0 |
||
х |
0,6 |
0,4 |
|
0,5 |
|
0,7 |
0,9 |
0,8 |
0,3 |
|
0,4 |
|
0,6 |
|
0,8 |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Исх. |
|
|
|
|
|
|
|
|
Варианты |
|
|
|
|
|
|
|
|
дан. |
11 |
12 |
|
13 |
|
|
14 |
15 |
16 |
17 |
|
18 |
|
19 |
|
20 |
|
р1 |
0,03 |
0,04 |
|
0,06 |
|
0,08 |
0,05 |
0,02 |
0,01 |
|
0,07 |
|
0,03 |
|
0,09 |
||
р2 |
5,6 |
6,0 |
|
6,6 |
|
7,0 |
7,6 |
8,0 |
8,6 |
|
9,0 |
|
9,6 |
|
10 |
||
х |
0,3 |
0,7 |
|
0,5 |
|
0,4 |
0,8 |
0,9 |
0,3 |
|
0,6 |
|
0,2 |
|
0,7 |
||
|
|
|
|
|
|
|
|
|
17 |
|
|
|
|
|
|
|
|
Построение диаграммы Т s начинают с осей ординат и абсцисс (температуры Т и удельной энтропии s). Температура в критической точке равна ТКР = 374,15 ОС, а энтропия в этой точке равна sКР = = 4,4237 кДж/(кг К). Поэтому на оси ординат следует отложить температуру от 0 до 500 ОС. Удобнее для дальнейшего построения диаграммы на каждые 100 ОС оставить 5 клеток тетрадного листа. По оси абсцисс следует отложить значения энтропии s от 0 до 10 кДж/(кг К). Удобнее для дальнейшего построения диаграммы на каждую единицу энтропии оставить 2 клетки тетрадного листа.
По значениям ТКР и sКР наносится критическая точка К. Затем строятся нижняя пограничная кривая (линия кипящей жидкости х = 0) и верхняя пограничная кривая (линия сухого насыщенного пара х = 1). Для этого по термодинамическим таблицам воды и водяного пара по известным давлениям определяют температуру и энтропию в точках 1', 1", 2', 2". Все определенные по таблицам параметры заносятся в отчет по форме табл. 2 без округлений из значений. Линии 1'- 1" и 2'-2" являются изобарно-изотермическими процессами.
При определении параметров воды в точках 1а и 2а необходимо задать температуры воды ниже температуры насыщения, а при определении параметров перегретого пара в точках 1б, 1в, 2б и 2в необходимо задать температуры выше (на 100–200 ОС) температуры насыщения при заданных давлениях р1 и р2 и по ним и табл. П.3 определить требуемые параметры. Параметры в критической точке К приведены в настоящем учебно-методическом пособии и в [7].
|
|
|
|
|
|
Таблица 1.2 |
|||
|
Параметры воды и водяного пара, найденные по таблицам |
|
|
||||||
|
|
|
|
|
|
|
|
|
|
Точки |
|
р, |
t, |
, |
h, |
s, |
|
х |
|
|
|
МПа |
ОС |
м3/кг |
кДж/кг |
кДж/(кг К) |
|
|
|
К |
|
|
|
|
|
|
|
|
|
1' |
|
|
|
|
|
|
|
|
|
1" |
|
|
|
|
|
|
|
|
|
1а |
|
|
|
|
|
|
|
|
|
1б |
|
|
|
|
|
|
|
|
|
1в |
|
|
|
|
|
|
|
|
|
2' |
|
|
|
|
|
|
|
|
|
2" |
|
|
|
|
|
|
|
|
|
2а |
|
|
|
|
|
|
|
|
|
2б |
|
|
|
|
|
|
|
|
|
2в |
|
|
|
|
|
|
|
|
|
|
|
|
|
18 |
|
|
|
|
|
Построение Т s-диаграммы выполняется в масштабе путем нанесения соответствующих точек и соединения их, как показано на рис. 1. Для нанесения линии постоянной степени сухости х = const необходимо линии постоянных давлений в области влажного пара 1'-1" и 2'-2" разбить каждую на 10 равных отрезков. Каждый отрезок будет соответствовать 0,1х, и затем надо от линии х = 0 отложить требуемое число отрезков в соответствии с заданным х. Полученные точки необходимо соединить линией, исходящей из критической точки.
Контрольные вопросы
1.Покажите, как изображается в Т s-диаграмме энтальпия кипящей воды, сухого насыщенного пара и перегретого пара.
2.Как при помощи таблиц водяного пара можно определить, в каком состоянии находится вода, если известны ее параметры»?
3.Как могут быть вычислены параметры в области влажного па-
ра?
4. Приведите определения следующих процессов и понятий: парообразование, конденсация, испарение, кипение, влажный и сухой насыщенный пар, перегретый пар.
5.За счет чего происходит изменение в изотермическом процессе водяного пара и как его подсчитать при заданных начальных и конеч-
ных параметрах р, , h.
6.Как могут быть графически построены линии постоянной сухости в р -, Т s- и h s-диаграммах?
7.Покажите с помощью Т s-диаграммы, как будет меняться влажность пара в адиабатных процессах сжатия, если в первом случае процесс протекает при значении энтропии меньше критического, а во втором – больше критического.
8.Изобразите на диаграммах р , Т s и h s изохорный и изотермический процессы превращения влажного насыщенного водяного пара в перегретый. Дайте краткие пояснения.
9.Изобразите р -диаграмму для воды и перегретого пара и покажите, как в этой диаграмме изображаются характерные линии. По-
ясните, на какие области можно разделить р -диаграмму. Какие состояния откладываются на нижней и верхней пограничных кривых? Что такое степень сухости и влажность пара?
19