Материал: Інформаційні міжклітинні взаємодії. Клітинні рецептори та їхня участь у процесах міжклітинної сигналізації
Внутрішньоклітинні сигнальні молекули передають сигнал від мембранних рецепторів на ефектори (виконавчі молекули), що опосередковують відповідь клітини на сигнал. До других (внутрішньоклітинних) посередникам свідносяться циклічні нуклеотиди (цАМФ і цГМФ), ІТФ, диацилглицерол, Ca2+, а також продукти окислення арахідонової кислоти. [3]
Циклічні нуклеотиди (цАМФ, цГМФ)
Ланцюг реакцій, ключовою ланкою в якій служить цАМФ, виглядає так: гормон - рецептор - активатор (Gs) аденілатциклази - активність аденілатциклази - [цАМФ] Т - активація цАМФ-залежної протеїнкінази A - фосфорилювання різних білків (переважно ферментів) - каскад ферментативного реакцій - фізіологічний відповідь клітини. Фундаментальна властивість цієї та інших систем других посередників полягає в тому, що сигнал багаторазово посилюється (феномен мультиплікації). [3] Наприклад, достатньо кількох молекул аденілатциклази, щоб активувати багато молекул інших ферментів і пустити в хід наростаючий каскад ферментних реакцій. Таким шляхом навіть невелика кількість молекул ліганда може викликати потужний фізіологічний відповідь клітини-мішені.
Іони Ca2 +
Іони Ca2 + - поширений другий посередник, що регулює безліч процесів. Функціонування іонів Ca2 + в якості других посередників можливо лише при підтримці нормальної [Ca2 +] в цитозолі у вкрай низьких межах (<100 нмоль / л), що підтримується Ca2 + -АТФазою плазмолемми і внутрішньоклітинними депо кальцію (наприклад, ендоплазматичний ретикулум). [3]
G-білки
Основним класом мембранних білків є рецептори,
зв'язані з G-білками. G-білки активують або пригнічують роботу аденілатциклази,
гуанілатциклази та фосфоліпази C, впливаючи на синтез вторинних посередників:
цАМФ, цГМФ, інозитол-3-фосфату (І3Ф), діацилгліцеролу (ДАГ). [4]
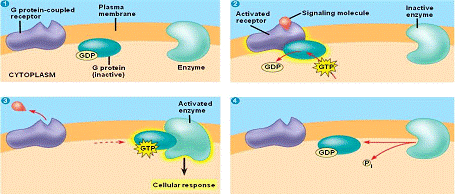
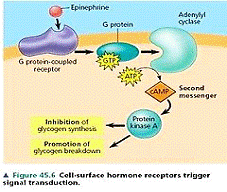
Рис. 2.3. Активація G-білка (приклад вторинного месенджера)
2.2 Рецептори
Рецептори в клітині-мішені - білки
(в ряді випадків гліко- і лі ліпопротеїни), в кожній клітині-мішені їх
налічуються тисячі і десятки тисяч. Кількість рецепторів в клітинах-мішенях не
залишається постійною: рецептори інактивуються або руйнуються в процесі їх
функціонування, реактивуються і постійно синтезуються. Ліганд, взаємодіючи з
його рецептором, утворює лігандрецепторний комплекс, що найсерйознішим чином
змінює функціональні можливості рецептора і є поштовхом до прояву
фізіологічного ефекту. Рецептори (залежно від їх розташування в клітині-мішені)
поділяються на мембранні (вбудовані в плазматичну мембрану) і
внутрішньоклітинні - цитозольні і ядерні. Деякі рецептори вбудовані в мембрани
внутрішньоклітинних органел (наприклад, в мембранах ендоплазматичної сітки
знаходяться рецептори ріанодина і інозітолтріфосфату - ІТФ).[2]
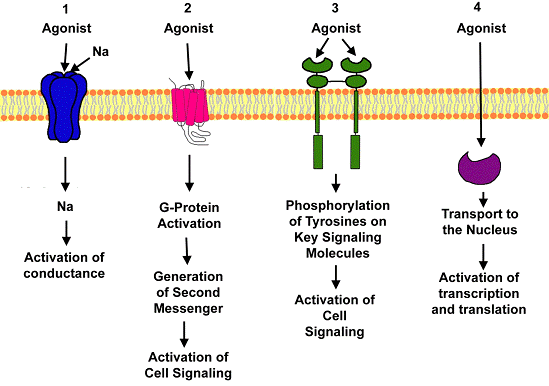
Рис. 2.4. Приклади рецепторів
Мембранні рецептори
Мембранні рецептори реєструють наявність ліганда і передають сигнал вторинним месенджерам. Вони класифікуються наступним чином:
• Каталітичні рецептори - трансмембранні білки, зовнішня частина яких містить зв'язуючу ліганд ділянку, а цитоплазматична частина або сама функціонує як активний центр ферменту, або тісно пов'язана з молекулою ферменту.
• Рецептори, пов'язані з іонними каналами, впливають на проникність іонних каналів через другі посередники. До них відносяться адренорецептори, мускаринові холінорецептори, рецептори серотоніну, дофаміну. Рецептори цього типу - метаботропні рецептори, вони активуються в клітині-мішені в результаті різних метаболічних процесів, що відбуваються після утворення комплексу «ліганд-рецептор». [4]
• Керовані лігандами іонні канали - інтегровані мембранні білки - поєднують властивості рецептора і іонного каналу і вбудовані в постсинаптичну мембрану нервових клітин, а також в постсинаптичну мембрану нервово-м'язових синапсів між розгалуженнями аксонів мотонейронів і скелетними м'язовими волокнами. [4] Іншими словами, деякі рецептори нейромедіаторів самі по собі є іонними каналами - іонотропні рецептори (зв'язування ліганда з рецептором регулює трансмембранну проникність за рахунок іонного каналу в складі рецептора).
• Рецептори, пов'язані з G-білком, - поліпептидні ланцюжки, розташовані в плазматичної мембрані клітини-мішені таким чином, що поліпептид пронизує мембрану сім раз, утворюючи при цьому по три назовні і досередини від мембрани петлі. Позаклітинний N-кінець поліпептида містить зв'язуючий ліганд ділянку, внутрішньоклітинний C-кінець розташований в цитозолі, а одна зі звернених всередину клітини петель пов'язує G-білок. [2]
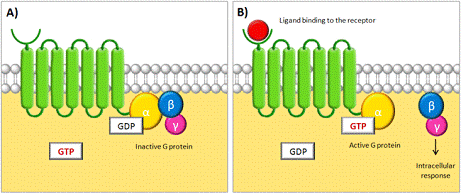
Рис. 2.5. Рецептор G-былка.
• Рецептори, що звільняють фактори транскрипції, - трансмембранні білки, вбудовані в плазмолему і в мембрани ЕПР. Після активації цього типу рецепторів протеолітичні ферменти відщіплюють від рецепторів звернений в цитозоль фрагмент, що надходить в ядро клітини і специфічно зв'язується з промоторними послідовностями ДНК, що запускає транскрипцію відповідного гена. Ці рецептори і звільнені ними фактори транскрипції регулюють процеси диференціювання (спеціалізації) клітин, внутрішньоклітинний вміст холестеролу, а також метаболізм амілоїду. [4]
Ядерні рецептори
Ядерні рецептори - білки-рецептори стероїдних гормонів (мінерало- і глюкокортикоїди, естрогени, прогестини, тестостерон), ретиноїдів, тиреоїдних гормонів, жовчних кислот, вітаміну D3. Кожен рецептор має область зв'язування ліганда і ділянку, що взаємодіє зі специфічними послідовностями ДНК. Іншими словами, ядерні рецептори - фактори транскрипції, що активуються лігандом. В геномі людини є більше 30 ядерних рецепторів, ліганди яких знаходяться в стадії ідентифікації (сирітські рецептори). [3]
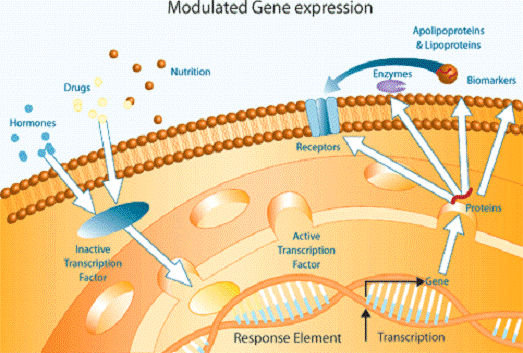
Рис. 2.7. Вплив біоактивних речовин
на експресію генів
2.3 Характеристика молекулярних рецепторів і різних трансмітерів
· Ацетилхолінові рецептори
Ацетилхолін як нейромедіатор периферичної та центральної нервової системи взаємодіє з двома видами холінорецепторів: мускариновими (m-холінорецепторами) метаботропними і нікотиновими (n-холінорецепторами) іонотропними. Ці підтипи рецепторів відрізняються по специфічності взаємодії з низкою агоністів і антагоністів ацетилхоліну. Так, м-ХР вибірково збуджуються мускарином, а н-ХР відповідають на вплив нікотину. Фізіологічно важливою відмінністю між м-ХР і н-ХР є швидкість відповіді на сигнал, що надходить. Вважають, що н-ХР забезпечують швидкі й нетривалі ефекти, тоді як м-ХР реагує більш повільно і тривало. [9]
o Нікотинові холінорецептори
Н-ХР виявилися більш вивченими біохімічно завдяки існуванню двох факторів: наявність специфічного нейротоксина, здатного блокувати функцію рецептора, і виявленню великої кількості цього рецептора в електричних органах риб. Н-ХР містить 5 субодиниць: дві а-субодиниці з М до 40 кД, одну р-субодиницю - М 49 кД, одну γ-субодиницю - 60 кД і одну 5-субодиницю - М 67 кД. Катіонні групи двох молекул ацетилхоліну зв'язуються з аніонними ділянками ct-субодиниць. Канал, що відкривається при контакті з АХ на кілька мілісекун, встигає пропустити до 5 іонів К + та Na +. АХ, що дисоціювали з рецептором, або "надлишковий" АХ в синаптичній щілині швидко розщеплюється ферментом ацетилхолінестеразою, розташованим на постсинаптичні мембрані в безпосередній близькості від рецептора. Ацетилхолінестераза є одним з найбільш швидкодіючих, високооборотних ферментів. Таким чином, сигнал обмежений у часі. Холін, що утворився, захоплюється білками-транспортерами пресинаптичної мембрани і служить далі для ресинтезу АХ в терміналі.
Активність рецептора може модулюватися з боку клітини фосфорилюванням окремих амінокислотних залишків ділянок, звернених всередину клітини. Рухливість рецептора обмежена зв'язком з цитоскелетними білками через білок 43К. [9]
Здатність різних сполук взаємодіяти з цими рецепторами має не тільки теоретичне, а й велике практичне значення. Оскільки порушення холінергічної медіації лежить в основі ряду патогенетичних механізмів захворювань нервової, ендокринної, імунної систем, то пошук лікарських речовин, що безпосередньо впливають на пострецепторні механізми, є перспективним. Як показала практика, багато використовувані в клініці н-холінергічні фармпрепарати мають точкою свого прикладання периферичні моторні синапси, ганглії і деякі хемочутливі структури вісцеральних систем. Часто в клініці застосовують блокатори н-ХР, серед яких виділяють гангліоблокатори і міорелаксанти. [6]
o Мускаринові рецептори ацетилхоліну
Ця категорія рецепторів ацетилхоліну відноситься до категорії метаботропних. Загальні їх характеристики вже описані. Пептидний ланцюг, що утворює основу м-ХР, складається з 800-950 амінокислотних залишків і пов'язаний з вуглеводними компонентами. Існує велике число підтипів м-ХР, пов'язаних з різними фізіологічними ефектами. [9]
Мускаринові рецептори АХ пов'язані з психоемоційним сприйняттям, секрецією слинних і шлункових залоз, функцією серцево-судинної системи тощо. Антагоністи м-ХР застосовуються в клініці в якості виразкозагоюючих, спазмолітичних препаратів, а також використовуються для симптоматичного лікування паркінсонізму. В якості заспокійливих засобів, транквілізаторів, знаходять застосування в терапії амізил і метамізіл - центральні блокатори м-ХР. [6]
· ГАМК-рецептори
Успіхи в ідентифікації різних типів ГАМК-рецепторів, їх біологічних і фармакологічних характеристик тісно пов'язані зі створенням специфічних аго-ністів і антагоністів. За локалізацією ГАМК-рецептори поділяються на центральні і периферичні, пре- і постсинаптичні. Розрізняють два типи рецепторів ГАМК: бікукулін-чутливі і баклофен-чутливі. Найбільш вивченим є перший тип рецепторів, який чутливий також до антагоніста пікротоксиніну. Виявлено, що цей тип рецепторів є швидкодіючим і пов'язаний з іонними каналами. Інший тип ГАМК-рецепторів відноситься до повільнодіючих рецепторам, і вважають, що він через G-білок асоційований з каналами для іонів К + та Са +. Дослідження фізико-хімічних властивостей очищеного ГАМКд-білка показали, що він представляє собою пентамер глікопротеїдної природи, який утворює канали для іонів хлору.
Особливістю ГАМКА-рецепторів є те, що вони містять специфічні ділянки зв'язування не тільки самої ГАМК, а й інших фізіологічно активних сполук. Найбільш цікавими і вивченими серед них є лікарські сполуки, об'єднані під назвою бензодіазепіни, а також ендогенні регулятори пептидної природи - ендозепіни. [9]
Важливою особливістю функціонування ГАМК-ергічної трансмісії є система видалення надлишкового ліганда з синаптичної щілини. На відміну від багатьох інших синаптичних систем ГАМК переважно зазнає зворотного захоплення і повертається в нервові закінчення за допомогою білків-транспортерів.
Місця специфічного зв'язування бензодіазепінів знаходяться на молекулах білка, що входить в структуру рецептора ГАМК. Активація ГАМК-рецепторів призводить до відкриття іонного каналу для хлору, а бензодіазепіни при цьому подовжують тривалість існування відкритих іонних каналів, не впливаючи на їх число і швидкість транспорту хлору.
Ділянка зв'язування бензодіазепінів взаємодіє також з ендогенними пептидними регуляторами. Останні володіють фізіологічними ефектами, протилежними бензодіазепінам - викликаютю збудження, тривожність і проконфліктну поведінку тварин. Таким чином, бензодіазепіни екзогенними антагоністами ендогенних антагоністів ГАМК. [9]
· Гліцинові рецептори
Найбільша щільність гліцинових рецепторів виявлена в області ядер під'язичного і трійчастого нервів, локалізованих в довгастому мозку. Ділянки зв'язування стрихніну знайдені також в ретикулярних ядрах довгастого мозку, моста і середнього мозку, сірії речовині спинного мозку як в передніх, так і в задніх рогах.
Гліциновий рецептор спинного мозку ссавців був очищений за допомогою афінної хроматографії на амінострихнин-агарози. Виявлено, що він представляє собою глікопротеїноліпідний комплекс з М понад 250 кД, що складається з 3 поліпептидів: 48, 58, 93 кД. Вбудований в ліпосоми білок активує транспорт іонів назовні, який блокується в присутності стрихніну. [9]
Є дані про те, що деякі ділянки гліцинового і ГАМК-рецепторів імунологічно ідентичні. Цей факт добре підтверджений генно-інженерними дослідженнями. [6]
· Глутаматні рецептори
Наявність глутаматзв’язуючої активності, незалежної від присутності в середовищі іонів Na+, виявлено практично у всіх структурах головного мозку. Найбільша кількість цих ділянок - в корі великих півкуль, гіпокампі, смугастому тілі, середньому мозку і гіпоталамусі.
) ділянку зв'язування нейромедіатора;
) регуляторну, або коактувючу, гліцінову ділянку;
) ділянка всередині каналу, який пов'язує фенциклідин і споріднені сполуки;
) потенціал-залежну Mg 2+ - зв'язуючу ділянку;
) гальмівну ділянку зв'язування двовалентних катіонів. [2]
Найважливішою функцією, яку здійснює рецептор NMDA в ЦНС, є керування іонним каналом.
До іншого підтипу рецепторів глутамата - не-NMDA-рецептори - належать, зокрема, рецептори квісквалової кислоти. Вивчення останніх привело до перегляду уявлення про те, що дія глутамату як нейромедіатора зводиться лише до деполяризації мембрани. Багато типів глутаматних рецепторів, і особливо рецептори квісквалата, можуть функціонувати як повільнодіючі метаботропи. [9]
Перспективними є дослідження складу глутаматних рецепторів в патохімії ряду захворювань ЦНС. Вважають, що ці нейрорецептори можуть служити маркерами деструктивних ушкоджень, що збуджують глутаматергічні шляхи головного мозку і беруть участь в аутоімунних реакціях організму людини. З'явилися вже конкретні приклади використання різних антагоністів глутаматних рецепторів проти явищ токсичної дії високих парціальних тисків кисню, при лікуванні інсультів тощо. [6] Крім того, антагоністи глутаматних рецепторів можуть скласти основу для створення малотоксичних інсектицидних препаратів для сільського господарства.
· Адренорецептори
Історія вивчення адренорецепторів тісно пов'язана з відкриттям біологічної функції катехолінів в клітинах надниркових залоз. Незважаючи на те що адренорецептори в нервової тканині присутні у відносно невеликій кількості, вони грають важливу роль в регуляції психоемоційних функцій і діяльності всіх відділів серцево-судинної системи. [9]білки мають суттєві відмінності в різних класах адренергічних рецепторів. Важливою загальною їх властивістю є взаємодія з ГТФ і ГДФ. У неактивному стані вони пов'язані з ГДФ. При взаємодії нейромедіатора з рецепторним білком останній вступає в контакт з G-білком і змінює його конформацію так, що на місце ГДФ стає ГТФ. З цього моменту G-білок набуває здатності впливати на активність білка-ефектора. [4][9]