Материал: В-Л-Быков-Цитогогия_и_общая_гистология
Наконец, в самые последние годы сформировалось и получило мощное развитие новое направление биоинженерии, использующее знания, накопленные в области гистологии и цитологии в целях медицины - тканевая инженерия. Задачей этого быстро совершенствующегося направления является выращивание в искусственных условиях клеток, тканей и органов человека для последующей трансплантации и замещения поврежденных в результате травмы или заболевания. Полученные результаты и имеющиеся тенденции развития методов тканевой инженерии свидетельствуют о большой перспективности этого направления для практической медицины.
- 11 -

Глава 2
МЕТОДЫ ЦИТОЛОГИЧЕСКИХ И ГИСТОЛОГИЧЕСКИХ ИССЛЕДОВАНИЙ
ОБЩИЕ СВЕДЕНИЯ
Гистология и цитология располагают разнообразным арсеналом как классических, так и современных методов, направленных на изучение строения и функций клеток, тканей и органов. Цитологические и гистологические методы исследования получают все большее распространение и в клинической диагностике различных заболеваний. В этой связи вопросы взятия, обработки и изучения материала для цитологического и гистологического исследования, рассматриваемые ниже, имеют не только теоретическое, но и сугубо прикладное, клиническое, значение. В последние годы особую роль в раскрытии закономерностей деятельности органов, тканей и клеток играют новые морфофункпиональные методы, использующие достижения современной биохимии, физики, иммунологии и молекулярной биологии - цито- и гистохимические, иммуноцито- и гистохимические, авторадиографические, метод гибридизации in situ и др. Использование методов электронной микроскопии позволяет с высоким разрешением выявить тонкие структурные детали на различных уровнях - от клеточного до макромолекулярного. Указанные современные методы из области научных исследований активно проникают в практическую клиническую диагностику.
Размеры объектов и их деталей, изучаемые с использованием цитологических и гистологических методов, обычно столь малы, что невидимы невооруженным глазом. Они составляют преимущественно микрометры (мкм) в световой микроскопии и нанометры (нм) в электронной микроскопии. Широко используемая ранее единица ангстрем (А), равная 10-1нм, в настоящее время более не применяется.
Соотношения между величинами линейных единиц измерения, наиболее часто используемых в гистологии и цитологии:
1 |
миллиметр (1 мм) |
= 10-3 |
м |
= 103 |
мкм |
= 106 |
нм |
= 10-7 |
А |
1 |
микрометр (1 мкм) = 10-6 |
м |
= 10-3 |
мм |
= 103 |
нм |
= 104 |
А |
|
1 |
нанометр (1 нм) |
= 10-9 |
м |
= 10-6 |
мм |
= 10-3 |
мкм |
= 10 |
А |
1 |
ангстрем (1 А) |
= 10-10 м |
= 10-7 |
мм |
= 10-4 |
мкм |
= 10-1 |
нм |
|
- 12 -
МЕТОДЫ ИЗУЧЕНИЯ ОГАНОВ, ТКАНЕЙ И КЛЕТОК ПОД СВЕТОВЫМ МИКРОСКОПОМ
ГИСТОЛОГИЧЕСКИЕ И ЦИТОЛОГИЧЕСКИЕ МЕТОДЫ ИССЛЕДОВАНИЯ
Взятие материала для гистологического исследования производится путем биопсии (от греч. bios - жизнь и opsis - зрение) - извлечения кусочка изучаемого органа (биоптата) из живого организма в целях прижизненной диагностики. Биоптат часто получают из внутренних органов при эндоскопии (от греч. endo - внутри, skopeo - смотреть) - исследовании полых органов с помощью гибких трубчатых приборов, снабженных освещением, оптическими системами и дополнительными приспособлениями (в частности, для взятия цитологического и гистологического материала). Материал для гистологического исследования в целях посмертной диагностики получают также при патологоанатомическом вскрытии - аутопсии (от греч. autos - сам и opsis - зрение, т.е. увиденное собственными глазами). В экспериментальных исследованиях получают ткани и органы лабораторных животных (целиком или в виде фрагментов). После взятия материала его подвергают специальной обработке для подготовки к последующему микроскопическому исследованию.
Подготовка материала к гистологическому исследованию. Основным методом в гистологических исследованиях является изучение окрашенных срезов различных тканей и органов. Традиционный способ подготовки материала для получения постоянного гистологического препарата включает:
(1) фиксацию материала, (2) проводку (обезвоживание), (3) заливку (уплотнение), (4) приготовление гистологических срезов (резку), (5) окрашивание срезов, (б) заключение срезов.
1. Фиксация гистологического материала (от лат. fixatio - закрепление)
осуществляется для "закрепления" его прижизненного строения. Она предотвращает разложение извлеченных из организма тканей под действием собственных ферментов (процесс аутолиза - от греч. autos - сам и lysis - распад), а также ферментов микроорганизмов и способствует сохранению целостности клеточных и тканевых структур. Воздействуя на ткани, фиксатор (например, формалин, спирт, пикриновая кислота или различные сложные смеси веществ), вызывает необратимую коагуляцию белков и быструю гибель клеток. Наиболее часто используют иммерсионную фиксацию - погружение (иммерсию - от лат. immersio - погружение) кусочка органа в раствор фиксатора; в экспериментальных условиях фиксатор нередко вводят через сосудистую систему (перфузионная фиксация - от лат. perfusio - вливание).
- 13 -
Хотя исследования фиксированного материала проводятся не на живых, а на мертвых тканях и клетках, при оптимальной фиксации они сохраняют морфологические особенности, свойственные живым объектам. Благодаря этому на основании анализа фиксированного материала можно делать заключения о прижизненном строении клеток и тканей. При фиксации материала, как и на всех дальнейших этапах его подготовки к исследованию, возможно появление артефактов.
Артефакты (от лат. arte - искусство и factum - продукт) - признаки, возникающие в структуре клеток и тканей в результате вмешательства исследователя на различных этапах обработки материала и отсутствующие в них прижизненно. При анализе конкретного объекта предпочтительно использование методов, дающих минимально выраженные артефакты. Типичным артефактом фиксации, в особенности, в спиртовых растворах, служит сжатие клеток и тканей.
2.Проводка (обезвоживание) материала осуществляется путем последовательного помещения кусочка в спирты возрастающих концентраций для удаления из него воды. Она необходима для выполнения следующего этана обработки материала - его заливки.
3.Заливка (уплотнение) материала достигается путем пропитывания обезвоженного кусочка затвердевающими средами: расплавленным парафином, целлоидином или специальной пластической массой. В результате заливки после охлаждения парафина или полимеризации пластмассы кусочек ткани (блок) становится достаточно плотным для получения тонких срезов при резке.
4.Приготовление гистологических срезов (резка) осуществляется на специальном приборе (микротоме) с помощью особых стальных ножей - бритв (рис. 2-1). При этом обычно получают срезы залитого в парафин или другую среду материала толщиной 5-7 мкм (в оптимальном варианте - серийные, т.е. следующие один за другим в виде непрерывной ленты).
Резка замороженного материала (затвердевшего при быстром охлаждении углекислотой или погружением в жидкий азот) позволяет получить тонкие срезы, минуя этап заливки. Она производится на замораживающем микротоме (микротоме, снабженном замораживающим устройством) или в криостате (специальном холодильном шкафу с помещенным в него микротомом). Благодаря своей скорости этот метод используется для экспресс-диагностики (в частности, в ходе выполнения хирургических операций, когда дальнейший характер вмешатель-
- 14 -
ства может определяться поставленным гистологическим диагнозом). Он применяется также в тех случаях, когда фиксация тканей нежелательна, например, при гистохимических и иммуногистохимических исследованиях (см. ниже). При проведении этих исследований важно, что нефиксированный материал, замороженный в жидком азоте, может храниться в нем неопределенно долго без изменения содержания, распределения и активности всех биологических веществ.
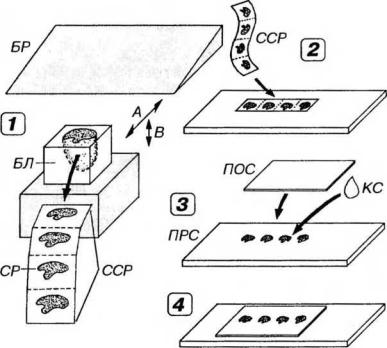
Рис. 2-1. Приготовление постоянного гистологического препарата из кусочка ткани, залитого в затвердевающую среду. Фиксированный и залитый в парафин, целлоидин или пластмассу кусочек ткани - блок (БЛ) - режут с помощью стальной бритвы (БР) на специальном приборе - микротоме (1). Для получения среза (СР) по оси А в различных конструкциях микротомов перемещается либо БР, либо БЛ, тогда как второй элемент остается неподвижным. Толщина СР определяется величиной шага взаимного смещения БЛ и БР по оси В. СР в виде серии (ССР) далее монтируют на предметное стекло (ПРС), подвергают депарафинированию (или удалению пластмассы) и окрашивают (2). Далее СР обезвоживают, просветляют, заключают в прозрачную консервирующую среду (КС) - бальзам или синтетическую смолу - и закрывают сверху покровным стеклом (ПОС) - (3). В результате получают постоянный гистологический препарат (4).
- 15 -