Материал: Термодинамические расчеты соединений
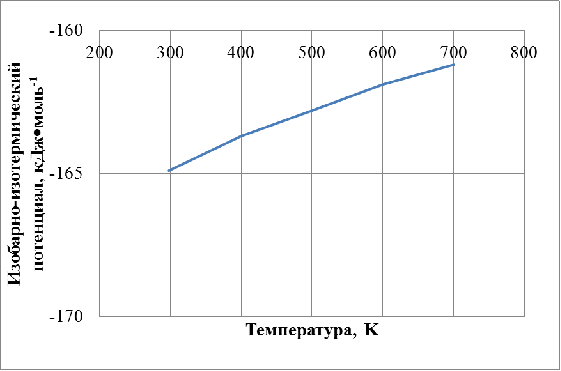
Рисунок 1 ˗ Зависимость изобарно-изотермического потенциала от
температуры
Как показывают полученные результаты, реакция образования CuFeO2 протекает в интервале температур от
298 до 700 К при стандартном давлении, с увеличением температуры её вероятность
убывает.
4. РАСЧЕТ ΔGтº ХИМИЧЕСКОЙ РЕАКЦИИ ОБРАЗОВАНИЯ
СОЕДИНЕНИЯ CuFe2O4
.1 РАСЧЕТ ΔG400º
4.1.1 Расчет ΔG400º реакции по уравнению Гиббса (первый метод)
1) Определяем энтальпию реакции при 298
К.
DH0298
= DH0298(CuFe2O4) - DH0298(CuO) -2•DH0298(FeO) = -959 + 157,03 + +2•266,65=
-268,67 кДж•моль-1.
2) Вычисляем изменение коэффициентов зависимости теплоемкости от температуры: Da, Db, Dc´.
Da = 138,62 - 43,83 - 51,82 = 42,97.
D b = (119,41 - 16,76 +6,78)•10-3 = 109,43•10-3.
Dc´= (22,76 - 5,88 + 1,59)•105 = 18,47•105.
3) Рассчитываем энтропию реакции при 298 К.
DS0298 = S0298 (CuFe2O4) - S0298 (CuO) - 2•S0298(FeO) = 141 - 42,63 - 2•59,44 = -20,51 Дж•моль-1•К-1
4) Находим значения величин интеграла.
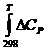 dT = (42,97•400 + 0,5•109,43•10-3•4002 -
18,47•105•400-1) -
dT = (42,97•400 + 0,5•109,43•10-3•4002 -
18,47•105•400-1) -
(42,97•298 + 0,5•109,43•10-3•2982 - 18,47•105•298-1) = 9858,9 Дж•моль-1•К-1.
) Находим значения величины интеграла.
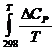 dT = (42,97•ln400 + 109,43•10-3•400 -
0,5•18,47•105•400-2) -
dT = (42,97•ln400 + 109,43•10-3•400 -
0,5•18,47•105•400-2) -
(42,97•ln298 + 109,43•10-3•298 - 0,5•18,47•105•298-2) = 28,4 Дж•моль-1•К-1
6) Рассчитываем значение величины изобарно-изотермического потенциала реакции при температуре 600 К.
DG0400 = -268670 + 9858,9 + 400•20,51 - 400•28,4 = -261967 Дж•моль-1•К-1 =
= -261,9 кДж•моль-1•К-1
1) Определяем изобарно-изотермический потенциал реакции при 298 К.
DG 0298 = -268670 + 298•20,51 = -262558 Дж•моль-1•К-1.
) Вычисляем постоянную интегрирования DH0.
DH0 = -268670 - 42,97•298 - 0,5•109,43•10-3•2982 + 18,47•105•298-1 = - 280136 Дж•моль-1.
) Находим постоянную интегрирования у.
у•298 = -262558 + 280136+ 42,97•298•ln298 + 0,5•109,43•10-3•2982 + 0,5•18,47•105•298-1 = 98487,53;
у = 330,5.
) Рассчитываем значение изобарно-изотермического потенциала реакции при 400 К.
DG0400 = - 280136 - 42,97•400•ln400 - 0,5•109,43•10-3•4002 - 0,5•18,47•105•400-1 + 330,5•400 = -261980 Дж/моль = -261,9 кДж•моль-1.
Полученное значение величины изобарно-изотермического потенциала, DG0400 = -261,9 кДж•моль-1, позволяет
сделать заключение о термодинамической вероятности, то есть возможности
протекания реакций образования соединения CuFe2O4 при
температуре 400 К.
4.2 РАСЧЕТ ΔG500º
4.2.1 Расчет ΔG500º реакции по уравнению Гиббса (первый метод)
1) Определяем энтальпию реакции при 298
К.
DH0298
= DH0298(CuFe2O4) - DH0298(CuO) -2•DH0298(FeO) = -959 + 157,03 + +2•266,65=
-268,67 кДж•моль-1.
2) Вычисляем изменение коэффициентов зависимости теплоемкости от температуры: Da, Db, Dc´.
Da = 138,62 - 43,83 - 51,82 = 42,97.
D b = (119,41 - 16,76 +6,78)•10-3 = 109,43•10-3.
Dc´= (22,76 - 5,88 + 1,59)•105 = 18,47•105.
3) Рассчитываем энтропию реакции при 298 К.
DS0298 = S0298 (CuFe2O4) - S0298 (CuO) - 2•S0298(FeO) = 141 - 42,63 - 2•59,44 = -20,51 Дж•моль-1•К-1
4) Находим значения величин интеграла.
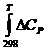 dT = (42,97•500 + 0,5•109,43•10-3•5002 -
18,47•105•500-1) -
dT = (42,97•500 + 0,5•109,43•10-3•5002 -
18,47•105•500-1) -
(42,97•298 + 0,5•109,43•10-3•2982 - 18,47•105•298-1) = 20003,8 Дж•моль-1•К-1
) Находим значения величины интеграла.
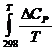 dT = (42,97•ln500 + 109,43•10-3•500 -
0,5•18,47•105•500-2) -
dT = (42,97•ln500 + 109,43•10-3•500 -
0,5•18,47•105•500-2) -
(42,97•ln298 + 109,43•10-3•298 - 0,5•18,47•105•298-2) = 51 Дж•моль-1•К-1
6) Рассчитываем значение величины изобарно-изотермического потенциала реакции при температуре 500 К.
DG0500 = -268670 + 20003,8 + 500•20,51 - 500•51 = -263911 Дж•моль-1•К-1 =
= -263,9 кДж•моль-1•К-1
4.2.2 Расчет DG0500 по уравнению Гиббса-Гельмгольца (второй метод)
1) Определяем изобарно-изотермический потенциал реакции при 298 К.
DG 0298 = -268670 + 298•20,51 = -262558 Дж•моль-1•К-1.
) Вычисляем постоянную интегрирования DH0.
DH0 = -268670 - 42,97•298 - 0,5•109,43•10-3•2982 + 18,47•105•298-1 =
= - 280136 Дж•моль-1.
) Находим постоянную интегрирования у.
у•298 = -262558 + 280136+ 42,97•298•ln298 + 0,5•109,43•10-3•2982 + 0,5•18,47•105•298-1 = 98487,53;
у = 330,5.
) Рассчитываем значение изобарно-изотермического потенциала реакции при 500 К.
DG0500 = - 280136 - 42,97•500•ln500 - 0,5•109,43•10-3•5002 - 0,5•18,47•105•500-1 + 330,5•500 = -263933 Дж•моль-1= -263,9 кДж•моль-1.
Полученное значение величины изобарно-изотермического потенциала, DG0500 = -263,9 кДж•моль-1, позволяет
сделать заключение о термодинамической вероятности, то есть возможности
протекания реакций образования соединения CuFe2O4 при
температуре 500 К.
.3 РАСЧЕТ ΔG600º
4.3.1 Расчет ΔG600º реакции по уравнению Гиббса (первый метод)
1) Определяем энтальпию реакции при 298 К.
DH0298
= DH0298(CuFe2O4) - DH0298(CuO) -2•DH0298(FeO) = -959 + 157,03 + +2•266,65=
-268,67 кДж•моль-1.
2) Вычисляем изменение коэффициентов зависимости теплоемкости от температуры: Da, Db, Dc´.
Da = 138,62 - 43,83 - 51,82 = 42,97.
D b = (119,41 - 16,76 +6,78)•10-3 = 109,43•10-3.
Dc´= (22,76 - 5,88 + 1,59)•105 = 18,47•105.
3) Рассчитываем энтропию реакции при 298
К.
DS0298 = S0298 (CuFe2O4) - S0298 (CuO) - 2•S0298(FeO) = 141 -
42,63 - 2•59,44 = -20,51 Дж•моль-1•К-1
) Находим значения величин интеграла.
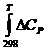 dT = (42,97•600 + 0,5•109,43•10-3•6002 -
18,47•105•600-1) -
dT = (42,97•600 + 0,5•109,43•10-3•6002 -
18,47•105•600-1) -
(42,97•298 + 0,5•109,43•10-3•2982 - 18,47•105•298-1) = 30935,1 Дж•моль-1•К-1.
) Находим значения величины интеграла.
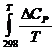 dT = (42,97•ln600 + 109,43•10-3•600 -
0,5•18,47•105•600-2) -
dT = (42,97•ln600 + 109,43•10-3•600 -
0,5•18,47•105•600-2) -
(42,97•ln298 + 109,43•10-3•298 - 0,5•18,47•105•298-2) = 70,95 Дж•моль-1•К-1.
6) Рассчитываем значение величины изобарно-изотермического потенциала реакции при температуре 600 К.
DG0600 = -268670 + 30935,1 + 600•20,51 - 600•70,95 = -267999 Дж•моль-1•К-1= -267,9 кДж•моль-1•К-1.
4.3.2 Расчет DG0600 по уравнению Гиббса-Гельмгольца (второй метод)
1) Определяем изобарно-изотермический потенциал реакции при 298 К.
DG 0298 = -268670 + 298•20,51 = -262558 Дж•моль-1•К-1
) Вычисляем постоянную интегрирования DH0.
DH0 = -268670 - 42,97•298 - 0,5•109,43•10-3•2982 + 18,47•105•298-1 = - 280136 Дж•моль-1.
) Находим постоянную интегрирования у.
у•298 = -262558 + 280136+ 42,97•298•ln298 + 0,5•109,43•10-3•2982 + 0,5•18,47•105•298-1 = 98487,53;
у = 330,5.
) Рассчитываем значение изобарно-изотермического потенциала реакции при 600 К.
DG0600 = - 280136 - 42,97•600•ln600 - 0,5•109,43•10-3•6002 - 0,5•18,47•105•600-1 + 330,5•600 = -267998 Дж•моль-1= -267,9 кДж•моль-1.
Полученное значение величины изобарно-изотермического потенциала, DG0600 = -267,9 кДж•моль-1, позволяет сделать заключение о термодинамической вероятности, то есть возможности протекания реакций образования соединения CuFe2O4 при температуре 600 К.
4.4.1 Расчет ΔG700º реакции по уравнению Гиббса (первый метод)
1) Определяем энтальпию реакции при 298
К.
DH0298 = DH0298(CuFe2O4) - DH0298(CuO) -2•DH0298(FeO) = -959 + 157,03 + +2•266,65= -268,67 кДж•моль-1.
2) Вычисляем изменение коэффициентов зависимости теплоемкости от температуры: Da, Db, Dc´.
Da = 138,62 - 43,83 - 51,82 = 42,97.
D b = (119,41 - 16,76 +6,78)•10-3 = 109,43•10-3.
Dc´= (22,76 - 5,88 + 1,59)•105 = 18,47•105.
3) Рассчитываем энтропию реакции при 298 К.
DS0298 = S0298 (CuFe2O4) - S0298 (CuO) - 2•S0298(FeO) = 141 - 42,63 - 2•59,44 = -20,51 Дж•моль-1•К-1
4) Находим значения величин интеграла.
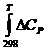 dT = (42,97•700 + 0,5•109,43•10-3•7002 -
18,47•105•700-1) -
dT = (42,97•700 + 0,5•109,43•10-3•7002 -
18,47•105•700-1) -
(42,97•298 + 0,5•109,43•10-3•2982 - 18,47•105•298-1) = 42784,8 Дж•моль-1•К-1.
) Находим значения величины интеграла.
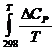 dT = (42,97•ln700 + 109,43•10-3•700 -
0,5•18,47•105•700-2) -
dT = (42,97•ln700 + 109,43•10-3•700 -
0,5•18,47•105•700-2) -
(42,97•ln298 + 109,43•10-3•298 - 0,5•18,47•105•298-2) = 89,2 Дж•моль-1•К-1.
6) Рассчитываем значение величины изобарно-изотермического потенциала реакции при температуре 700 К.
DG0700
= -268670 + 42784,8 + 700•20,51 - 700•89,2 = -273968 Дж•моль-1•К-1= -273,9
кДж•моль-1•К-1
4.4.2 Расчет DG0700 по уравнению Гиббса-Гельмгольца (второй метод)
1) Определяем изобарно-изотермический потенциал реакции при 298 К.
DG 0298 = -268670 + 298•20,51 = -262558 Дж•моль-1•К-1
) Вычисляем постоянную интегрирования DH0.
DH0 = -268670 - 42,97•298 - 0,5•109,43•10-3•2982 + 18,47•105•298-1 = - 280136 Дж•моль-1.
) Находим постоянную интегрирования у.
у•298 = -262558 + 280136+ 42,97•298•ln298 + 0,5•109,43•10-3•2982 + 0,5•18,47•105•298-1 = 98487,53;
у = 330,5.
) Рассчитываем значение изобарно-изотермического потенциала реакции при 700 К.
DG0700 = - 280136 - 42,97•700•ln700 - 0,5•109,43•10-3•7002 - 0,5•18,47•105•700-1 + 330,5•700 = -273966 Дж•моль-1= -273,9 кДж•моль-1.
Полученное значение величины изобарно-изотермического потенциала, DG0700 = -273,9 кДж•моль-1, позволяет
сделать заключение о термодинамической вероятности, то есть возможности
протекания реакций образования соединения CuFe2O4 при
температуре 700 К.
.5 ЗАКЛЮЧЕНИЕ
Результаты расчетов изменения изобарно-изотермического потенциала DG0т, полученные по уравнению Гиббса и
уравнению Гиббса-Гельмгольца для реакции образования CuFe2O4,
приведены в таблице 3. Графическая зависимость DG0т=f(T) показана на рисунке 2.
Таблица 3 - Значения величины DG0т реакции образования CuFe2O4
|
Т, К |
298 |
400 |
500 |
600 |
700 |
|
DG0т, кДж•моль-1 |
-262,5 |
-261,9 |
-263,9 |
-267,9 |
-273,9 |
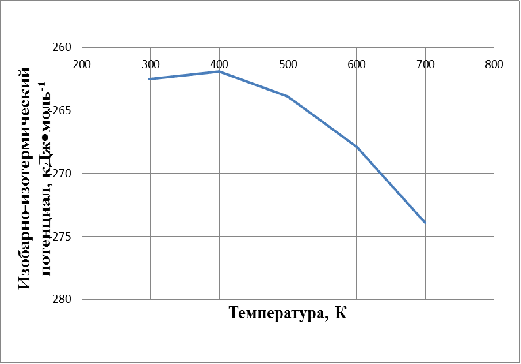
Рисунок 2 ˗ Зависимость изобарно-изотермического потенциала от
температуры
Как показывают полученные результаты, реакция образования CuFe2O4 протекает в интервале температур от 298 до 700 К при стандартном давлении, с увеличением температуры её вероятность убывает в интервале температур от 298 до 400 К и возрастает в интервале температур от 400 до 700 К.
ВЫВОД
Термодинамический анализ системы «CuO ˗˗ FeO» и
системы «CuO ˗˗ 2FeO» в интервале температур 298…700 К
показывает, что энергетически наиболее вероятно протекание реакции образования CuFe2O4 (DG0т= ˗262,5…˗273,9
кДж•моль-1). Реакция образования CuFeO2
будет протекать во вторую очередь (DG0т= ˗164,9…˗161,2 кДж•моль-1).
Список литературы
1. Хомич В.А. Термодинамические расчеты: метод. указания к курсовой работе по физической химии для студентов специальности 330200 « Инженерная защита окружающей среды». - Омск: Изд-во СибАДИ, 2005. - 14 с.
. Бобкова Н.М., Силич Л.М., Терещенко И.М. Сборник задач по физической химии силикатов и тугоплавких соединений: учеб. пособие для вузов. - Минск: «Университетское», 1990. - 175 с.
. Кругляков П.М. Физическая и коллоидная химия: учебное пособие / П.М. Кругляков, Т.Н. Хаскова. 2-ое изд., испр. ˗ М.: Высшая школа, 2007. ˗ 319 с.
. Краткий справочник физико-химических величин: учебное пособие / Ред. А.А. Равдель, А.М. Пономарева. ˗ 11˗е изд., испр. и доп. ˗ М.: As˗book, 2009. ˗ 240 с.