Материал: Свойства аренов
Свойства аренов
Федеральное государственное автономное образовательное учреждение
высшего профессионального образования
«Национальный исследовательский технологический университет «МИСиС»
Новотроицкий филиал
Реферат
по органической химии
По теме: «Свойства аренов»
Выполнил студент группы
ХТ-12-22 Тимофеева Е.В.
Проверил преподаватель:
Саблин А.В.
Новотроицк
Содержание
Введение
Глава 1.Получение ароматических углеводородов и их свойства
Глава 2. Химические свойства ароматических углеводородов
Заключение
Список литературы
Введение
Ароматические углеводороды , арены - органические соединения карбоциклического ряда, молекулы которых содержат бензольное кольцо С6Н6 (моно- и полициклические функциональные производные бензола).
Бензол был открыт М.Фарадеем в 1825г., он же установил его формулу. В 1865 г. А. Кекуле предложил структурную формулу бензола, в которой в шестичленном кольце изобразил три чередующиеся =. Но это не истинно двойные связи, это только условное обозначение общих шести электронов, в одинаковой степени принадлежащих всем шести атомам углерода. Доказательствами отсутствия непредельности в ароматическом кольце являются следующие факты:
а) Алкены, содержащие =, обесцвечивают бромную воду и раствор KMnO4, бензол не обесцвечивает указанные растворы;
б) Для бензола характерны реакции замещения аналогично алканам, а не присоединения, как для алкенов;
в) Длина одинарной связи 0,154 нм, двойной связи - 0,134 нм. В бензоле длина всех связей одинаковая, равна 0,140 нм.
В молекулах бензола нет чередования - и = связей, а есть «полуторная»,
особая связь. Атом С в молекуле бензола находится в Sp2-гибридном состоянии: 3 σ
-связи, образованные
перекрыванием трех гибридных орбиталей + единая π-электронная система, общая для всех
атомов С.
Глава 1.Получение ароматических углеводородов и их свойства.
Известны следующие способы получения ароматических углеводородов:
) Каталитическая дегидроциклизация алканов, т.е. отщепление водорода с одновременной циклизацией (способ Б.А.Казанского и А.Ф.Платэ). Реакция осуществляется при повышенной температуре с использованием катализатора, например оксида хрома.
) Каталитическое дегидрирование циклогексана и его производных
(Н.Д.Зелинский). В качестве катализатора используется палладиевая чернь или
платина при 300°C.

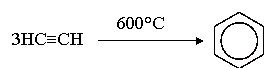
) Циклическая тримеризация ацетилена и его гомологов над активированным углем при 600°C (Н.Д.Зелинский).
) Сплавление солей ароматических кислот со щелочью или натронной известью.
Толуо́л - метилбензол, бесцветная жидкость
<#"822995.files/image003.gif">
Реакция
Гриньяра
<#"822995.files/image004.gif">
образуется смесь изомеров гексахлорциклогексана.
· Взаимодействие с бромом (чистый):
С6H6 + Br2 -(FeBr3 или AlCl3)→ С6H5Br + HBr
образуется бромбензол.
· Взаимодействие
с галогенопроизводными алканов (алкилирование бензола, -реакция Фриделя
Крафтса
<#"822995.files/image005.gif">метилбензол 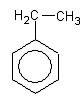 этилбензол
этилбензол  1,2-диметилбензол
1,2-диметилбензол
Согласно номенклатуре ИЮПАК, арены с одним бензольным кольцом рассматривают как производные бензола. В качестве главной цепи выбирают бензольное кольцо. Многие арены имеют свои исторические названия.
Например:


изопропилбензол винилбензол
Нумерацию начинают с одного из заместителей так, чтобы сумма номеров заместителей была минимальна.
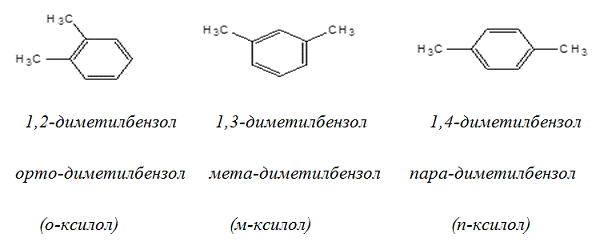
Если соединение содержит два заместителя у бензольного кольца, то
располагаться они могут тремя разными способами друг относительно друга. Часто
вместо нумерации для 1,2-дизамещенных бензолов используют обозначение орто-,
для 1,3-замещенных - мета-, а для 1,4-замещенных - пара-.
2.
Изомерия аренов <#"822995.files/image011.gif">
Им изомерны также метилэтилбензолы (приведем в пример один из них), а также пропил- и изопропилбензолы:
У аренов есть и межклассовые изомеры - соединения с несколькими двойными и тройными связями, циклы и т.п.
3.
Физические свойства аренов
<#"822995.files/image012.gif">
Арены похожи на остальные углеводороды - они нерастворимы в воде и легче ее. Бензол при комнатной температуре - бесцветная прозрачная жидкость со своеобразным запахом. Тпл = 5,5оС, Ткип = 80оС.
Бензол токсичен и легко воспламеняется.
.
Получение аренов
<#"822995.files/image013.gif">
.
Тримеризация алкинов.
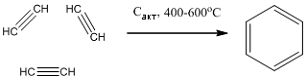
Глава 2. Химические свойства ароматических углеводородов
ароматический углеводород молекула реакция
Арены имеют склонность к реакциям замещения. Бензольное кольцо устойчиво к окислению.
. Реакции электрофильного замещения.
Подвижные π-электроны, образующие электронное облако, способны активно взаимодействовать с электрофильными реагентами (заряженными +).
Механизм реакции:стадия - образование электрофильной частицы А+ из
реагента А : В путем гетеролитического распада молекулы.
А:ВàА++:В-
стадия - взаимодействие электрофильной частицы А+ с π-электронным облаком
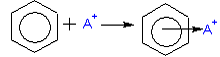 π-комплекс или
π-комплекс или 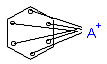
Особенность этой стадии в том, это частица А+ пока ещё не образует настоящей химической связи с определенным атомом С бензольного кольца;π-комплекс-неустойчивстадия - образование σ-комплекса

σ-комплекс
Для того, чтобы образовать химическую связь между частицей А+ и атомом С
бензольного кольца, нужна пара электронов. Их предоставляют два соседних атома
С. Один электрон отдаёт тот атом С, к которому присоединена частица А+, а
другой - соседний атома С.У него появляется + заряд. Таким образом,
ароматическая система оказывается разрушенной. Оставшиеся 4 электрона
распределяются между 5 атомами С, между ними распределяется и + заряд. Молекула
неустойчива, поэтому она вынуждена отдать Н+, чтобы вернуться в прежнее
ароматическое состояние.стадия - отщепление Н+ от σ
- комплекса и возврат
катализатора в исходную форму:
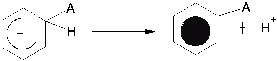
Н++:В-àH-B
Примеры реакций электрофильного замещения (SE ) и их механизм:
а)Реакция хлорирования бензола:
Механизм:
+Cl2<==>Cl++FeCl-4
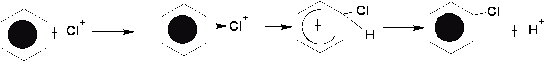
++FeCl4àFeCl3+HCl
)Реакция нитрования бензола:
С6Н6+HNO3H2SO4>C6H5-NO2+H2O нитробензол.
Механизм:
HNO3+H2SO4<==>NO+2+H3O++2HSO-4
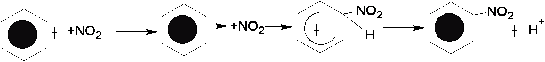
++HSO-4àH2SO4
с)Реакция сульфирования бензола:
С6Н6+H2SO4_____>C6H5-SO3H+H2O бензолсульфокислота
Механизм:
SO4+SO3<==>HSO+3+HSO-4
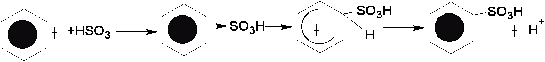
H++HSO4àH2SO4
)Реакция алкилирования
бензола олефинами, например, пропиленом:
С6Н6+СН3-CH2=СН2→C6H5СН(СН3)2
Механизм:
SO4↔H++HSO-4
δ+δ-
СН3àCH=СН2+H+àCH3-CH+-CH3

++HSOà4àH2SO4
. Реакции присоединения
Протекают с трудом, при
высокой температуре и в присутствии катализатора.
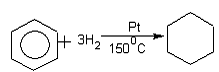 циклогексан
циклогексан
С6Н6+3Cl2----hν,40ºC----→C6H6Cl6 гексахлорциклогексан
. Реакции окисления
Бензол не окисляется KМnO4;Cr2O3.
Толуол окисляется KМnO4.
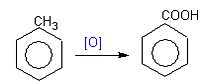 бензойная кислота
бензойная кислота
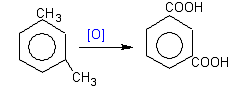 терефталевая
кислота
терефталевая
кислота
Независимо от длины боковой
цепи при окислении образуются СООН-группы. В том случае, если в молекуле
ароматического соединения есть несколько боковых радикалов, то их окисление
происходит постепенно.
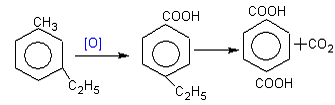 терефталевая
к-та.
терефталевая
к-та.

Заключение
Ароматические углеводороды являются важным сырьем для производства различных синтетических материалов, красителей, физиологически активных веществ. Так, бензол - продукт для получения красителей, медикаментов, средств защиты растений и др. Толуол используется как сырье в производстве взрывчатых веществ, фармацевтических препаратов, а также в качестве растворителя. Винилбензол (стирол) применяется для получения полимерного материала - полистирола.
Список литературы
1. Рудзитис Г.Е. Химия. Основы общей химии. 10 класс: учебник для общеобразовательных учреждений: базовый уровень / Г. Е. Рудзитис, Ф.Г. Фельдман. - 14-е издание. - М.: Просвещение, 2012.
. Химия. 10 класс. Профильный уровень: учеб. для общеобразоват. учреждений/ В.В. Еремин, Н.Е. Кузьменко, В.В. Лунин и др. - М.: Дрофа, 2008. - 463 с.
. Химия. 11 класс. Профильный уровень: учеб. для общеобразоват. учреждений/ В.В. Еремин, Н.Е. Кузьменко, В.В. Лунин и др. - М.: Дрофа, 2010. - 462 с.
. Хомченко Г.П., Хомченко И.Г. Сборник задач по химии для поступающих в вузы. - 4-е изд. - М.: РИА «Новая волна»: Издатель Умеренков, 2012. - 278 с.
Дополнительные рекомендованные ссылки на ресурсы сети Интернет :
. Interneturok.ua
. Интернет-портал Prombud.ua