Материал: Структурная организация молекул нуклеиновых кислот
1) молярная доля пуринов
<#"823465.files/image012.gif">
) количество аденина
<#"823465.files/image013.gif">
) количество аденина <#"823465.files/image014.gif">
4) существенным для характеристики
вида (таксономическое значение) оказался так называемый коэффициент
специфичности <#"823465.files/image015.gif">
Это отношение часто выражают в молярных процентах (Г + Ц), или процентах ГЦ-пар. Для животных и большинства растений этот коэффициент ниже 1 (от 0,54 до 0,94), у микроорганизмов <#"823465.files/image016.gif">
Рис. 10. Фосфодиэфирная связь
между нуклеотидами.
Второй, разработанный А. Максамом и В.
Гильбертом, сводится к химической модификации пуриновых и пиримидиновых
оснований в ДНК, избирательном расщеплении фосфодиэфирных связей по месту
модифицированных оснований, разделении продуктов расщепления электрофорезом в
полиакриламидном геле и прямому считыванию структуры фрагмента ДНК с полученных
электрофореграмм (число полос на электрофореграмме продуктов расщепления
фрагмента ДНК с модифицированным азотистым основанием равно числу нуклеотидных
остатков, содержащих этот пурин или пиримидин, а их положение на
электрофореграмме указывает место этого нуклеотидного остатка в анализируемом
фрагменте ДНК).
3.3 Вторичная структура НК
В соответствии с моделью Дж.
Уотсона и Ф. Крика, предложенной в 1953 г. на основании ряда аналитических
данных, а также рентгеноструктурного анализа молекула ДНК состоит из двух
цепей, образуя правовращающую спираль, в которую обе полинуклеотидные цепи закручены
вокруг одной и той же оси. Удерживаются цепи благодаря водородным связям,
образующимся между их азотистыми основаниями. Обе цепи полинуклеотидов в
биспиральной молекуле ДНК имеют строго определенное пространственное
расположение, при котором азотистые основания находятся внутри, а фосфорные и
углеводные компоненты - снаружи.
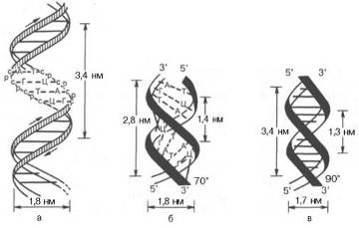
Рис. 11. Схематическое изображение двойной спирали <#"823465.files/image018.gif">
Рис. 12. Две формы Na-соли ДНК
Позднее была открыта С-форма. В
таблице приведены характеристики А-, В-, С-форм ДНК. Они различаются значениями
шага двойной спирали, углами поворота между соседними парами оснований и наклоном
пар к оси спирали.
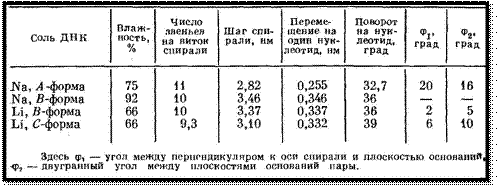
Конформация полинуклеотидной цепи
определяется набором углов поворота, показанных на рисунке:
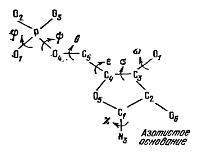
Углы отсчитываются следующим образом: если смотреть вдоль связи, вокруг которой происходит вращение, то дальняя связь вращается по часовой стрелке относительно ближней. Отсчет от цис-положения связей.
Конформация полинуклеотидной цепи зависит от конформации сахара - рибозы или дезоксирибозы. Сахар встречается в четырех конформациях, различающихся тем, какой из атомов пятичленного цикла, С2 или С3 (на рисунке) выведен из плоскости остальных четырех атомов. Если атом С2 (или С3) находится по ту же сторону от плоскости, что и С5, то конформация именуется эндо, в противоположном случае - экзо. Возможны, следовательно, С2-эндо, С3-эндо, С2-экзо и С3-экзо-формы. Первые две встречаются чаще.
Эксперимент (диффузное рассеяние
рентгеновских лучей, КД и т.д.) и теория показали, что следует говорить не об
отдельных конформациях А, В, С ДНК, а о конформационных семействах А и В.
С-форма, а также Т- и D-формы сходны с В-формой и относятся
к В-семейству. Двойная спираль оказывается структурой, способной к непрерывному
изменению конформации. В пределах семейств А и В конформации меняются
некооперативно, вероятно, путем плавного изменения параметров спирали.
Напротив, переход от одного семейства к другому, АàВ,
происходит резко, кооперативно и сопровождается скачкообразным изменением
конформации сахара от 3-эндо к 2-эндо. Сведения о конформационной структуре
нуклеиновых кислот получаются непосредственно из данных рентгеноструктурного
анализа монокристаллов олигонуклеотидов. На рисунке показаны структуры двух
форм ДНК - В и Z.
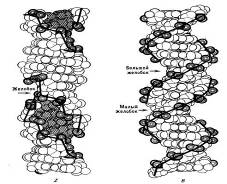
Рис. 13. Z и В-формы
ДНК.
Двойная спираль ДНК в любой возможной ее конформации характеризуется широкой и узкой спиральными бороздками, выемками на поверхности макромолекулы.
Двойные спирали ДНК в А-, В-, С-формах - правые. Позднее была открыта левая двойная спираль ДНК. Так как она зигзагообразна, эта форма была названа Z-формой. Z-формы образуются цепями из чередующихся пуринов и пиримидинов. ДНК стабилизируются в Z-форме при высокой концентрации соли или в результате бромирования или метилирования.
Работа с синтетическими ДНК показала, что последовательности пурин-пиримидин могут испытывать переходы от правой В-формы к левой Z-форме, в зависимости от концентрации соли или химической модификации - от метилирования. Такие переходы обратимы. Метилирование и демитилирование, по-видимому, существенны для контроля активности генов.
Возможно и то, что конформационные превращения ДНК существенны для ее функционирования, для взаимодействия с ферментами (полимеразы), для регуляции действия генов и т.д.
Очевидно, что имеются две возможности организации двойной спирали - из параллельных и антипараллельных цепей. Справедливость второй модели доказана рентгенографическими и биохимическими данными. Цепи в двойной спирали антипараллельны.
Специфическая двуспиральная
структура ДНК непосредственно объясняет важные факты - репликацию ДНК при
митозе и метаболическую устойчивость ДНК. При репликации двойная спираль
сначала разделяется вследствие разрыва водородных связей и раскручивания цепей.
Каждая из них служит матрицей для сборки новой цепи, комплементарной к матрице.
Мономеры новой цепи соединяются с матрицей, образуя уотсон-криковские пары АТ,
ТА, ГЦ и ЦГ. Одновременно происходит поликонденсация нуклеозидтрифосфатов, и в
результате образуются две двойные спирали, тождественные первоначальной. Такая
полуконсервативная модель (новая спираль содержит одну старую и одну новую
цепь) действительно подтверждается опытом. Ошибки при репликации являются точечными
мутациями. Наибольший гипохромизм, т.е. наибольшая степень двуспиральности,
наблюдается при составе смеси полинуклеотидов 1:1.
.4 Оптические характеристики
нуклеиновых кислот
Интенсивное поглощение нуклеиновых кислот в УФ-области спектра обусловлено пуриновыми и пиримидиновыми основаниями. Спектры поглощения отдельных оснований сливаются в одну широкую полосу и дают характерное поглощение НК с лmax= 260 нм.
Квантово-механические расчеты
показали, что интенсивное поглощение света пуриновыми и пиримидиновыми
основаниямипри 260 нм связано с рàр*-
переходами. Определенный вклад в это поглощение вносят nàр-переходы.
Коэффициент молярной экстинции е260 для нуклеиновых кислот почти на
порядок больше, чем е280 для белков. Оптические свойства хромофорных
групп зависят от конформации ДНК. После тепловой денатурации оптическая
плотность D увеличивается примерно на 30%. Явление, связанное с увеличением
оптической плотности НК, называется гиперхромным эффектом. Уменьшенное
поглощение нативных препаратов ДНК есть гипохромный эффект.
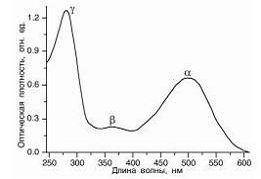
Рис. 14. Спектр поглощения ДНК.
На основании линейной зависимости температуры плавления ДНК от содержания ГЦ-пар гиперхромный эффект пытались объяснить разрывом водородных связей. Но исследования одноцепочечных полинуклеотидов показали, что стабилизацию двойной спирали невозможно объяснить только горизонтальными взаимодействиями комплементарных пар, стабилизированных водородными взаимодействиями. Оказалось, что спектры поглощения поли-А и АМФ в водном растворе, содержащем одинаковое количество нуклеотидов, значительно отличаются. Интегральное поглощение поли-А существенно меньше, чем поглощение составляющих его мономеров АМФ, т.е. для поли-А наблюдается гипохромный эффект, аналогичный и для нативной ДНК. Для поли-А при увеличении температуры наблюдается гиперхромный эффект.
В том же температурном интервале для АМФ не наблюдается гиперхромного эффекта. На основании этих экспериментальных данных сделано заключение, что наряду с горизонтальными взаимодействиями имеют место вертикальные взаимодействия между основаниями. Анализ упорядоченной структуры ДНК показывет, что плоскости оснований, следующие друг за другом вдоль оси спирали, практически параллельны. Компланарное расположение (стэкинг) оснований обусловливает вертикальные взаимодействия и вызывает гипохромный эффект в нативной ДНК и в модельном полинуклеотиде (поли-А) при низкой температуре.
Наибольшая энергия вертикальных стэкинг-взаимодействий с таким расположением вдоль оси спирали комплементарных пар: ↓ЦГ и ↑ГЦ. Она составляет - 82,8 кДж*моль-1. Наименьшая энергия (6,7 кДж*моль-1) отвечает стэкингу ↑АТ и ↓ТА-пар. Участки ДНК, содержащие АТ-пары, менее стабильны и быстрее денатурируются, чем участки, содержащие ГЦ-пары. Гиперхромный эффект обусловлен разрушением структуры ДНК и нарушением стэкинга оснований.
Зависимость оптической
плотности D260 ДНК от температуры называется кривой плавления ДНК. В
области низких температур для нативных молекул ДНК характерен гипохромный
эффект, обусловленный стэкинг-взаимодействиями между основаниями. Тепловая
денатурация ДНК происходит в узком температурном интервале и сопровождается
гиперхромным эффектом. Из кривых плавления ДНК определяется важная
характеристика - температура плавления Тп. Это - температура, при
которой гиперхромный эффект составляет D260/2.
3.5 Третичная структура ДНК
ДНК имеют формы: линейная, кольцевая, 2-х и 1- цепочечная.
Двуцепочечные ДНК с «липкими» концами могут образовывать кольцо, которое далее ковалентно сшивается по сахарофосфатной цепи при помощи ДНК-лигазы.
Третичная структура ДНК у эукариотических клеток отличается тем, что многократная спирализация ДНК сопровождается образованием комплексов с белками.
хромосом (хроматид) человека организованы в 23
пары. Средняя длина хромосомы составляет 130 млн. пар оснований (п. о.) и имеет
длину 5 см. Хромосома № 1 - 263 млн. п. о., хромосома № 46 - меньше 50 млн. п.
о. Если проложить все ДНК в В-конформации в линию, то их общая длина превысит 2
метра. Человеческая хромосома 16 имеет 2,5 мкм в длину, а длина самой ДНК - 3,7
см.
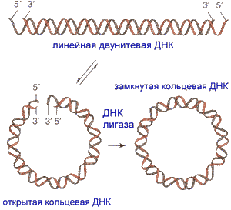
Рис. 15. Линейная, кольцевая третичные структуры
ДНК.
Понятно, что уместить такой длины ДНК в ядре
возможно только путем ее определенной упаковки. При образовании третичной
структуры ДНК человека происходит в среднем уменьшение ее размеров в 100 тысяч
раз.
Заключение
Нуклеиновым кислотам принадлежит очень важная роль в обеспечении специфического синтеза биополимеров в организме человека, животных, растений и микробов. В ядре клетки расположены хромосомы. В свою очередь, хромосомы состоят из двух частей, соединенных перемычкой. В каждой из этих частей находится хроматин. Он склонен образовывать спиралеобразные нити - хроматиды, перед делением клетки. В хроматидах содержится ДНК. Какой компактной должна быть структура ДНК, чтобы вместиться в хромосому! Именно в ней и содержится наследственная информация или ген. ДНК имеет структуру закрученных ступенек и определяется, как двойная закрученная спираль. Ее составляют две очень тонкие нити, соединенные перемычками. Единицей этой структуры является нуклеотид. Нуклеотид включает в себя 3 компонента: сахар, остаток фосфорной кислоты и азотистого основания (тимин, аденин, цитозин а также гуанин). Ступеньки спиральной лестницы как раз образованы последним, т.е. соединением аденин с тимином и цитозин с гуанином, причем их связь водородная. Перилами же лестницы являются остатки фосфорной кислоты, а сахар - это связующая в общей цепи молекулы ДНК. Гены или отдельные фрагменты составляют молекулу ДНК. Репликация ДНК Прямо перед делением клетки посредством митоза, ее ДНК реплицируется, т.е. удваивается.
Структура двойной спирали характерна для подавляющего большинства ДНК. Но в настоящее время известны разные конформации молекулы ДНК.
Спектры поглощения растворов ДНК позволяют выяснить оптическую плотность ДНК, Т плав.
Измерение спектра поглощения раствора ДНК
проводят на спектрофотометре. В свою очередь измерения используются для
последующего расчета концентрации растворов нуклеиновых кислот. Метод определения
концентрации нуклеиновых кислот в растворе основан на существовании у ДНК и РНК
максимума поглощения при длине волны 260 нм. Это означает, что в растворах
нуклеиновых кислот максимальная фотометрическая абсорбция наблюдается при 260
нм и прямо коррелирует с концентрацией ДНК или РНК.
Литература
1. А.С. Спирин Молекулярная биология: Структура и биосинтез нуклеиновых кислот, 1986. - 496с.
. А.Ю. Ершов Общая химия. Биофизическая химия. Химия биогенных элементов. Учебник для вузов, 2003. - 423с.
. А.Я. Николаев Биологическая химия, 2004 - 254с.
. Аппель Б., Бенеке И., Бенсон Я., под ред. С. Мюллер Нуклеиновые кислоты от А до Я, 2012. - 352с.
. В.Ф. Антонов и др. Биофизика: Учебник, 2000. - 288с.
. И.Ф. Шаяхметов. Основы биотехнологии растений: Учебное пособие, 2007. - 136с.
. Л.Н. Стрельникова ред. Химия и жизнь, научно-популярный журнал, 2010. - 68с.
. М.В. Волькенштейн. Биофизика, 1988. - 588с.
. М.В. Волькенштейн. Молекулярная биофизика, 1990. - 650с.
. П.Г. Костюк, Д.М. Гроздинский, В.Л. Зима и др. Биофизика, 1988. - 505с.
. Ревин В.В., Максимов Г.В. Биофизика. Учебник, 2000. - 206с.
. Рубин А.Б. - Биофизика (том 1,2), 2003. - 642с.
. Э. Чаргафф, Дж. Дэвидсон. Нуклеиновые кислоты, 1962. - 456с.
. Ю.А. Владимиров, Д.И. Рощупкин Биофизика, 1999. - 480с.
. Ю.Б. Филиппович Основы биохимии, 1993. - 495с.