Материал: семинар 1
СЕМИНАР 1
Фазовое равновесие в однокомпонентных системах. Процессы испарения и возгонки
Прежде чем начать рассмотрение задач, необходимо познакомиться с таблицей, содержащей основные справочные материалы по данной теме. Это таблица 24 (стр. 30
– 35 справочника А.А. Равделя).
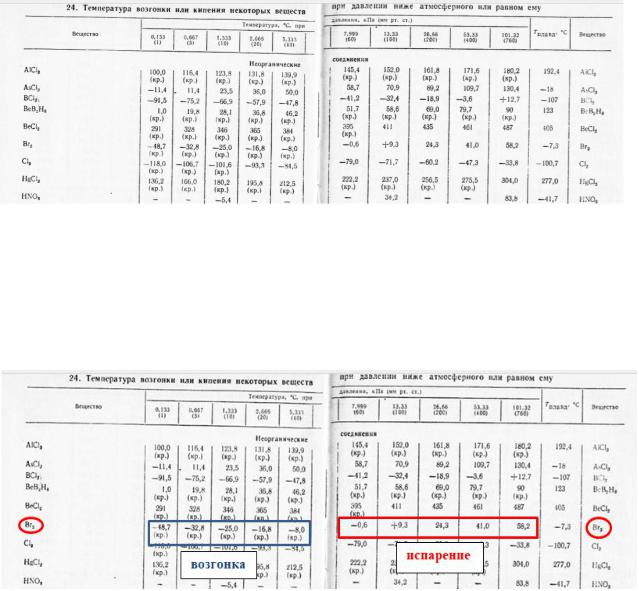
В ней приведены температуры фазовых превращений (испарения и возгонки) различных веществ при разных внешних давлениях. Под температурами возгонки можно увидеть пометку (кр.), то есть речь идет о кристаллическом веществе. Например, для брома:
1
С другой стороны, из таблицы можно узнать давление насыщенного пара (в кПа или мм рт.ст.) над жидкой или твердой фазой при разных температурах:
Если по данным таблицы построить график в координатах |
− |
, то мы |
получим линии испарения и/или возгонки на фазовой диаграмме. |
|
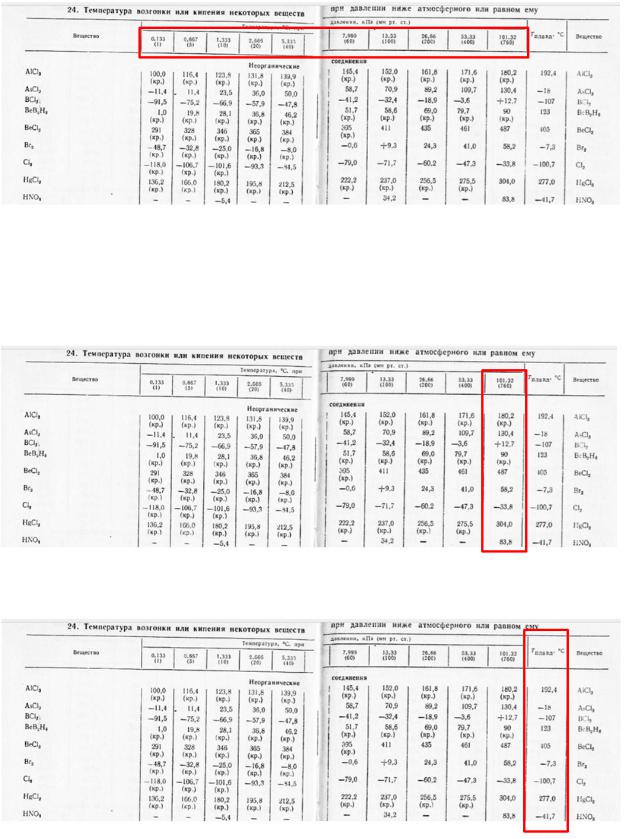
Нормальные температуры кипения веществ находятся в крайнем правом столбце и соответствуют атмосферному давлению (101,32 кПа или 760 мм рт.ст.).
Последний столбец таблицы содержит температуры плавления.
И если температур возгонки и испарения для каждого вещества несколько, так как они зависят от давления, то температура плавления только одна (от давления практически не зависит, и ее можно относить к любому внешнему давлению).
2

Задача 3
В задаче требуется найти изменение энтропии и внутренней энергии при испарении вещества. Уравнение Клапейрона-Клаузиуса позволяет найти теплоту испарения. Поэтому, прежде чем вычислять другие термодинамические функции, сначала необходимо найти ∆исп .
Так как в условии сказано, что «теплоту испарения в интервале температур можно считать постоянной», то тепловой эффект ищем именно средний, используя интегральную форму уравнения Клапейрона-Клаузиуса:
= ∆исп 1 − 1
или
∆исп = −
Для использования этой формулы необходимы две пары данных (давления насыщенного пара жидкости при двух разных температурах). В условии явно нет этих значений, но есть отсылка к справочным данным. Поэтому давления и температуры мы будем брать из таблицы 24, стр. 30 (справочник А.А. Равделя). Кроме того, в условии задан приблизительный температурный интервал температур, на который мы должны ориентироваться для выбора данных из справочника. Наиболее близкие температуры в справочнике (и
соответствующие им давления):
= 26 ( |
= 26 + 273 = 299 К) |
= 60 мм рт. ст. |
= 34,9 ( |
= 34,9 + 273 = 307,9 К) |
= 100 мм рт. ст. |
Именно их мы и подставим в расчетную формулу (не забывая переводить
температуру в Кельвины): |
100 |
|
Дж |
|
∆исп = |
8,314 ∙ 307,9 ∙ 299 |
= 43931,25 |
||
307,9 − 299 |
60 |
моль |
||
На следующем этапе рассчитаем изменение энтропии при заданной указанной температуре 27 :
3

∆исп = ∆исп исп
исп = 27 исп = 27 + 273 = 300 К
Подставляем значения: |
43931,25 |
|
Дж |
|
∆исп = |
= 146,44 |
|||
300 |
моль ∙ К |
Это изменение энтропии при испарении 1 моль вещества. В условии задано другое количество, а именно 1,5 моль. Учитываем это:
∆исп = 146,44 ∙ 1,5 = , |
Дж |
К |
Для расчета внутренней энергии испарения воспользуемся формулой связи изобарного и изохорного тепловых эффектов:
∆исп |
= ∆исп |
+ ∆исп |
∆исп |
= ∆исп |
− ∆исп |
|
∆исп |
= 1 |
∆исп = 43931,25 − 1 ∙ 8,314 ∙ 300 = 41437,05 Дж/моль
Учтём количество вещества: |
, Дж |
∆исп = 1,5 ∙ 41437,05 = |
Внимание! Для обратных фазовых переходов абсолютные значения термодинамических функций остаются такими же, но знак меняется на
противоположный. Например, для конденсации:
∆конд = −∆исп
∆конд = −∆исп
∆конд = −∆исп
∆конд = −∆исп = −1
Задачи для самостоятельного решения: № 1, 2, 4, 5, 6, 7
4

Задача 8
В данной задаче требуется найти теплоту испарения при заданной температуре, т.е. истинный тепловой эффект. В основе расчета лежит дифференциальная форма уравнения Клапейрона-Клаузиуса:
= ∆исп
откуда можно выразить тепловой эффект:
∆исп = |
|
∙ |
|
Вид уравнения аналогичен виду дифференциальной формы уравнения
изобары Вант-Гоффа. И нахождение истинной теплоты испарения проводится по той же схеме, что и расчет истинного теплового эффекта реакции, а именно:
, |
производная по |
|
|
|
|
|
|
|
|
|
|
|
|
∙ |
→ ∆исп = ( ) |
|
|
|
Вусловии дана функциональная зависимость:
=− 3308 + 10,373 − 0,8 ∙
Действуем по предложенной схеме:
2,303 ∙ = −2,303 ∙ 3308 + 2,303 ∙ 10,373 − 2,303 ∙ 0,8 ∙
=−2,303 ∙ 3308 + 2,303 ∙ 10,373 − 0,8 ∙
=+2,303 ∙ 3308 + 0 − 0,8
5