Материал: Роль ФАТ в профилактике ССО

РЕКОМЕНДАЦИИ ПО ЛЕЧЕНИЮ
РОЛЬ ТЕСТИРОВАНИЯ ФУНКЦИОНАЛЬНОЙ АКТИВНОСТИ ТРОМБОЦИТОВ В ПРОФИЛАКТИКЕ СЕРДЕЧНО-СОСУДИСТЫХ ОСЛОЖНЕНИЙ У БОЛЬНЫХ, ПОЛУЧАЮЩИХ АНТИТРОМБОЦИТАРНУЮ ТЕРАПИЮ
Заключение междисциплинарного Совета Экспертов Российского общества ангиологов и сосудистых хирургов, Российского научного общества специалистов по рентгенэндоваскулярной диагностике и лечению, Национальной ассоциации по борьбе с инсультами, Национального научного общества воспаления
Представлено заключение междисциплинарного Совета Экспертов о роли тестирования функциональной активности тромбоцитов в профилактике сердечно-сосудистых осложнений у больных, получающих антитромбоцитарную терапию. Рассмотрены показания к антитромбоцитарной терапии, связь реактивности тромбоцитов на фоне приема антитромбоцитарной терапии с риском развития неблагоприятных событий, а также факторы, обуславливающие высокую остаточную реактивность тромбо-
цитов на фоне приема антитромбоцитарных препаратов. Отдельно рассматриваются результаты исследований по коррекции антитромбоцитарной терапии на основании данных агрегатометрии, показания к ее проведению в клинической практике, а также методы оценки остаточной реактивности тромбоцитов.
Ключевые слова: функциональная активность тромбоцитов, антитромбоцитарная терапия, высокая остаточная реактивность тромбоцитов, агрегатометрия.
Рациональная фармакотерапия в кардиологии 2014;10(6):679-687
The significance of platelet functional activity testing in the prevention of cardiovascular complications in patients receiving antiplatelet therapy
Conclusion of Interdisciplinary Expert Council of Russian Association of Angiologists and Vascular Surgeons, Russian Scientific Society of Endovascular Surgeons and Interventional Radiologists, National Stroke Association, National Scientific Inflammation Society
The Conclusion of Interdisciplinary Expert Council on the significance of testing of platelet functional activity in the prevention of cardiovascular complications in patients receiving antiplatelet therapy is presented. Indications for antiplatelet therapy, relation of platelet reactivity with the risk of adverse events, as well as factors that contribute to high residual platelet reactivity in patients receiving antiplatelet therapy are considered. The results of studies on the correction of antiplatelet therapy based on aggregometry data, indications for its implementation in clinical practice, as well as methods for evaluation of residual platelet reactivity are discussed separately.
Key words: functional platelet activity, antiplatelet therapy, high residual platelet reactivity, aggregometry.
Ration Pharmacother Cardiol 2014;10(6):679-687
*Автор, ответственный за переписку (Correspondingauthor): Андреев Денис Анатольевич dennan@mail.ru
Состав Экспертного совета: |
|
1. Алекян Баграт Гегамович – д.м.н, профессор, академик РАН, |
8. Иванова Галина Евгеньевна – д.м.н., профессор, |
главный специалист МЗ РФ по рентгенэндоваскулярной |
главный специалист по медицинской реабилитации МЗ РФ, |
диагностике и лечению, руководитель отделения рентгенохирурги- |
руководитель отдела медицинской и социальной |
ческих методов исследования и лечения сердца и сосудов Научно- |
реабилитации НИИ цереброваскулярной патологии и инсульта |
го центра сердечно-сосудистой хирургии им. А.Н. Бакулева, пред- |
Российского национального исследовательского медицинского |
седатель Российского национального общества специалистов по |
университета им. Н.И. Пирогова |
рентгенэндоваскулярной диагностике и лечению |
9. Ломакин Никита Валерьевич – к.м.н., руководитель |
2. Абугов Сергей Александрович – д.м.н., профессор, |
отделения кардиореанимации Центральной клинической |
руководитель отдела рентгенохирургии и аритмологии |
больницы (ЦКБ) с поликлиникой Управления делами |
Российского научного центра хирургии им. Б.В. Петровского; |
Президента РФ (УДП РФ), руководитель антитромботической |
зав. кафедрой рентгенэндоваскулярных методов диагностики |
клиники поликлиники ЦКБ; доцент кафедры кардиологии |
и лечения Российской медицинской академии последипломного |
и общей терапии Учебно-научного медицинского |
образования |
центра УДП РФ |
3. *Андреев Денис Анатольевич – д.м.н., профессор кафедры |
10. Мешкова Кетевана Сергеевна – к.м.н., с.н.с. НИИ |
неотложной и профилактической кардиологии факультета |
цереброваскулярной патологии и инсульта Российского |
послевузовского профессионального образования врачей |
национального исследовательского медицинского |
Первого Московского государственного медицинского университе- |
университета им. Н.И. Пирогова |
та им. И.М. Сеченова, зав. отделением для больных инфарктом |
11. Покровский Анатолий Владимирович – д.м.н., |
миокарда Университетской клинической больницы №1 |
профессор, академик РАН, президент Российского общества |
4. Бурячковская Людмила Ивановна – д.б.н., руководитель |
ангиологов и сосудистых хирургов, руководитель отделения |
группы механизмов тромбообразования Российского |
хирургии сосудов Института хирургии им. А. В. Вишневского; |
кардиологического научно-производственного комплекса |
зав. кафедрой клинической ангиологии и сосудистой |
5. Вавилова Татьяна Владимировна – д.м.н., профессор, |
хирургии Российской медицинской академии последипломного |
зав. кафедрой клинико-лабораторной диагностики и генетики |
образования |
Института послевузовского образования Федерального |
12. Стаховская Людмила Витальевна – д.м.н., профессор, |
медицинского исследовательского центра им. В. А. Алмазова |
директор НИИ цереброваскулярной патологии и инсульта |
6. Вершинина Марина Германовна – к.м.н., руководитель лабо- |
Российского национального исследовательского медицинского |
раторной службы Центральной клинической больницы с поликли- |
университета им. Н.И. Пирогова, ответственный секретарь |
никой Управления делами Президента РФ |
Президиума Национальной ассоциации по борьбе |
7. Воробьева Надежда Александровна – д.м.н., профессор, |
с инсультами |
зав. кафедрой клинической фармакологии и фармакотерапии |
13. Сычев Дмитрий Алексеевич – д.м.н., профессор, |
Северного Государственного Медицинского Университета; |
зав. кафедрой клинической фармакологии Российской |
директор северного филиала Гематологического научного центра |
медицинской академии последипломного образования |
РАМН, главный гемостазиолог МЗ Архангельской области |
|
Рациональная Фармакотерапия в Кардиологии 2014;10(6) |
679 |

Роль тестирования активности тромбоцитов при антитромбоцитарной терапии
Введение
Вструктуре смертности населения России сер- дечно-сосудистые заболевания (ССЗ) составляют 56,4%, что значительно превышает аналогичный показатель в развитых странах. Смертность от ССЗ среди трудоспособного населения достигает 38% (среди мужчин – 37,7%, среди женщин – 40,1%) [1]. Это
в3-6 раз выше, чем в странах Евросоюза. Экономический ущерб только от ССЗ заболеваний составляет около 1 трлн. рублей в год (около 3% ВВП) [2]. По мнению ведущих российских экспертов, основной причиной такой удручающей статистики является недостаточное развитие мер по профилактике ССЗ, направленных на коррекцию факторов риска, по терапии имеющихся заболеваний, предупреждению осложнений, а также контролю эффективности проводимого лечения [2].
Воснове патогенеза большинства ССЗ лежит атеросклероз. Это заболевание, как правило, обуслав-
ливает ИБС, цереброваскулярную болезнь, перемежающуюся хромоту. Фатальные осложнения ССЗ [инфаркт миокарда (ИМ) и острое нарушение мозгового кровообращения (ОНМК)] связаны с появлением нестабильной атросклеротической бляшки и последующим внутрисосудистым тромбообразованием. Это состояние получило название атеротромбоз. Морфологически атеротромбоз характеризуется наличием эрозии, трещины или разрыва на поверхности бляшки, с прилегающим тромбом различных размеров (от пристеночного до полностью закрывающего просвет артерии). Одним из основополагающих аспектов первичной и вторичной профилактики тромботических осложнений атеросклероза является антитромбоцитарная терапия.
Показания к антитромбоцитарной терапии
Согласно современным российским и зарубежным рекомендациям, антитромбоцитарная терапия показана
при лечении и профилактике многих ССЗ, в том числе она должна проводиться следующим категориям пациентов [3-11]:
1.Больным, перенесшим острый коронарный синдром ОКС (ИМ с подъемом ST, ИМ без подъема ST, нестабильная стенокардия) показана двойная антитромбоцитарная терапия (ДАТ) продолжительностью не менее 1 года.
2.Больным после чрескожного коронарного вмешательства (ЧКВ) рекомендована ДАТ:
при стабильной стенокардии
• 1 мес после имплантации стента без лекарственного покрытия;
• 6-12 мес после имплантации стента с лекарственным покрытием;
больные ОКС (ИМ с подъемом ST, ИМ без подъема ST)
•1 год всем больным независимо от стратегии реваскуляризации;
3.Пациентам, после аортокоронарного шунтирования (АКШ) и других операций по поводу атеросклеротического поражения сосудов показания к ДАТ
иеё длительность определяются клиническими критериями, независимо от метода реваскуляризации.
4.Больным со стабильной ИБС, без перенесенного ИМ в анамнезе показана ацетилсалициловая кислота (АСК), а при непереносимости АСК – клопидогрел. Продолжительность приема – пожизненно.
5.После ишемического некардиоэмболического инсульта – АСК/комбинация АСК с дипиридамолом замедленного высвобождения; при непереносимости АСК и дипиридамола или высоком риске развития ишемического инсульта, при наличии нескольких факторов риска (ИБС и/или атеротромботическое поражение периферических артерий, сахарный диабет) начинать те-
рапию следует с клопидогрела.
6.ДАТ рекомендована пациентам, перенесшим некардиоэмболический инсульт или транзиторную ишемическую атаку (ТИА), у которых развился ОКС (ИМ с подъемом ST, ИМ без подъема ST) или после стентирования коронарных артерий.
7.Антитромбоцитарная терапия рекомендована больным с перемежающейся хромотой.
Реактивность тромбоцитов на фоне приема антитромбоцитарной терапии и риск развития неблагоприятных событий
Адекватность и эффективность ДАТ в значительной степени определяют прогноз. Следствием недостаточного подавления повышенной активности тромбоцитов может стать повторное сердечно-сосудистое событие или тромбоз стента [12-14]. Чрезмерное подавление агрегации тромбоцитов приводит к повышению риска кровотечений. Для более объективной
оценки недостаточного действия антиагрегантов (резистентности) введено понятие «высокая остаточная реактивность тромбоцитов» (ВОРТ), а для избыточного
– «низкая реактивность тромбоцитов» (НРТ). ВОРТ, выявленная на фоне приема антиагреганта, позволяет сделать вывод о неспособности препарата подавить активацию тромбоцита при воздействии специфического агониста [15].
Связь реакции тромбоцитов и риска возникновения неблагоприятных исходов изучалась и про-
должает изучаться во многих клинических исследованиях (GRAVITAS [15], TRIGGER-PCI [13], ARCTIC [16]) и регистрах. В регистре ADAPT-DES [17,18] показано, что у пациентов с ВОРТ отмечается четырехкратное увеличение риска развития тромбоза стен-
680 |
Рациональная Фармакотерапия в Кардиологии 2014;10(6) |

Роль тестирования активности тромбоцитов при антитромбоцитарной терапии
та. Эти данные подтверждаются результатами нескольких мета-анализов, которые свидетельствуют о повышенном риске развития тромбоза стента, смерти, инфаркта миокарда у больных, имеющих ВОРТ (табл. 1).
Тактика интенсификации терапии для преодоления ВОРТ ведет к повышению риска кровотечений, особенно при замене клопидогрела на новые блокаторы P2Y12-рецепторов. Таким образом, чтобы добиться максимальной эффективности антитромбоцитарной терапии, не преступая при этом границ безопасности, предложена концепция «терапевтического окна», основанного на результатах тестирования функции тромбоцитов различными методами (рис.1) [20-22]. Это дает возможность врачу иметь показатель контроля эффективности и безопасности антитромбоцитарной терапии по типу целевого МНО (международное нормализованное отношение) при терапии варфарином, сохраняя равновесие
между риском ишемических и геморрагических осложнений.
Определение высокой остаточной реактивности тромбоцитов на фоне антитромбоцитарной терапии признано одним из важнейших прогностических факторов развития атеротромботических осложнений ИБС
Факторы, обуславливающие ВОРТ на фоне приема антитромбоцтарных препаратов
Ацетилсалициловая кислота
На сегодняшний день накопилось достаточное количество данных, о значительной индивидуальной
Рисунок 1. Визуализация терапевтического окна реак-
тивности тромбоцитов [адаптировано из 19]
AU – arbitrary units – условные единицы; TEG ADP – тромбоэластография со стимуляцией АДФ; VASP PRI – vasodilator-stimulated phosphoprotein-phosphorylation platelet reactivity index – фосфорилирование вазодилатор-стимулированного фосфопротеина индекс реактивности тромбоцитов; VN PRU – VerifyNow P2Y12 Platelet Reactivity Units – единицы реактивности тромбоцитов метод VerifyNow
вариабельности ответа на различные антитромбоцитарные препараты. Так, факт, что у многих больных на фоне АСК развиваются сердечно-сосудистые осложнения, связанные с тромбозом, дал повод выделять больных, резистентных к АСК. Частота резистентности к АСК значительно варьирует по данным разных исследований (от 2 до 28%) [4]. Причины снижения эффективности АСК многообразны, среди них чаще всего отмечают:
•генетические особенности (генетический полиморфизм)
•прием НПВП, конкурирующих с АСК за COX-1-ре- цепторы
•недостаточная абсорбция кишечнорастворимой формы АСК
Таблица 1. Риск развития тромбоза стента, смерти, инфаркта миокарда у больных, имеющих высокую остаточную
реактивность тромбоцитов
Автор, год |
Количество |
Больные, |
Срок |
Частота |
Риск развития конечных точек при |
|
исследований |
(n) |
наблюдения |
выявления |
выявлении ВОРТ ОШ, (95% ДИ) |
|
(n) |
|
|
ВОРТ (%) |
|
Aradi et al , 2010 |
20 |
9187 |
1 мес-3 г |
32 (6-79) |
Смерть 3,35 (2,39-4,70) |
|
|
|
|
|
Нефатальный ИМ 3,0 (2,26-3,99) |
|
|
|
|
|
Тромбоз стента 4,14 (2,74-6,25) |
Snoep et al., 2007 |
25 |
3688 |
14 дней-6 мес |
21 (17-25) |
Комбинированая точка (смерть, |
|
|
|
|
|
тромбоз стента, ИМ, ОНМК, ОКС, |
|
|
|
|
|
реваскуляризация) – 12,02 (5,91-724,42) |
Brar et al., 2011 |
6 |
3059 |
1 мес-12 мес |
- |
Смерть – 1,66 (1,03-2,68) |
|
|
|
|
|
ИМ – 2,04 (1,51-2,76) |
|
|
|
|
|
Тромбоз стента – 3,11 (1,50-6,46) |
Sofi et al., 2010 |
14 |
4564 |
14 дней-12 мес |
- |
Комбинированная точка (смерть, |
тромботические осложнения) – 5,67 (2,97-10,84)
Включены исследования с использованием VerifyNow
ВОРТ – высокая остаточная реактивность тромбоцитов; ОШ – отношение шансов; ДИ – доверительный интервал; ИМ – инфаркт миокарда; ОНМК – острое нарушение мозгового кровообращения; ОКС – острый коронарный синдром
Рациональная Фармакотерапия в Кардиологии 2014;10(6) |
681 |
Роль тестирования активности тромбоцитов при антитромбоцитарной терапии
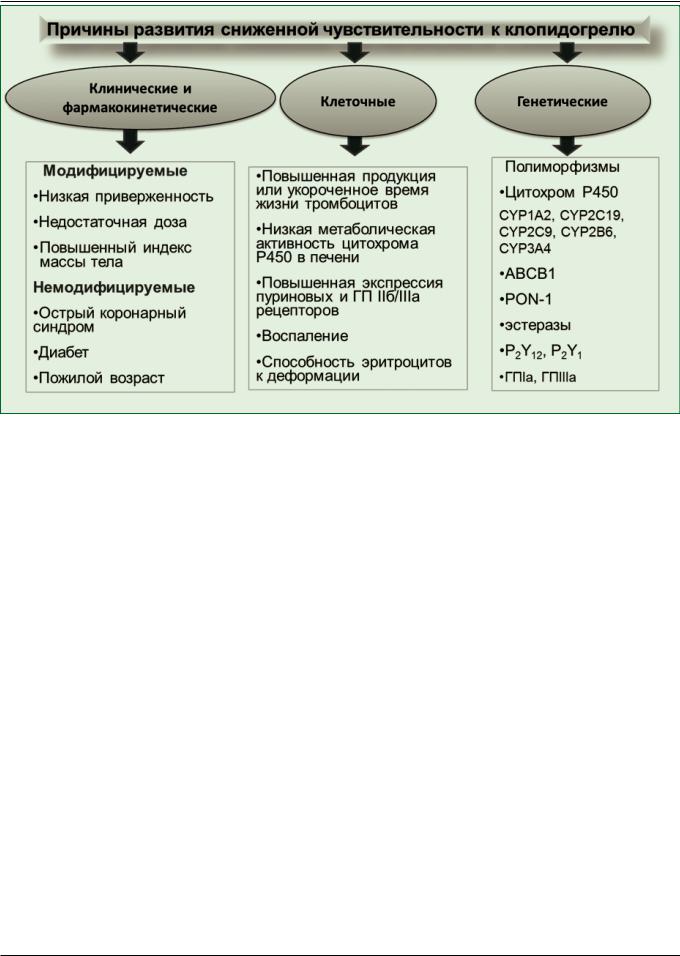
Рисунок 2. Факторы, определяющие недостаточную эффективность клопидогрела
•возрастные особенности
•сокращение времени жизни тромбоцитов (например, при ОКС, воспалении, атеросклерозе, ХСН) [23-26].
P2Y12 ингибиторы (клопидогрел, прасугрел, тикагрелор)
Высокая остаточная реактивность к клопидогрелу по данным мета-анализа Snoep J.D. и соавт. (2007) составляет 21% [27]. По данным мета-анализа Combescure C. и соавт. было показано, что до 25% пациентов резистентны к клопидогрелу [12]. Доказано, что ВОРТ зависит от генетических полиморфизмов, клеточных осо-
бенностей и клинических факторов, которые могут быть как немодифицируемые (генетические, клеточные), так и модифицируемые [28-31] (рис. 2).
Сегодня также показано существование ВОРТ на фоне терапии прасугрелом и тикагрелором [20,32].
Результаты исследований по коррекции антитромбоцитарной терапии на основании результатов агрегатометрии
В настоящее время опубликованы результаты не-
скольких крупных клинических исследований с измерением активности тромбоцитов с помощью Verify Now: GRAVITAS [15], TRIGGER-PCI [13] и ARCTIC [16].
Исследование GRAVITAS было проведено для выяснения вопроса об эффективности стратегии на-
значения двойной дозы клопидогрела больным ИБС с ВОРТ после ЧКВ в сравнении со стандартной дозой [15]. В исследование было включено 5429 пациентов со стабильной ИБС (60,2%) или ОКС без подъема сегмента ST (39,8%) получавших ДАТ (клопидогрел и аспирин). Агрегатометрия проводилась через 12-24 час после ЧКВ. ВОРТ, определяемая как PRU ≥230 (Platelet Reactivity Units – единицы реактивности тромбоцитов), была выявлена у 2214 пациентов (40,8%), которые в дальнейшем были рандомизированы в группы стандартной дозы клопидогрела (75 мг) или удвоенной (150 мг) в течении 6 мес (нагрузочная доза составляла 600 мг). Увеличение дозы
клопидогрела не снижало частоту развития сердечнососудистой смерти, ИМ или тромбоза стента [отношение шансов (ОШ) 1,01; 95% доверительный интервал (ДИ) 0,58-1,76; р=0,97] и не влияло на частоту кровотечений (ОШ 0,59; 95% ДИ 0,31-1,11; р=0,10) через 6 мес. Очевидными недостаткам исследования GRAVITAS являются: 1) включение в основном стабильных пациентов с низким риском развития неблагоприятных исходов 2) большое число больных с ВОРТ (до 40%) в группе удвоенной дозы клопидогрела;
3) установленный в исследовании порог PRU >230 не являлся оптимальным, т.к. снижение точки разделения до значения PRU >208 позволило выявить выраженную корреляцию с низким риском ишемических событий через 6 месяцев.
682 |
Рациональная Фармакотерапия в Кардиологии 2014;10(6) |

Роль тестирования активности тромбоцитов при антитромбоцитарной терапии
Таблица 2. Замена терапии на основании результатов тестирования и частота сердечно-сосудистых событий по
результатам исследования MADONNA
Событие |
Замена терапии (n=403) |
Без замены терапии (n=395) |
Р |
Тромбоз стента, n (%) |
1 (0,2) |
7 (1,9) |
0,027 |
ОКС, n (%) |
0 (0) |
10 (2,5) |
0,001 |
Сердечно-сосудистая смертность, n (%) |
8 (2) |
5 (1,3) |
0,422 |
Большие кровотечения, n (%) |
4 (1) |
1 (0,3) |
0,186 |
ОКС – острый коронарный синдром
Основной клинический вопрос исследования TRIG- |
В исследовании ARCTIC участвовало 2440 пациен- |
GER PCI – имеет ли преимущество стратегия назначе- |
тов со стабильной ИБС (73%) и ОКС (27%) [16]. |
ния прасугрела в сравнении с назначением стандарт- |
Сравнивалась стратегия контроля агрегации тромбо- |
ной дозы клопидогрела у пациентов, имеющих ВОРТ че- |
цитов (тестирование агрегации на аспирине и клопи- |
рез 24 час после ЧКВ [13]. Исследование проводилось |
догреле до ЧКВ и через 7-14 дней) со стандартной стра- |
у 423 пациентов со стабильной ИБС, получающих |
тегией ведения пациента (без тестирования). Порог ВОРТ |
ДАТ. Агрегатометрия проводилась через 24 час после |
для клопидогрела составлял PRU >235. Пациентом с |
ЧКВ и 2-7 час после назначения поддерживающей дозы |
ВОТР, доля которых до ЧКВ составила 34,5%, на- |
клопидогреля 75 мг. Пациенты с ВОРТ (PRU >208) были |
значали удвоенную нагрузочную дозу клопидорела |
рандомизированы в группы прасугрела 10 мг/сут или |
(600 мг), либо 60 мг прасугрела до процедуры. После |
клопидогрела 75 мг/сут. Исследование было прекра- |
ЧКВ пациенты в группе мониторинга получали 150 мг |
щено досрочно (после рандомизации 423 пациентов) |
клопидогрела (80,2%) или 10 прасугрела (3,3%). В |
из-за крайне низкой частоты ишемических событий, так |
течение 14-30 дней после имплантации стента, паци- |
частота развития комбинированной точки (сердечно- |
енты с ВОРТ на клопидогреле были переведены на пра- |
сосудистая смерть, ИМ или тромбоз стента) через 6 мес |
сугрел 10 мг или получили дополнительно 75 мг кло- |
составила 0,5% в контрольной группе. Исследование |
пидогрела, а пациенты с НОРТ (ингибирование более |
также имеет существенные ограничения: 1) досрочное |
90%) были переведены на клопидогрел 75 мг. В кон- |
прекращение; 2) включение больных с низким риском |
це исследования среди пациентов с ВОРТ лишь 17% по- |
неблагоприятных исходов; 3) высокая частота выбы- |
лучали прасугрел. Через 12 мес стратегия выбора те- |
вания пациентов с ВОРТ после открытой рандомизации |
рапии на основании мониторинга функции тромбоцитов |
(32%). |
не продемонстрировала преимущества по сравнению |
|
|
|
|
Рисунок 3. Влияние замены терапии на основании результатов тестирования на риск сердечно-сосудистых событий (адаптировано из [33])
Рациональная Фармакотерапия в Кардиологии 2014;10(6) |
683 |