Материал: РФ Теоретическое обоснование технологии радикального процесса хлорирования олефиновых углеводородов
СОДЕРЖАНИЕ
СОДЕРЖАНИЕ |
2 |
ВВЕДЕНИЕ |
3 |
1 Химизм и механизм реакции |
4 |
2 Термодинамика и кинетика процесса |
7 |
3 Инициирование реакции |
9 |
4 Условия проведения и основные показатели процесса |
11 |
5 Принципы технологического оформления |
13 |
ЗАКЛЮЧЕНИЕ |
16 |
СПИСОК ИСПОЛЬЗОВАННЫХ ИСТОЧНИКОВ |
17 |
ВВЕДЕНИЕ
Одним из наиболее важных процессов органического синтеза является галогенирование углеводородов и их производных. Этот, без сомнения, широчайший класс процессов позволяет производить и использовать большое разнообразие самых различных веществ. В их число входят, например, промежуточные продукты органического синтеза (такие как 1,2-дихлорэтан или хлоргидрины), из которых в дальнейшем получают винилхлорид, окись этилена, этиленгликоль и многие другие вещества; растворители, пестициды, хладагенты и т.д.
С точки зрения катализа процессы хлорирования можно разделить на три основные категории: радикально-цепные, ионно-каталитические и гетерогенно-каталитические. Они имеют принципиально разные механизм, условия проведения и закономерности протекания.
В данном реферате рассмотрим процессы радикально-цепного хлорирования олефинов, а именно химизм и механизм основных реакций, перечислим возможные побочные реакции, условия проведения и основные показатели, оценим кинетику и термодинамику, а также рассмотрим типичную принципиальную технологическую схему производства хлористого аллила.
1 Химизм и механизм реакции
Реакции радикально-цепного хлорирования олефинов можно разделить на два основных класса – заместительные и аддитивные. В первом случае происходит замещение атома водорода на хлор, во втором присоединение молекулы хлора по кратной связи. Примеры реакций:
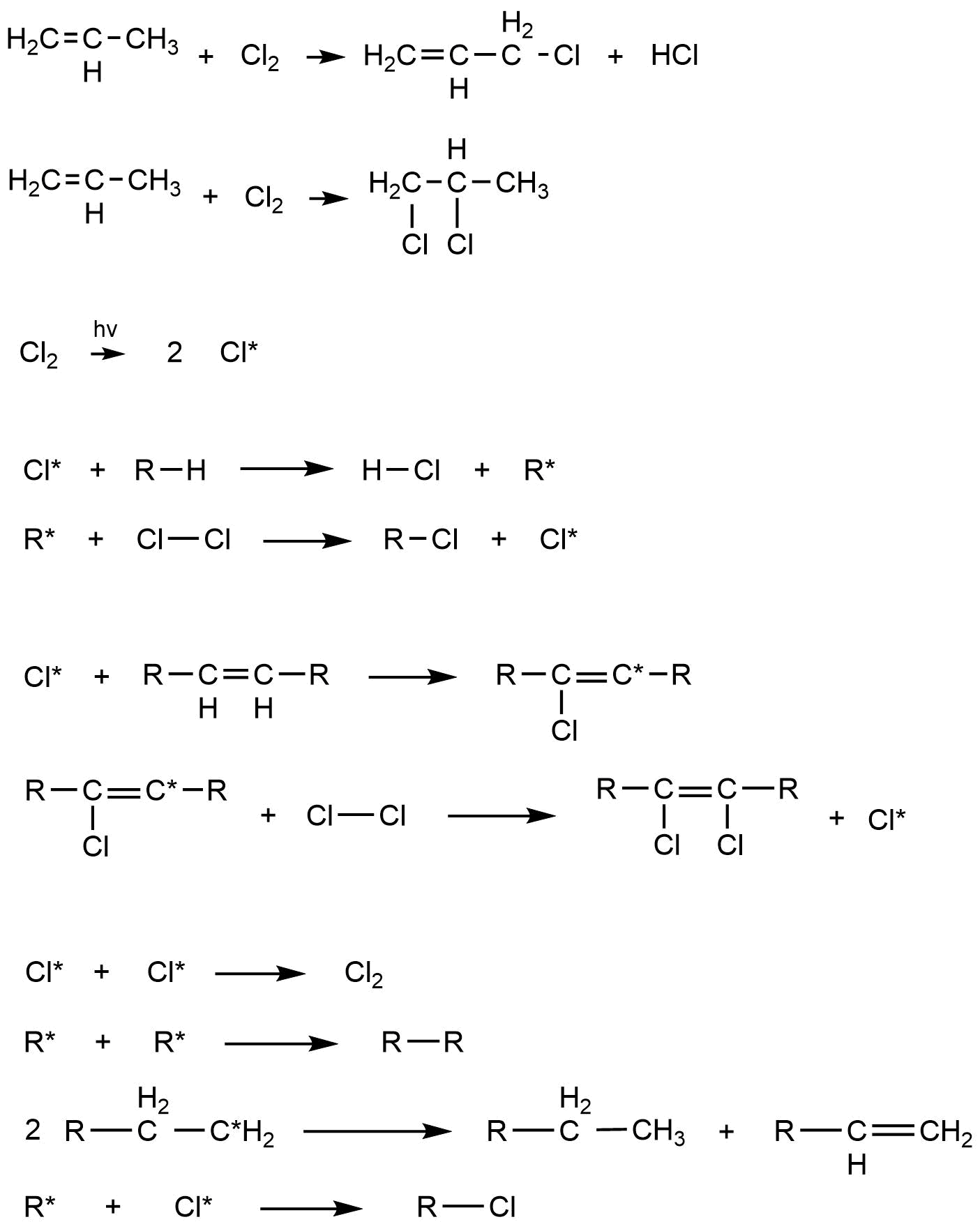
При замещении из пропилена получили аллилхлорид, при присоединении 1,2-дихлорпропан. Впрочем, механизмы обеих реакций схожи. Рассмотрим три стадии радикально-цепного механизма хлорирования олефинов: зарождение цепи, ее рост и обрыв.
1) Зарождение цепи
Реакция начинается с образования радикалов – крайне реакционноспособных частиц с неспаренным электроном. Это может быть достигнуто при помощи высокой температуры, УФ-облучения или другими способами, которые будут более подробно рассмотрены в разделе 3 [1].
2) Рост цепи
Образовавшиеся в процессе зарождения цепи радикалы хлора начинают атаковать молекулы олефина, при этом возможны два варианта развития событий.
В первом случае радикал отнимает у молекулы олефина атом водорода. При этом образуется хлороводород, а молекула олефина становится радикалом. В свою очередь, новообразованный радикал атакует молекулу хлора, отнимая у него атом хлора. Таким образом возникает новый радикал хлора, который также атакует молекулы олефина – так происходит заместительное хлорирование [1].
Во втором случае атом хлора присоединяется по кратной связи олефина, при этом образуется радикал, который в свою очередь атакует молекулу Cl2, отбирая у нее атом хлора. Так происходит аддитивное хлорирование [1].
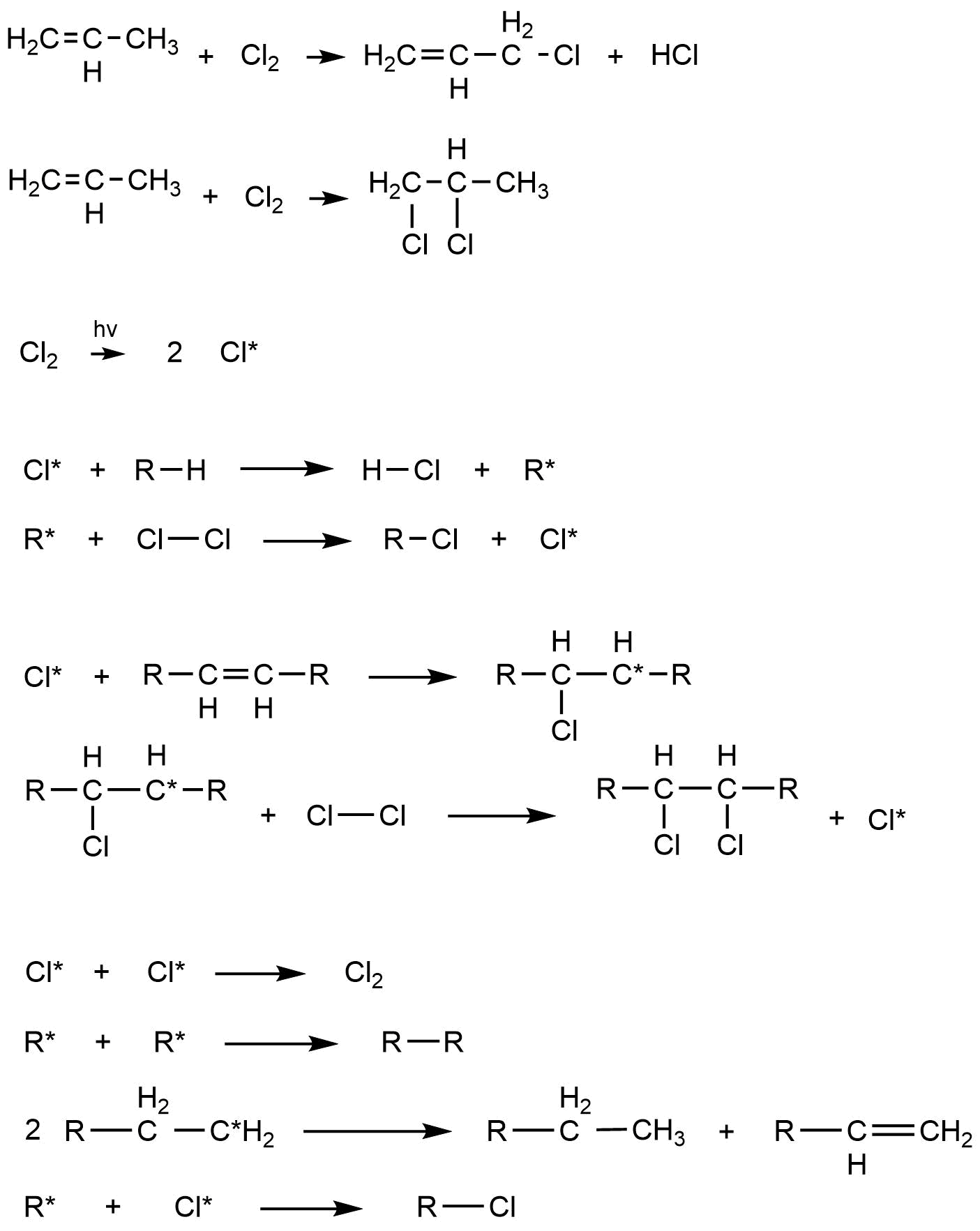
Следует отметить, что олефины, имеющие разветвление при ненасыщенном атоме углерода (изобутен) неподвержены аддитивному хлорированию [1].
3) Обрыв цепи
Рано или поздно происходит гибель радикалов. В газофазных процессах, например, возможна гибель радикалов при попадании на стенку реактора. Также гибель радикалов происходит при их рекомбинации и диспропорционировании:
Помимо этого, возможен обрыв цепи на молекулах ингибиторов, таких как фенолы и соединения серы [1].
Следует отметить, что реакции замещения и присоединения конкурируют между собой. Таким образом, при проведении процесса заместительного хлорирования пропилена побочной будет считаться реакция присоединения и наоборот. Также побочным процессом может считаться получение ди-, три- и перхлорпроизводных углеводородов, если требуется максимальный выход монохлорпроизводного [1].
2 Термодинамика и кинетика процесса
Реакции хлорирования олефинов необратимы, а также весьма экзотермичны. Так, при хлорировании метана выделяется 105 кДж/моль тепла, при аддитивном хлорировании этилена еще больше – 184 кДж/моль. Это диктует определенные условия при проектировании установки [1].
Как было отмечено выше, в процессе хлорирования олефинов имеют место параллельные реакции замещения и присоединения, при этом энергия активации реакций присоединения значительно ниже. Отсюда следует вывод, что скорость реакций замещения намного сильнее зависит от температуры проведения процесса. Действительно, при высоких температурах преобладают реакции замещения, а при низких – присоединения. На рисунке 2.1 представлен график зависимости расхода хлора на реакции присоединения и замещения от температуры при хлорировании пропилена. Как видно, при низких температурах (50–100 °С) протекают практически только реакции присоединения, а при высоких – замещения [1].
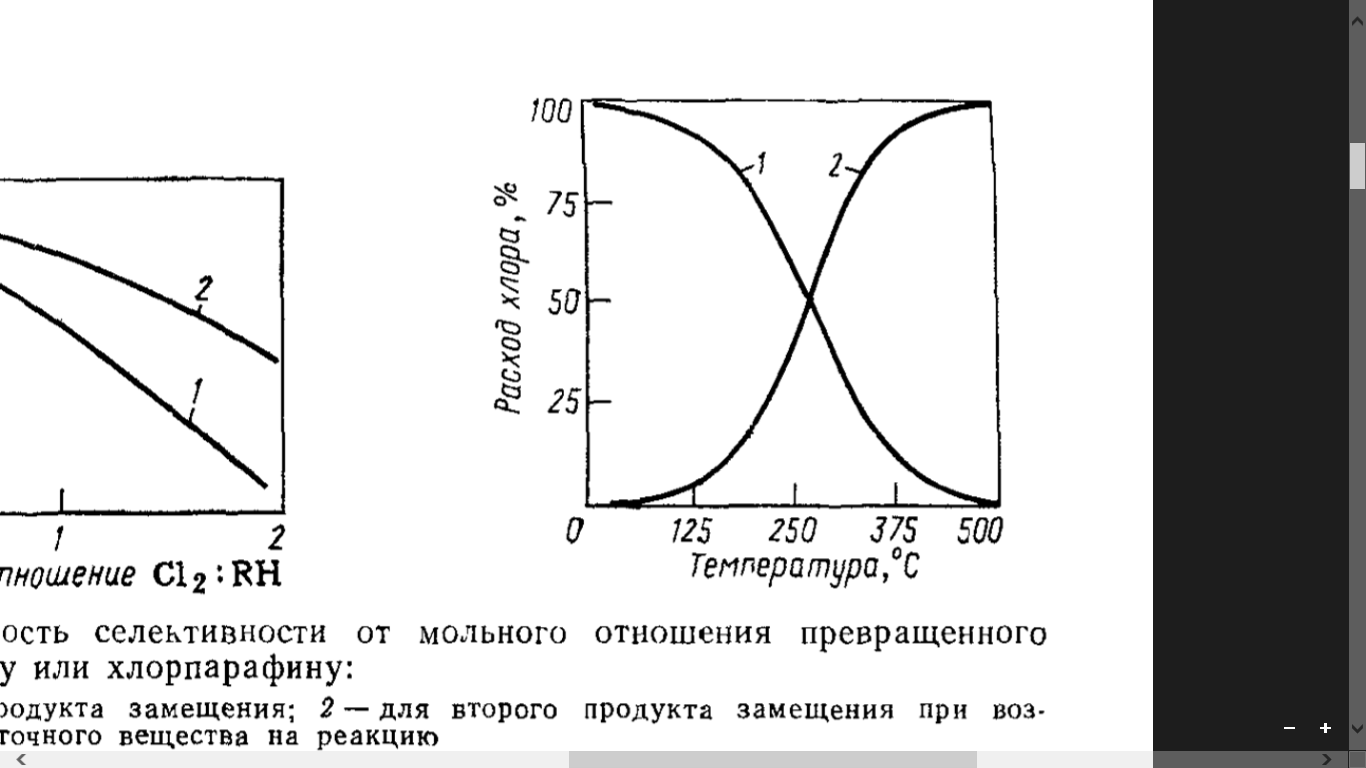
Рисунок 2.1 – График зависимости расхода хлора на реакции присоединения (1) и замещения (2) при хлорировании пропилена
В свою очередь при заместительном хлорировании алкенов С3+ реакция также может пойти в разных направлениях. Речь идет о возможности замещения атома водорода как при насыщенном, так и при ненасыщенном атоме углерода. При этом реакционная способность и константа скорости реакции растут в ряду
СН2=СН–Н << СН2=СН–СН2–СН2–Н << СН2=СН–СН2–Н
Как следует, при заместительном хлорировании алкенов С3+ преимущественно образуются продукты с атомом хлора в аллильном положении.
Лимитирующей стадией процесса радикального хлорирования олефинов является стадия зарождения цепи, причем энергия активации существенно изменяется при использовании разных методов инициирования. При термическом инициировании она лежит в пределах 125-170 кДж/моль, при химическом - порядка 85 кДж/моль, при фотохимическом – 20-40 кДж/моль.
3 Инициирование реакции
В разделе 1 отмечалось, что существует несколько методов инициирования радикально-цепной реакции хлорирования олефинов. Рассмотрим их:
1) Термическое инициирование
Термическое инициирование реакции применяется в газофазных процессах. При попадании молекулы хлора на стенку реактора или поверхность насадки она хемосорбируется, за счет чего связь Cl–Cl ослабевает, а под действием высокой температуры разрывается. При этом образуется радикал хлора [1].
Этот способ наиболее прост, но применим только в газофазных процессах.
2) Химическое инициирование
Химическое инициирование применяется в жидкофазных процессах и основывается на введении в сырье т.н. инициаторов – веществ, которые при относительно небольших температурах разлагаются, образуя радикалы. В качестве инициаторов, как правило, выступают перекисные соединения (например пероксид бензоила (С6Н5СОО)2, разлагающийся с образованием фенил-радикалов и СО2).
Такой способ инициирования не требует значительных капиталовложений, но приводит к увеличению эксплуатационных затрат, связанных с необходимостью покупки инициаторов, а также к загрязнению конечного продукта примесями [1].
3) Фотоинициирование
Фотоинициирование также применяется в жидкофазных процессах. Энергия сообщается молекуле хлора в виде квантов света, излучаемых при помощи мощных УФ-ламп. В отличие от химического инициирования, данный способ значительно усложняет конструкцию реактора и увеличивает капиталовложения за счет необходимости установки дорогостоящих ламп, однако имеет меньшие эксплуатационные затраты и более чистые продукты [1].
4) Индуцированное хлорирование
Иногда имеет место термическое инициирование реакции при температурах, недостаточных для разрыва связи Cl–Cl (100-200 °С). В таком случае говорится об индуцированном хлорировании – образовании радикалов при взаимодействии молекул хлора и олефина [1].
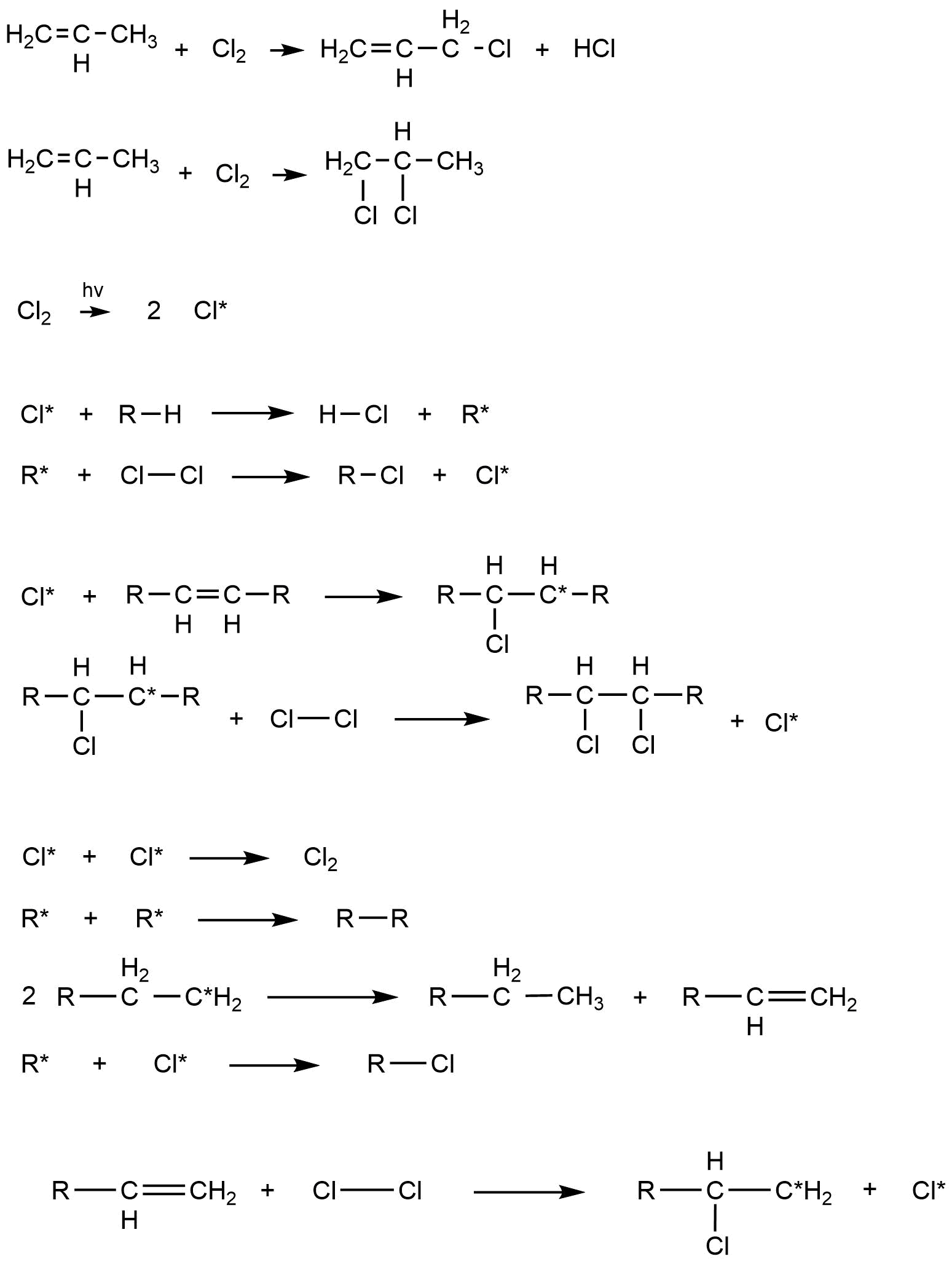
5) Термокаталитическое хлорирование
Как частный случай термического инициирования существует так называемое термокаталитическое хлорирование, протекающее при более низких температурах (на 150-200 °С ниже, чем при термическом инициировании) в присутствии активированного угля. Механизм стадии зарождения цепи слабо изучен; предполагается, что уменьшение энергии активации вызвано адсорбцией молекул хлора на поверхности активированного угля и следующем из этого ослаблении связи Cl–Cl. Данный способ инициирования во многом схож с термическим и может быть применен только в газофазных процессах [1].
4 Условия проведения и основные показатели процесса
Существуют два основных способа проведения радикально-цепного хлорирования углеводородов – газофазный и жидкофазный. Впрочем, поскольку радикально-цепное хлорирование олефинов в жидкой фазе в промышленности не проводится, рассмотрим только газофазный процесс. Итак, основные технологические параметры процесса:
Выбор температуры определяется целевым продуктом реакции. Так, при хлорировании пропилена в аллилхлорид температура выдерживается в районе 500-520 °С для большего выхода целевого продукта. В то же время синтез дихлорбутенов аддитивным хлорированием бутадиена проводится при более низких температурах (порядка 300 °С) в целях замедления протекания реакций замещения. Процесс проводится при атмосферном давлении, время контакта изменяется в пределах 0,1-2 с [1]. При этом, если температура процесса приближается к температуре крекинга сырья или продукта, увеличение времени контакта приводит к ухудшению селективности [3].
Большое значение имеет соотношение концентраций углеводорода и хлора. При хлорировании олефинов в подавляющем большинстве случаев протекание реакций перхлорирования (последовательное введение в молекулу нескольких атомов хлора) крайне нежелательно, поэтому олефин подается в реактор в большом избытке (5 моль пропилена на 1 моль хлора при синтезе аллилхлорида). Это позволяет добиться выхода аллилхлорида порядка 80% и стопроцентной конверсии хлора [2]. Еще одной причиной большого избытка олефина является высокая экзотермичность процесса: тепло реакции снимается избыточным олефином [2].
Большое значение имеет удаление из сырьевого олефина и хлора воды, поскольку даже небольшое ее присутствие приводит к резкому усилению коррозии оборудования. В связи с этим газообразный хлор предпочитают получать испарением сжиженного, а олефин осушают серной кислотой или при помощи адсорбентов [2].
5 Принципы технологического оформления
Рассмотрим технологию получения аллилхлорида хлорированием пропилена в газовой фазе.
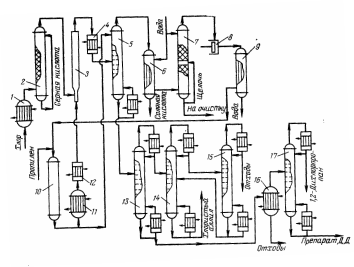
Рисунок 5.1 – Принципиальная технологическая схема получения аллилхлорида 1, 11, 16 – испарители; 2 – колонна; 3 – реактор; 4 – холодильник; 5 – конденсационно-отпарная колонна; 6 – абсорбер; 7 – колонна очистки пропилена; 8 – компрессор; 9 – конденсатор; 10 – осушитель; 12 – теплообменник; 13, 14, 15, 17 – ректификационные колонны.
На рисунке 5.1 представлена принципиальная технологическая схема процесса получения аллилхлорида. В испарителе 1 происходит испарение жидкого хлора, а в колонне 2 осушение его серной кислотой. Свежий пропилен в смеси с возвратным осушается в осушителе 10 и после подогрева в теплообменнике 12 до 350-370 °С поступает в реактор 3, где смешивается с хлором.
На выходе из реактора реакционная масса поступает в холодильник 4 и затем в колонну 5, орошаемую жидким пропиленом, где происходит отделение смеси пропилена и хлороводорода от хлорпроизводных. Смесь хлороводорода и пропилена подается в абсорбер 6, куда также прямотоком подается вода, за счет чего большая часть хлороводорода переходит в воду, образуя соляную кислоту. Пропилен, загрязненный хлором, далее попадает в колонну очистки пропилена 7, в которую подается вода и раствор щелочи, для окончательной очистки от хлороводорода. После этого пропилен, теперь содержащий уносимые пары воды сжимается в компрессоре 8 и охлаждается в конденсаторе 9, в результате чего отделяется большая часть воды. Очищенный таким образом рециркулирующий пропилен далее поступает на смешение со свежим.
Остаток колонны 5, представляющий собой смесь хлорпроизводных, поступает в систему ректификационных колонн. В колонне 13 отделяются тяжелые побочные продукты. Дистиллят колонны 13, содержащий аллилхлорид и легкие примеси подается в колонну 14, где в качестве остатка отводится аллилхлорид. Дистиллят колонны 14 также содержит аллилхлорид и потому направляется в колонну 15, дистиллят которой отводится в виде отходов, а остаток поступает на смешение с питанием колонны 14.
Остаток колонны 13, представляющий собой тяжелые побочные продукты поступает в испаритель 16, где от него отделяются сажа и продукты осмоления, после чего подается в колонну 17. Дистиллат колонны 17 представляет собой 1,2-дихлорпропан, остаток – смесь дихлорпропана и дихлопропенов [2].
Следует отметить, что технологии разных фирм имеют отличия. Так, например, технология фирмы Dow Chemical Co предполагает подачу побочного продукта дихлорэтана в печь крекинга; образующиеся при этом продукты смешиваются с реакционным газом из реактора и подаются на разделение. Таким образом повышается селективность процесса, так как основным продуктом термического разложения 1,2-дихлопропана является аллилхлорид [4].
ЗАКЛЮЧЕНИЕ
Итак, нами были рассмотрены химизм и механизм основных реакций процесса радикально-цепного хлорирования олефинов, а также их основные термодинамические, кинетические и технологические параметры и принципиальная технологическая схема производства аллилхлорида.
Подводя итоги, можно сказать, что технологическое оформление процессов радикально-цепного хлорирования олефинов обосновано особенностями реакции. Так, несмотря на необратимость реакции, в технологии используется рециркуляция олефина – это вызвано необходимостью съема большого количества тепла и минимизации протекания реакций перхлорирования.
СПИСОК ИСПОЛЬЗОВАННЫХ ИСТОЧНИКОВ
1) Лебедев, Н. Н. Химия и технология основного органического и нефтехимического синтеза: учебник для вузов / Н. Н. Лебедев. – 4-е изд., перераб. и доп. – М.: Химия, 1988. – 592 с.
2) Промышленные хлорорганические продукты: справочник / под ред. Л. А. Ошина. – М.: Химия, 1978. – 656 с.