Материал: Региональные особенности содержания и распределения ртути в водных экосистемах Оби
Региональные особенности содержания и распределения ртути в водных экосистемах Оби
Курсовая работа
Региональные особенности содержания и распределения ртути в водных
экосистемах Оби
Введение
водный ртуть экосистема
Уникальные биогеохимические и экотоксикологические свойства ртути известны достаточно давно. Суть проблемы ртутного загрязнения заключается не только в продолжающемся нарастании масштабов ее поступления в биосферу. Увеличивающаяся общая антропогенная нагрузка на природные комплексы, даже отдаленно не связана с ртутной, очень часто приводит к тому, что уже имеющаяся в окружающей среде ртуть переходит в более подвижные и токсичные формы [1].
Ртуть и её соединения относятся к наиболее опасным токсичным веществам, являясь веществами 1-го класса опасности (чрезвычайно опасные), и их содержание строго лимитируется во всех компонентах окружающей среды, питьевой воде, воздухе и продуктах питания. Несмотря на то, что ртуть издавна используется в различных отраслях деятельности человека и её токсичность известна с древних веков, только в последние десятилетия появились новые сведения о поистине глобальном ртутном загрязнении окружающей среды.
В 2003 г. Совет управляющих ЮНЕП на основе Отчета о глобальной оценке выбросов ртути [2] пришел к выводу, что масштабы глобального неблагоприятного воздействия ртути приводят к необходимости организации международной кампании по снижению опасности для человека и живой природы от выбросов ртути в окружающую среду.
Основной причиной для принятия
решения о необходимости мер, направленных на проблему ртутного загрязнения,
стал глобальный перенос ртути в окружающей среде. Для решения этих проблем была
создана программа ЮНЕП по ртути, а в октябре 2013 г. открыта для подписи
Минаматская конвенция по ртути (The Minamata Convention on Mercury), цель
которой заключается в охране здоровья человека и окружающей среды от
антропогенных выбросов и высвобождений ртути и ее соединений [20]. Этот
документ предусматривает взаимный обмен знаниями и данными о наличии и
перемещении ртути и ртутных соединений в окружающей среде, а также
географически репрезентативного мониторинга уровней ртути и ртутных соединений
в уязвимых группах населения и компонентах окружающей среды (Статья 19, пункт 1b) [21]. В новом отчете ЮНЕР
«Глобальная оценка ртути» [22] представлены оценки природных и техногенных
выбросов ртути в воздух и в водную среду от различных источников. В отчете
подчеркивается необходимость мониторинга и систематизации данных о ртути в
окружающей среде по всему миру для дальнейшего понимания транспорта и
глобального цикла ртути. Изучение ртути, поступающей в водную среду чрезвычайно
важно, так как именно в водных экосистемах вследствие метилирования
неорганические формы ртути превращаются в более токсичные и биодоступные
органические формы, делая возможным накопление и биомагнификацию ртути по
водным пищевым цепям [15]. Наиболее опасное концентрирование происходит в цепи:
вода - донные отложения - биота - рыбы - питающиеся рыбой птицы / животные /
человек.
1. Ртуть в водных экосистемах
В окружающую среду ртуть попадает в
результате комплексного действия физико-химических и биохимических процессов.
Ее пространственное перемещение происходит, по двум каналам - водному и
атмосферному. В глобальном масштабе более важным является второй. В пресные
вода суши она поступает при разрушении коренных пород, выщелачивании из рыхлых
отложений и почв, разложении растительности и водных организмов, а также при
выпадении атмосферных осадков. Среди природных источников поступления ртути в
атмосферу главная роль принадлежит дегазации земной коры (включая зоны ртутной
минерализации), вулканам и испарению из океанов (при фотовосстановлении Hg(II)
в водной толще до Hg(O)).
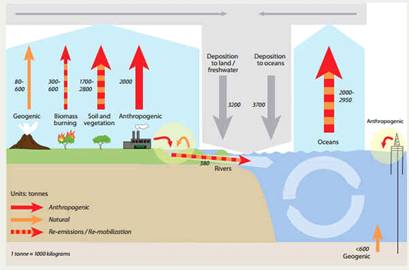
Рисунок 1. Глобальный цикл ртути [15]
Находясь в атмосфере, ртуть легко
может транспортироваться на значительные расстояния, выпадая затем на
поверхность земли вместе с осадками или благодаря сухому осаждению. Ее поток в
непосредственное окружение человека увеличился в индустриальную эпоху.
Некоторые виды хозяйственной деятельности возмущают естественные
биогеохимические циклы элемента, приводя к значительным отклонениям его
содержания от фоновых значений в различных природных объектах.
1.1 Важнейшие свойства ртути
Ртуть является элементом IIб Периодической системы Д.И. Менделеева. Её атомный номер 80, атомная масса 200,59. В природе существует семь изотопов с атомными массами 196 (0,15%), 198 (10,12%), 199 (17,04%), 200 (23,13%), 201 (13,18%), 203 (29,8%), 204 (6,72%). Атомный радиус ртути 1,60 Ангстрем (для К=6), межъядерное расстояние 3,005 Ангстрем. Потенциалы ионизации ртути 10,43 и 18,65 эВ, работа выхода электрона из металла 4,52 эВ.
Ртуть - серебристо - белый металл, обладающий низкой температурой плавления (-38,36°C). В твердом виде - приобретает белый цвет и становится ковкой. Плотность металла зависит от температуры и изменяется от 14,193 (- 38,36°C) до 13,546 (20°C) г/см3. Удельная теплота плавления ртути 2,79 кал/г. Температура кипения ртути относительно низка и составляет 356,66°C при 760 мм рт. ст.
В соединениях ртуть проявляет степень окисления +2 и +1. Обладая высоким потенциалом ионизации, высоким положительным окислительным потенциалом, ртуть является относительно стойким в химическом отношении элементом. В соляной и разбавленной серной кислотах и в щелочах ртуть не растворяется. Но она легко растворяется в азотной кислоте и в царской водке, а при нагревании - в концентрированной серной кислоте. Металлическая ртуть способна растворяться в органических растворителях, а также в воде. Растворимость ее в воде зависит от рН раствора.
Еще одно свойство ртути связано с тем, что при растворении в ней металлов образуются амальгамы - металлические системы, одним из компонентов которых является ртуть. Это используется в некоторых технологических процессах (амальгамной металлургии).
Ионы Hg (II) образуют большое количество комплексных соединений с координационными числами 2 и 4. Имея конфигурацию электронной оболочки d10, ртуть также может образовывать комплексы с координационными числами 3, 5, 6 и 8. Во всех комплексных соединениях связь ртуть-лиганд является ковалентной и весьма прочной. Наиболее устойчивы комплексы с лигандами, содержащими атомы галогенов, углерода, азота, фосфора и серы [2].
Она реагирует с галогенами (хлор, йод, фтор, бром), серой, селеном, фосфором и другими неметаллами. Практическое значение имеют йодная ртуть HgJ, хлористая ртуть (каломель) Hg2Cl2 и хлорная ртуть (сулема) HgCl2. При взаимодействии ртути с серой образуется сульфид ртути HgS - самое распространенное в природе ее соединение, в форме которого добывается почти вся ртуть. Оно известно в трех модификациях: красная (идентичная минералу киноварь), черная (черный сульфид ртути, или метациннабарит) и β-киноварь (в природных условиях не обнаружена). Из других соединений ртути известны такие, как гремучая ртуть Hg(ONC)2, нитрат Hg(NO3)2, сульфат (HgSO4) и сульфит (HgSO3) ртути, красный и желтый йодид ртути и др. При воздействии на соли ртути аммиака образуются комплексные соединения (белый плавкий преципитат HgCl.2NH3, белый неплавкий преципитат HgNH2Cl и др.).
Существует большое количество ртутьсодержащих органических соединений, в которых атомы металла связаны с атомами углерода. Среди них выделяют две основных группы: 1) арилртутные соединения, как правило синтетические, характеризующиеся присутствием в их молекуле радикала ароматических углеводородов; 2) алкилртутные (метил- и диметилртутные) соединения, имеющие в своем составе однозамещенный углеводородный радикал и образующиеся в природных условиях (например, ион метилртути СH3-Hg+). Химическая связь углерода и ртути очень устойчива. Она не разрушается ни водой, ни слабыми кислотами, ни основаниями. С позиций опасности для живых организмов (т.е. с позиций токсикологии - науки о ядах) наиболее токсичными из металлоорганических соединений ртути являются алкилртутные соединения с короткой цепью, прежде всего, метилртуть [14].
Уникальный комплекс таких физико-химических свойств ртути, как текучесть, однородное объемное расширение в широком интервале температур, высокое поверхностное натяжение и несмачиваемость стеклянных поверхностей, обусловливает ее широкое использование в измерительных приборах (термометрах, барометрах, манометрах) [2].
Уникальные свойства сделали ртуть в современных отраслях промышленности важным элементом. Нет такой отрасли, где бы ни использовался этот необычный металл:
Металлургия:
Ø использует свойство ртути растворять в себе большинство металлов, в результате чего получаются амальгамы;
Ø целый ряд важнейших сплавов получается с помощью ртути, находящих применение в гальванопластике, гравировке и литографии;
Ø ртутные соединения применяют в производстве драгоценных металлов.
Тяжёлое машиностроение:
Ø вакуумные установки;
Ø современны ртутные диффузионные насосы;
Ø тяжело нагруженные гидродинамические подшипники; ртутнопаровые турбины содержат большое количество ртути в жидком состоянии и его необходимо постоянно пополнять.
Электротехническая промышленность:
Ø лампы дневного света, кварцевые, люминесцентные;
Ø выпрямители электрического тока, преобразующие трёхфазный ток в постоянный посредством жидкого ртутного катода;
Ø сухие батареи, технология изготовления которых включает применение ртути, сегодня на них работают слуховые аппараты;
Ø аккумуляторы.
Приборостроение и радиотехническая промышленность:
Ø контрольно-измерительные приборы (манометры, ареометры, барометры, термометры), полярографы;
Ø ртутные муфты входят в сборку миниатюрных двигателей для стиральных машин, холодильников, кондиционеров;
Ø в астрономии есть ртутный прибор - горизонт, где металл выступает в роли идеальной зеркальной поверхности для наблюдения за небесными телами.
Ø В горном деле ртуть помогает отделить от золота неметаллические примеси.
Ø Нефтеперерабатывающая промышленность использует способность ртутных паров к точной регулировке температур при очистке нефти.
Ø Военная промышленность из ртути и её соединений получает «гремучую ртуть» - взрывчатое вещество, закладываемое в детонаторы снарядов и гранат.
Ø Медицина получает антисептические, противопаразитарные, мочегонные препараты ртути. Стоматология изготавливает зубные протезы и пломбы из амальгамы олова, серебра и кадмия.
Ø Сельское хозяйство применяет органические соединения ртути как гербициды и для протравливания семян.
Ø В судостроении подводную часть морских судов покрывают специальной краской, содержащей ртуть. Соединяясь с морским хлором, на покрытии днища образуется сулема, от которой вредные бактерии гибнут.
Ø Органические
и неорганические соединения ртути находят применения в фотографии, пиротехнике,
при изготовлении художественных изделий из фарфора, дублении кожи, окрашивании
тканей. [6].
1.2 Содержание ртути в водных экосистемах и источники ее поступления
Ртуть - редкий элемент. Ее средние содержания в земной коре и основных типах горных пород оцениваются в 0,03-0,09 мг/кг, т.е. в 1 кг породы содержится 0,03-0,09 мг ртути, или 0,000003-0,000009% от общей массы (для сравнения - одна ртутная лампа в зависимости от конструкции может содержать от 20 до 560 мг ртути, или от 0,01 до 0,50% от массы). Масса ртути, сосредоточенная в поверхностном слое земной коры мощностью в 1 км, составляет 100 000 000 000 т (сто миллиардов тонн), из которых в ее собственных месторождениях находится только 0,02%. Оставшаяся часть ртути существует в состоянии крайнего рассеяния, по преимуществу в горных породах (в водах Мирового океана рассеяно 41,1 млн. т ртути, что определяет невысокую среднюю концентрацию ртути в его водах - 0,03 мкг/л). Именно эта рассеянная ртуть создает природный геохимический фон, на который накладывается ртутное загрязнение, обусловленное деятельностью человека и приводящее к формированию в окружающей среде зон техногенного загрязнения.
Известно более 100 ртутных и ртутьсодержащих минералов. Основным минералом, определяющим промышленную значимость ртутных месторождений, является киноварь. Самородная ртуть, метациннабарит, ливингстонит и ртутьсодержащие блеклые руды имеют резко подчиненное значение и добываются попутно с киноварью. Размер кристаллов киновари обычно варьируется в пределах от 2-3 до 0,1 мм; реже наблюдаются кристаллы до 1 см, более крупные (3-5 см) составляют редкость. Теоретический состав киновари: ртуть 86,2%, сера 13,8%. Но в ней часто обнаруживается примесь 15-20 элементов: кремния, алюминия, магния, меди, цинка, мышьяка, сурьмы, серебра и др.
Всего в мире обнаружено около 5000 ртутных месторождений, рудных участков и рудопроявлений, получивших самостоятельное название; из них в разное время разрабатывались около 500. Но за всю историю ртутной промышленности подавляющая часть ртути (более 80%) получена на 8 месторождениях: Альмаден (Испания), Идрия (Словения), Монте-Амиата (Италия), Уанкавелика (Перу), Нью-Альмаден и Нью-Идрия (США), Никитовка (Украина), Хайдаркан (Киргизия). Ртутные руды делятся на очень богатые (5-10% ртути и более), богатые (около 1%), рядовые (0,2-0,3%, бедные (0,06-0,12%), убогие (0,02-0,06%) и ртутьсодержащие (0,01-0,00001%). Руды большинства ныне разрабатываемых месторождений ртути - это в основном рядовые руды [14].
Загрязнение водоемов ртутью вызывает отравления водных животных и весьма опасно для человека из-за накопления ее соединений в пищевых гидробионтах. Металлическая ртуть и ее неорганические соли менее токсичны для рыб, чем органические соединения. Высокая токсичность органических препаратов ртути объясняется тем, что органический радикал способствует проникновению их в организм, что приводит к тяжелому отравлению, поражению центральной нервной системы, печени, почек и других органов за счет ингибирования тиоловых ферментов и биосинтеза белков. Ртутные препараты обладают гонадотропным и эмбриотоксическим действием. Из неорганических соединений на рыб действуют в основном растворимые соли ртути - хлориды, сульфаты и нитраты. Токсичность ртути в мягкой воде выше, чем в жесткой [14].
Согласно оценкам, кустарная и мелкомасштабная золотодобыча (КМЗ) является источником выбросов более чем 700 тонн в год ртути в атмосферу и, кроме того, 800 тонн в год ртути поступает на землю и в воды, что делает ее крупнейшим антропогенным источником ртути [15].
1.3 Поступление ртути в водные экосистемы
Распределение и миграция ртути в окружающей среде осуществляются в виде круговорота двух типов. Во-первых, глобального круговорота, включающего циркуляцию паров ртути в атмосфере (от наземных источников в Мировой океан и наоборот). Во-вторых, локального круговорота, основанного на процессах метилирования неорганической ртути, поступающей главным образом из техногенных источников. Многие этапы локального круговорота еще недостаточно ясны, но полагают, что он включает циркуляцию в среде обитания диметилртути. Именно с круговоротом второго типа чаще всего связано формирование опасных с экологических позиций ситуаций.
Поступающие в окружающую среду из природных и техногенных источников ртуть и ее соединения подвергаются в ней различным преобразованиям. Неорганические формы ртути (элементарная ртуть Hgo и неорганический ион Hg2+) претерпевают преобразования в результате окислительно-восстановительных процессов. Пары ртути окисляются в воде в присутствии кислорода неорганическую двухвалентную ртуть (Hg2+), чему в значительной мере способствуют присутствующие в водной среде органические вещества, которых особенно много в зонах загрязнения. В свою очередь, ионная ртуть, поступая или образуясь в воде, способна формировать комплексные соединения с органическим веществом. Значение имеет взаимодействие ртути с серой (сульфид-ионом), приводящее к образованию (в безкислородных условиях) устойчивого сульфида ртути HgS, который, однако, в присутствии кислорода может окисляться в растворимые соли - сульфит и сульфат ртути, что обусловливает участие металла в последующих химических реакциях. Наряду с окислением паров ртути образование Hg2+ может происходить при разрушении ртутьорганических соединений.