Материал: Разработка технологического регламента на лекарственную форму
На этикетке емкостей для сбора и хранения воды для инъекций должно быть обозначено, что содержимое, не простерилизовано.
Кислота хлористоводородная Acidum hydrochloricum
Кислота хлористоводородная разведенная Acidum hydrochloricum dilutum
Кислота соляная
HCl М.м. 36,46
Кислота хлористоводородная должна содержать газа HCl 24,8 - 25,2% ( р 1,125 - 1,127 г/см3). Кислота хлористоводородная разведенная должна содержать газа HCl 8,2 - 8,4 % ( р 1,040 - 1,041 г/см3). Описание. Бесцветная прозрачная летучая жидкость, своеобразного запаха, кислого вкуса.
Растворимость. Смешивается с водой и спиртом во всех соотношениях, образуя растворы сильно кислой реакции.
Хранение. В склянках с притертыми пробками.
Применение. Разведенную соляную кислоту применяют (внутрь в каплях в виде микстур с пепсином) при пониженной кислотности желудка; назначают с препаратами железа, т.к. соляная кислота улучшает их всасывание. В прописи Демьяновича для лечения чесотки (6%). 1) Раствора тиосульфата натрия 60% - 100 мл; 2) Раствора соляной кислоты 6% - 100 мл.
лекарственный инъекция глюкоза
2. Исследовательская часть
.1 Расчеты, особенности и технология
приготовления
Rp.:Sol. Glucosi 3% - 200 ml Natrii chloridi q.s. Ut fiat solutio isotonica Sterilisetur! D.S. Для внутривенного введения Жидкая лекарственная форма для парентерального применения - изотоничный раствор для инъекций для внутривенного введения. Ингредиенты совместимы. Дозы не проверяются, так как все ингредиенты общего списка.
Расчеты: mглюкозы= 6,0 с
учетом влажности m =![]()
![]() Эглюкозы=0,18 Э -
эквивалент изотоничности (приложение №1) 0,18 - 1,0 х - 6,67 х=1,2 -
осмотическое давление, создаваемое глюкозой. С% =
Эглюкозы=0,18 Э -
эквивалент изотоничности (приложение №1) 0,18 - 1,0 х - 6,67 х=1,2 -
осмотическое давление, создаваемое глюкозой. С% = ![]()
![]() Расчет NaCl: 0,9 - 100
мл х - 200 мл х = 1,8 NaCl - без учета глюкозы Находим
осмотическое давление, создаваемое глюкозой: 0,18 - 1,0 х - 6,67 х=1,2 mNaCl = 1,8 - 1,2
= 0,6 или по формуле:
Расчет NaCl: 0,9 - 100
мл х - 200 мл х = 1,8 NaCl - без учета глюкозы Находим
осмотическое давление, создаваемое глюкозой: 0,18 - 1,0 х - 6,67 х=1,2 mNaCl = 1,8 - 1,2
= 0,6 или по формуле:
mNaCl = 0.009 * V - (Э*m) =
0,009*200 - (6,67*0,18) = 0,6 Vстабилизатора = ![]()
![]() %сухих ЛС =
%сухих ЛС = ![]()
![]()
вода c учетом КУО
КУО - коэффициент увеличения объема (приложение №2)
Vводы = Vo - (m1*КУО1+m2 *КУО2)
- Vжидких ЛС = 200 -
(6,67*0,69 + 0,2*0,33) - 10 = 185 мл
Особенности изготовления:
a) готовим массо-объемным способом) готовим методом доведения (по приказу МЗ РФ№308)) глюкозу отвешиваем с учетом влажности (10%)) добавляем аптечный стабилизатор для стерилизации (по приказу МЗ РФ №308)) строго соблюдается режим стерилизации (по приказу МЗ РФ №308)) обеспечение быстрого охлаждения, т.к. увеличение времени стерилизации ведет к увеличению продуктов разложения) готовим в асептических условиях (так как лекарственная форма для инъекций)) фильтруем через промытый фильтр (так как концентрация >2%)) используем флаконы из нейтрального стекла) стерилизуем в паровом стерилизаторе при t 120oC; давлении 0,11 МПа; 12 минут
Рабочая пропись: Aquae pro injectionibus q.s. Natrii chloridi 0,6 Glucosi hydrici 10% 6,67 Stabilisatori officinalis 10 ml Aquae pro injectionibus ad 200 ml Vo = 200 ml
Оформление и отпуск: Основная этикетка: «Для инъекций» с синей сигнальной полосой и предупредительной надписью «Беречь от детей». Дополнительные этикетки: «Хранить в прохладном месте» - требует жидкая лекарственная форма «Стерилизовано» - так как лекарственная форма для инъекций. «Изотонично» - требует пропись в рецепте. На основной этикетке указывается:
· № аптеки
· Адрес аптеки
· Дата приготовления
· Наименование медицинского учреждения
· Отделение
· Наименование лекарственной формы (Раствор глюкозы 3% - 200 мл)
· Способ применения (внутривенно)
· Изотонирующие вещества (Натрия хлорида 0,6)
· Срок годности
· № анализа
· Подпись приготовившего
· Подпись проверившего
Регистрация лекарственной формы осуществляется в «Журнале регистрации результатов контроля различных стадий изготовления инъекций и инфузий» (приложение №3)
Технология
изготовления: В асептических условиях, в асептическом блоке. В стерильную
подставку отмерила ~ 100 мл воды для инъекций. Отвесила 0,6 натрия хлорида,
поместила в подставку и растворила. Затем отвесила 6,67 глюкозы водной (10%),
поместила в подставку и растворила. Затем в подставку добавила 10 мл аптечного
стабилизатора. Перенесла раствор в мерный цилиндр и довела водой для инъекций
до 200 мл. Н.о. ± 2% (приложение №4); Примерно 4 мл отлила в пенициллиновый
флакон и вместе с заполненным ППК и оформленным рецептом передала провизору-аналитику
для полного химического анализа. После положительного результата раствор
профильтровала во флакон для отпуска через стерильный промытый складчатый
фильтр из плотной фильтровальной бумаги с подложенным под нее тампоном ваты,
завернутым в стерильную марлевую салфетку. Затем флакон укупорила и проверила
на чистоту на приборе УК-2 (приложение №5). После проверки обкатала флакон
металлическим колпачком, промаркировала и простерилизовала в паровом
стерилизаторе при t 120oC; давлении
0,11 МПа; 12 минут. После стерилизации снова проверила раствор на чистоту на
УК-2, также проверила цветность, прозрачность и качество укупорки раствора.
Затем оформила флакон этикетками. Зарегистрировала лекарственную форму в
«Журнале регистрации результатов контроля различных стадий изготовления
инъекций и инфузий».
.2 Приготовление и контроль
качества раствора глюкозы 3% для инъекций
. Характеристика готового продукта
Изотоничный раствор глюкозы 3% для инъекций.
Препарат представляет 3% раствор глюкозы и натрия хлорида в воде для инъекций.
Состав: Глюкозы водной 10% 6,67 Натрия хлорида 0,6 Стабилизатор аптечный 10 мл Воды для инъекций до 200 мл
Бесцветная прозрачная жидкость без запаха.
Препарат по стерильности и отсутствию механических примесей должен выдерживать требования, указанные в ст. 286 ГФ X.
Содержание глюкозы водной в 1 мл препарата соответственно должно быть 0,0291 - 0,0309 г.
Препарат выпускают во флаконах вместимостью 200 мл, укупоренных резиновыми пробками ИР-119, И-51, 25П, ИР-21 под обкатку алюминиевыми колпачками.
Хранят при комнатной
температуре, срок хранения 10 суток.
Таблица 1. Характеристика сырья
и материалов
№
п/п
Наименование
сырья, полуфабрикатов
Нормативно-техническая
документация
Квалификация
Содержание
основного в-ва в %
Примечание
1.
2
I. Сырье Вода
очищенная Глюкоза Натрия хлорид Кислота хлориствоводородная
ГФ
X
Для
инъекций
Не
менее 5,82 и не более 6,18
Хранить
в хорошо укупоренной таре.
II. Материалы
1.
2.
Марля
медицинская Вата медицинская
ГОСТ
9412-77 ГОСТ 5556-75
Гигроскопическая
Гигроскопическая
3.
Бумага
фильтровальная лабораторная
ГОСТ
12026-76
4.
Колпачки
алюминевые
5.
Пробки
резиновые
25П,
ИР - 21 ИР -119, И-51
6.
Пергамент
7.
Флаконы
стеклянные
НС-2,
НС-1
8.
Мерная
посуда для приготовления растворов и др.
. Изложение технологического
процесса
Технологический процесс
производства раствора глюкозы для инъекций состоит из 6 стадий.
1.
Подготовительные
работы.
2.
Приготовление
раствора.
3.
Фильтрование
и фасовка раствора.
4.
Стерилизация
раствора.
5.
Контроль
готовой продукции.
6.
Оформление.
Стадия 1. Подготовительные
работы
.1. Подготовка помещения,
персонала, вспомогательного материала, тароукупорочных средств.
Уборку помещения, подготовку
персонала, стерилизацию воздуха проводят в соответствии с действующими
приказами Минздрава СССР.
Вспомогательный материал,
сосуды для приготовления растворов, «мерные колбы, цилиндры, вороний,
стеклянные фильтры, тароукупорочные средства (сосуды, пергамент, резиновые
пробки) обрабатывают и стерилизуют в соответствии с действующей инструкцией по
приготовлению растворов для инъекций в аптеках, утвержденной Минздравом СССР.
Алюминиевые колпачки
выдерживают 15 мин в 1- 2% растворе моющих средств, подогретом до 70-80°С,
моют, затем раствор сливают, а колпачки промывают водопроводной проточной
водой.
Чистые колпачки сушат в биксах
в воздушных стерилизаторах.
.2. Подготовка сырья.
Для получения 3% раствора
глюкозы попользуют глюкозу с содержанием влаги 10%.
Стадия 2. Приготовление
раствора
Загрузка сырья, растворение,
анализ пробы.
Раствор глюкозы для инъекций
готовят массо - объемным способом. В мерник-смеситель или другую емкость
загружают воды для инъекций приблизительно % нужного количества, добавляют
натрия хлорид, глюкозы и стабилизатор аптечный и с помощью мешалки раствор
перемешивают до полного растворения веществ, затем доливают воды для инъекций
до заданного объема и снова перемешивают.
Раствор контролируют на
качественное и количественное содержание глюкозы.
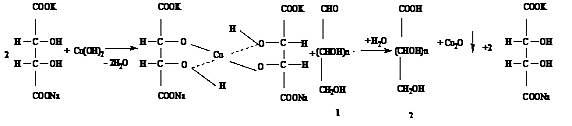
Определение подлинности. 1. С реактивом Фелинга:
При нагревании глюкозы с реактивом Фелинга образуется кирпично-красное
окрашивание.
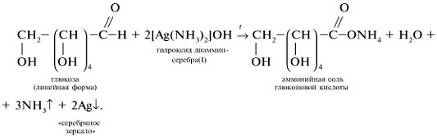
. Реакция «серебряного зеркала»:
AgNO3+2NH4OH→[Ag(NH3)2]OH+HNO3
K2HgI4
+ Количественное определение: Метод
рефрактометрии: н.о. = ±3% 5,82 - 6,18 Fглюкозы5% = 0,00142 -
Фактор показателя преломления глюкозы m = Стадия 3. Фильтрование и фасовка
раствора
.1. Фильтрование, розлив, укупорка
пробками, первичный контроль на отсутствие механических загрязнений.
При удовлетворительном результате
анализа раствор с использованием приборов. Для фильтрования используют
фильтрующие воронки со стеклянными фильтрами ПОР' 10 (размер пор 3-'0 мкм), ПОР
16 (размер пор 10-16 мкм), разъемные фильтр-воронки Ф-30, или стеклянные
воронки в сочетании с разными фильтровальными материалами.
Фильтрование проводим через промытый
фильтр. Фильтрование раствора сочетают с одновременным розливом его в
подготовленный стерильный флакон, укупоривают пробкой и проводят первичный
контроль раствора на отсутствие механических загрязнений в соответствии с
действующей инструкцией по контролю растворов для инъекций, изготовленных в
аптеках, на чистоту от механических загрязнений.
При обнаружении механических
загрязнений раствор перефильтровывают.
.2. Укупорка алюминиевыми
колпачками, маркировка.
Сосуд с раствором закрывают
металлическими колпачками с помощью обкаточного приспособления, маркируют путем
надписи, штамповки, используя жетоны и др., затем передают на стерилизацию.
Стадия 4. Стерилизация растворов
Раствор во флаконах по 200 мл
стерилизуют в паровом стерилизаторе паром под давлением 0,11 МПа при
температуре 120°С в течение 12 мин.
Стадия 5. Контроль готовой продукции
1.
Раствор
во флаконах контролируют на отсутствие механических загрязнений (см. п. 3.1.).
2.
От
каждой серии раствора отбирают 1 флакон для контроля по всем физико-химическим
показателям.
Определяют внешний вид
раствора, рН, подлинность, количественное содержание глюкозы в соответствии с
методиками, изложенными в разделе «Стадия 2».
5.3. Бракераж.
Раствор во флаконах считают
забракованным при несоответствии его физико-химическим показателям, содержании
видимых механических загрязнений, нестерильности, нарушений герметичности
укупорки, недостаточности объема заполнения флаконов.
Стадия 6. Оформление
Флаконы с растворами оформляют
согласно действующим правилам оформления лекарств в аптеках.
Техника безопасности
При приготовлении растворов для
инъекции следует руководствоваться правилами по устройству, эксплуатации,
технике безопасности и производственной санитарии при работе в аптеках,
действующими правилами по эксплуатации и технике безопасности при работе на
автоклавах.
Выводы
. Изучила научную литературу и
нормативную документацию по вопросу изготовления лекарственных средств
. Изучила актуальность данной темы
. В ходе работы была приготовлена
лекарственная форма, проанализирована и составлен технологический регламент.
Список литературы
1. Попова Т.Н., Пегова И.А., Рыжова
Е.С. «Краткий курс лекций по фармацевтической химии», под редакцией
заслуженного учителя РФ Пигаловой Н.А.
2. И.И. Краснюк, Г.В.
Михайлова, Л.И. Мурадова «Фармацевтическая технология» учебник
. Государственная фармакопея XI
издания
. Государственная фармакопея
X издания
. Образовательный портал
. И.А. Муравьев «Технология
лекарственных форм» учебник
. Приказ МЗ РФ №214 «О
контроле качества лекарственных форм»
. Приказ МЗ РФ №308
«Инструкция по изготовлению жидких лекарственных форм в аптеке»
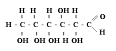 +
3KOH →
+
3KOH →
![]() +
4KI + Hg↓
+ 2H2O
+
4KI + Hg↓
+ 2H2O
![]()
![]()