Материал: Расчетно-графическая работа
2.2. Рельеф.
Дача расположена на самом высоком в пределах территории академии плоском водораздельном мореном холме с пологим склоном на юго-запад и крутым на северо-восток.
Максимальная отметка высоты холма 175 метров над уровнем моря; минимальная – 160 метров над уровнем моря; что составляет разницу высот в 15 метров в пределах территории ЛОД.
Уровень грунтовых вод при средней для ЛОД высоте над уровнем моря – 166 метров находится на глубине 5 метров.
Выход грунтовых вод на поверхность наблюдается на высоте 165 метров над уровнем моря в виде ключей.
2.3. Территория.
Площадь ЛОД составляет 248,7 га и расположена в северо-западной части города Москвы, на юго-западе территориального землярасположения академии.
По форме Лесная опытная дача представляет собой практически правильный прямоугольник, протягивающийся с северо-запада на юго-восток, длиной в 2,8 км и шириной в 1,6 км. Общее протяжение границ ЛОД составляет 8,3 км.
Дача находится в кольце шоссейных дорог. Из общего периметра около 85% территория обращена к городу.
Юг дачи граничит с городской больницей №50, восток – с автотранспортным шоссе, запад – с железной дорогой (станция «Гражданская», римского направления).
Дача была объявлена заповедной зоной 3 декабря 1940 года, а также вторично – 30 мая 1950 года.
После Великой Отечественной войны началось масштабное строительство в городе Москве, а также по границам ЛОД, что привело к положению Дачи между многоэтажными домами, асфальтированными дорогами с интенсивным движением уже в 1962 году.
С повышением роста населения, увеличилась и посещаемость ЛОД, которая использовалась как рекреационная зона.
2.4. Почва.
Первые исследования почвенного покрова ЛОД были проведены в 70-х годах ХХ века.
ЛОД расположена на юге лесолуговой зоны (дерново-подзолистой), с редкими включениями торфяно-глеевых почв.
Исследования показывают, что с каждым годом происходит уплотнение почв, хотя по сведениям недавних лет было показано, что ЛОД имеет мощный перегнойный горизонт, отличающийся рыхлым сложением.
Валовые запасы питательных веществ( азота и фосфора) в верхних горизонтах довольно высокие, и при благоприятных условиях они легко используются корнями древесных растений.
2.5. Климат.
Осадки годовые(средние): 538мм.
Максимальные осадки: в июле и августе.
Минимальные осадки: в январе и феврале.
Осадки за период май-август (вегетационный период для яровых культур):269мм.
Число дней с осадками (среднее): 173 дня
Снег: 24% от годовых осадков.
Средняя глубина промерзания почвы открытого места: 40 см
Средняя высота снежного покрова: 50 см.
Глава III.
Экология элемента.
Медь — элемент одиннадцатой группы четвёртого периода (побочной подгруппы первой группы) периодической системы химических элементов Д. И. Менделеева, с атомным номером 29. Обозначается символом Cu. Простое вещество медь — это пластичный переходный металл золотисто-розового цвета (розового цвета при отсутствии оксидной плёнки).
3.1. История Cu.
Медь — один из первых металлов, широко освоенных человеком из-за сравнительной доступности для получения из руды и малой температуры плавления. Он входит в семёрку металлов, известных человеку с очень древних времён. Этот металл встречается в природе в самородном виде чаще, чем золото, серебро. Экспериментальные исследования С. А. Семёнова с сотрудниками показали, что, несмотря на мягкость меди, медные орудия труда по сравнению с каменными дают значительный выигрыш в скорости рубки, строгания, сверления и распилки древесины, а на обработку кости затрачивается примерно такое же время, как для каменных орудий. В древности медь применялась также в виде сплава с оловом — бронзы — для изготовления оружия и т. п., бронзовый век пришел на смену медному. Сплав меди с оловом (бронзу) получили впервые за 3000 лет до н. э. на Ближнем Востоке. Бронза привлекала людей прочностью и хорошей ковкостью, что делало её пригодной для изготовления орудий труда и охоты, посуды, украшений. Все эти предметы находят в археологических раскопах.
Первоначально медь добывали из малахитовой руды. Для этого смесь руды и угля помещали в глиняный сосуд, сосуд ставили в небольшую яму, а смесь поджигали. Выделяющийся угарный газ восстанавливал малахит до свободной меди.
3.2. Нахождение Cu в природе.
Среднее содержание меди в земной коре (Кларк) — (4,7-5,5)·10−3% (по массе). В морской и речной воде содержание меди гораздо меньше: 3·10−7% и 10−7% (по массе).
Медь встречается в природе, как в соединениях, так и в самородном виде. Промышленное значение имеют халькопирит(CuFeS2), также известный как медный колчедан, халькозин(Cu2S) и борнит(Cu5FeS4). Вместе с ними встречаются и другие минералы меди: ковеллин (CuS),куприт(Cu2O),азурит (Cu3(CO3)2(OH)2),малахит(Cu2CO3(OH)2). Иногда медь встречается в самородном виде, масса отдельных скоплений может достигать 400 тонн. Сульфиды меди образуются в основном в среднетемпературных гидротермальных жилах. Также нередко встречаются месторождения меди в осадочных породах— медистые песчаники и сланцы. Наиболее известные из месторождений такого типа — Удокан в Забайкальском крае, Жезказган в Казахстане, медоносный пояс Центральной Африки и Мансфельд в Германии. Другие самые богатые месторождения меди находятся в Чили (Эскондида и Кольяуси) и США (Моренси). Большая часть медной руды добывается открытым способом. Содержание меди в руде составляет от 0,3 до 1,0 %.
3.3. Физические свойства Сu.
Медь — золотисто-розовый пластичный металл, на воздухе быстро покрывается оксидной плёнкой, которая придаёт ей характерный интенсивный желтовато-красный оттенок. Тонкие плёнки меди на просвет имеют зеленовато-голубой цвет.
Медь
обладает высокой тепло- и электропроводностью (занимает
второе место по электропроводности
среди металлов после серебра).
Удельная электропроводность при 20 °C:
55,5-58 МСм/м.
Медь имеет относительно большой температурный
коэффициент сопротивления:
0,4 %/°С и в широком диапазоне температур
слабо зависит от температуры. Медь
является диамагнетиком.
Атомная плотность Cu
=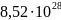 {\displaystyle
8,52\centerdot 10^{28}}
(атом/м³).
{\displaystyle
8,52\centerdot 10^{28}}
(атом/м³).
3.4. Химические свойства Cu.
В
соединениях медь проявляет две степени
окисления: +1 и +2. Соединения с
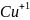 бесцветны, а с
бесцветны, а с
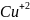 синие, сине-зеленые. Медь
является
слабым восстановителем, не вступает в
реакцию с водой и разбавленной соляной
кислотой. Окисляется концентрированными
серной и азотной кислотами(1), «царской
водкой»(2), кислородом(3), галогенами(4),
оксидами неметаллов(5). Вступает в реакцию
при нагревании с галогеноводородами.
синие, сине-зеленые. Медь
является
слабым восстановителем, не вступает в
реакцию с водой и разбавленной соляной
кислотой. Окисляется концентрированными
серной и азотной кислотами(1), «царской
водкой»(2), кислородом(3), галогенами(4),
оксидами неметаллов(5). Вступает в реакцию
при нагревании с галогеноводородами.
1)Cu + H2SO4 (конц.) → CuO + SO2↑ + H2O
3Cu + 8HNO3( разбав.) → 3Cu(NO3)2+2NO↑+4H2O
2)3Cu
+ 2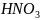 + 6HCl →
+ 6HCl →
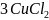 + 2NO↑ +
+ 2NO↑ +
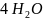
3)
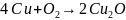
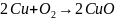
4)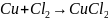
5)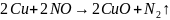
3.5. Биологическая роль.
Медь является необходимым элементом для всех высших растений и животных. В токе крови медь переносится главным образом белком церулоплазмином. После усваивания меди кишечником она транспортируется к печени с помощью альбумина.
Медь встречается в большом количестве ферментов, например, в цитохром-с-оксидазе, в содержащем медь и цинк ферменте супероксид дисмутазе, и в переносящем молекулярный кислород белке гемоцианине. В крови всех головоногих и большинства брюхоногих моллюсков и членистоногих медь входит в состав гемоцианина в виде имидазольного комплекса иона меди, роль, аналогичная роли порфиринового комплекса железа в молекуле белка гемоглобина в крови позвоночных животных.
Предполагается, что медь и цинк конкурируют друг с другом в процессе усваивания в пищеварительном тракте, поэтому избыток одного из этих элементов в пище может вызвать недостаток другого элемента. Здоровому взрослому человеку необходимо поступление меди в количестве 0,9 мг в день.
При недостатке меди в хондро- и остеобластах снижается активность ферментных систем и замедляется белковый обмен, в результате замедляется и нарушается рост костных тканей.
Содержание меди в питьевой воде не должно превышать 1 мг/л, однако недостаток меди в питьевой воде также нежелателен. Всемирная Организация Здравоохранения сформулировала (ВОЗ) в 1998 году это правило так: «Риски для здоровья человека от недостатка меди в организме многократно выше, чем риски от её избытка».
В 2003 году в результате интенсивных исследований ВОЗ пересмотрела прежние оценки токсичности меди. Было признано, что медь не является причиной расстройств пищеварительного тракта.
Бактерицидные свойства меди и её сплавов были известны человеку давно. В 2008 году после длительных исследований Федеральное Агентство по Охране Окружающей Среды США (US EPA) официально присвоило меди и нескольким сплавам меди статус веществ с бактерицидной поверхностью. Особенно выраженно бактерицидное действие поверхностей из меди (и её сплавов) проявляется в отношении метициллин-устойчивого штамма стафилококка золотистого, известного как «супермикроб» MRSA.
Излишняя концентрация ионов меди придает воде отчётливый «металлический вкус». У разных людей порог органолептического определения меди в воде составляет приблизительно 2—10 мг/л. Естественная способность к такому определению повышенного содержания меди в воде является природным механизмом защиты от приёма внутрь воды с излишним содержанием меди.
3.6. Производство Cu.
Медь производится из сульфидных руд, которые содержат эту медь в объеме минимум 0,5%. В природе существует около 40 минералов, содержащих данный металл. Наиболее распространенным сульфидным минералом, который активно используется в производстве меди, является халькопирит. Производство состоит из следующих этапов:
Измельчение руды в специальных дробилках и последующее более тщательное ее измельчение в мельницах шарового типа.
Флотация. Предварительно измельченное сырье смешивается с малым количеством флотореагента и затем помещается во флотационную машину. В качестве такого добавочного компонента обычно выступает ксантогенат калия и извести, который в камере машины покрывается минералами меди.
Обжиг. Руды и их концентраты проходят процесс обжига в моноподовых печах, что необходимо для выведения из них серы. В результате получается огарок и серосодержащие газы, которые в дальнейшем используют для получения серной кислоты.
Плавка шихты в печи отражательного типа. На этом этапе можно брать сырую или уже обожженную шихту и подвергать ее обжигу при температуре 1500°С. Важным условием работы является поддержанием нейтральной атмосферы в печи. В итоге происходит сульфидирование меди и ее преобразование в штейн.
Конвертирование. Полученная медь в сочетании с кварцевым флюсом продувается в специальном конвекторе на протяжении 15-24 ч. В итоге получается черновая медь в результате полного выгорания серы и выведения газов. В ее состав может входить до 3% различных примесей, которые благодаря электролизу выводятся наружу.
Рафинирование огнем. Металл предварительно расплавляется и затем рафинируется в специальных печах. На выходе образуется красная медь.
Электролитическое рафинирование. Этот этап проходит анодная и огневая медь для максимальной очистки.
3.7. Применение Cu.
Из-за низкого удельного сопротивления , медь широко применяется в электротехнике для изготовления силовых и других кабелей, проводов или других проводников, например, при печатном монтаже. Медные провода, в свою очередь, также используются в обмотках электроприводов и силовых трансформаторов.
Другое полезное качество меди — высокая теплопроводность. Это позволяет применять её в различных теплоотводных устройствах, теплообменниках, к числу которых относятся и широко известные радиаторы охлаждения, кондиционирования и отопления, компьютерных кулерах, тепловых трубках.
В связи с высокой механической прочностью и пригодностью для механической обработки медные бесшовные трубы круглого сечения получили широкое применение для транспортировки жидкостей и газов: во внутренних системах водоснабжения, отопления, газоснабжения, системах кондиционирования и холодильных агрегатах. В ряде стран трубы из меди являются основным материалом, применяемым для этих целей: во Франции, Великобритании и Австралии для газоснабжения зданий, в Великобритании, США, Швеции и Гонконге для водоснабжения, в Великобритании и Швеции для отопления.
В ювелирном деле часто используются сплавы меди с золотом для увеличения прочности изделий к деформациям и истиранию, так как чистое золото — очень мягкий металл и нестойко к механическим воздействиям.
Медь — самый широко употребляемый катализатор полимеризации ацетилена. Из-за этого трубопроводы из меди для транспортировки ацетилена можно применять только при содержании меди в сплаве материала труб не более 64 %.
Широко применяется медь в архитектуре. Кровли и фасады из тонкой листовой меди из-за автозатухания процесса коррозии медного листа служат безаварийно по 100—150 лет.
3.8. Опасность Cu.
Медь относиться ко 2 классу опасности. Ее обнаруживают в сульфидных осадках вместе со свинцом, кадмием и цинком. Медь присутствует в небольших количествах в цинковых концентратах и может переноситься на большие расстояния с воздухом и водой. Аномальное содержание меди обнаруживается в растениях с воздухом и водой. Аномальное содержание меди обнаруживается в растениях и почвах на расстоянии более 8 км от плавильного завода. Токсические свойства меди изучены гораздо меньше, чем те же свойства других элементов.