Материал: Рак мочевого пузыря
Начальным признаком инфильтрации подслизистого слоя может быть инъецированность кровеносных сосудов вокруг опухоли. Ворсинки плотные, а основание опухоли шире.
При папиллярном раке существенно меняется внешний вид опухоли, ее ворсины становятся короткими, широкими и ригидными, ножка опухоли укорачивается, а иногда становится и вовсе неразличимой. Поверхность опухоли очень часто бывает покрыта участками геморрагий и фиброзными наложениями, может быть инкрустирована солями. На поверхности опухоли появляются изъязвления и очаги некроза. Границы опухоли плохо различимы, а слизистая оболочка вокруг опухоли отечна. При гистологическом исследовании чаще всего определяется переходно-клеточный рак второй или третьей степени дифференцировки. Опухоль прорастает мышечный слой, имеет очаги некроза, кровоизлияний и обызвествлений. Если опухоль расположена вблизи устья мочеточника, то оно может быть или невидимым, или расположенным асимметрично из-за деформации мочевого пузыря.
При эндофитном росте (солидный, или первично инфильтрирующий рак мочевого пузыря) опухоль не имеет ворсин, а основание сливается с резко измененной слизистой оболочкой мочевого пузыря. Новообразование как бы выбухает в полость мочевого пузыря. Границы опухоли нечеткие. Очень часто опухоль изъязвляется, а язвы покрываются фиброзным налетом. Такие опухоли при цистоскопии диагностировать трудно, так как они симулируют туберкулез мочевого пузыря или интерстициальный язвенный цистит.
Следует помнить, что цистоскопия является субъективным методом исследования. Иногда даже опытные врачи принимают за опухоль мочевого пузыря туберкулезные изменения слизистой оболочки, простую язву мочевого пузыря, уретероцеле или интерстициальный цистит. Цистоскопия затруднена при малой емкости мочевого пузыря, мутной среде, интенсивной гематурии, тампонаде мочевого пузыря сгустками крови, больших и вдающихся в полость мочевого пузыря аденоматозных узлах предстательной железы. Расширяет диагностические возможности цистоскопии видеозапись изображения, применение жесткой системы линз с высокой разрешающей способностью. Окончательный диагноз возможен после биопсии опухоли.
Биопсия позволяет не только морфологически подтвердить диагноз, но и
оценить особенности морфологического строения опухоли (переходно-клеточный или
плоскоклеточный рак, аденокарцинома, недифференцированный рак, неэпителиальная
опухоль), и, что особенно важно для прогноза и назначения в послеоперационном
периоде комбинированной химио- и иммунотерапии, определить степень
дифференцировки клеток. Кроме того, эндовезикальная биопсия позволяет отличить
опухоль мочевого пузыря от опухолеподобных поражений: фолликулярного цистита,
малакоплакии, эндометриоза, амилоидоза, железистой метаплазии, кистозного
цистита и других.
. Лечение
Касаясь вопросов лечения больных РМП нужно сказать, что в настоящее время хирургические методы являются ведущими. В большинстве случаев они дополняются иммуно-химиотерапией, лучевой терапией.
Все виды хирургического лечения больных раком мочевого пузыря разделяют на четыре группы:
) ТУР мочевого пузыря, которая может сочетаться с лазерным воздействием;
) Открытую резекцию мочевого пузыря, в том числе резекцию "в ложках", плазменное или лазерное выпаривание опухоли;
) Цистэктомию с различными вариантами деривации мочи;
) Паллиативные операции.
Основным методом лечения в такой ситуации является трансуретральная электрорезекция стенки мочевого пузыря с новообразванием (ТУР). Эта методика имеет диагностическое и лечебное значение - она позволяет забрать материал для гистологического исследования (подтверждение диагноза) и удалить новообразование в пределах здоровых тканей. К сожалению, после ТУР стенки мочевого пузыря с новообразованием вероятность рецидива опухоли составляет в среднем 50%. Снизить этот процент позволяет использование фотодинамической диагностики и внутрипузырное введение вакцины БЦЖ или химиопрепаратов (митомицин, доксорубицин и др.). В фазе разработки находятся многообещающие методики внутрипузырного лекарственного электрофореза. После выполнения ТУР абсолютно ОБЯЗАТЕЛЬНО выполнять повторные контрольные осмотры мочевого пузыря для исключения рецидива. При многократных рецидивах после ТУР и обнаружении низкодифференцированного ("злого") рака нередко бывает целесообразно прибегнуть к радикальной операции - цистэктомии (удаление мочевого пузыря) с формированием нового мочевого пузыря из сегмента кишки.
Радикальная цистэктомия - метод выбора в лечении глубоко инфильтрирующих опухолей. Она включает удаление мочевого пузыря и простаты у мужчин; удаление мочевого пузыря, уретры, передней стенки влагалища и матки у женщин. В случае распространенного поражения (уретра, матка, простата, мочеиспускательный канал) возможность применения эндоскопических операций практически исключена. Иногда последний этап операции (создание кишечного мочевого пузыря) откладывается на некоторое время (это позволяет минимизировать объем операции у ослабленных больных на запущенных стадиях рака), и тогда используется методика выведения мочеточников на кожу.
Химиотерапия при инвазивном РМП применяют в неоадъювантном, адъювантном периоде, а также в качестве самостоятельного вида лечения при дессиминированном процессе. Следует отметить, что до недавнего времени спектр противоопухолевых препаратов, активных при РМП, был ограниченным. Традиционно применяемой схемой являлась М-VАС/ М-VЕС (метотрексат, винбластин, адриамицин и цисплатин). Эффективность схемы у больных с генерализованным РМП составляет около 40%, средняя выживаемость - 13 мес. Однако это достаточно жесткая схема, приводящая к развитию более чем у 85% больных побочных реакций и осложнений. Наиболее значимы из них - миелосупрессия, которая наблюдается у 38% больных, нефротоксичность, возникающая у 36% больных, высокая эметогенность - до 76%.
В настоящее время препаратом выбора при лечении инвазивного и метастатического РМП являются гемцитабин (гемзар). Гемзар - препарат из группы антиметаболитов антагонистов пиримидина. Действие препарата заключается в нарушении функции ДНК-полимеразы, что в конечном итоге блокирует клетку в фазах G1 и S и приводит к ее гибели.
Режимы химиотерапии при РПМ должны базироваться на платиносодержащих препаратах. С этих позиций особенно важными являются данные о синергизме действия гемцитабина и цисплатина. Так по данным литературы, эффективность комбинации гемцитабина и препаратов платины (GC) составляют 45-79%. При этом лечебный режим GC обладает меньшей токсичностью по сравнению со схемой М-VACи требует меньшего объема сопутствующей терапии.
В настоящее время режим GC считается лучшей альтернативой для больных распространенным и метастатическим РМП и является стандартом лечения этой категории больных.
Лучевая терапия рака мочевого пузыря.
В мировой практике, до настоящего времени, существует неоднозначное отношение к лучевой терапии при РМП. В США первичная лучевая терапия РМП практически не применяется. В Великобритании и Европе это основной метод лечения распространенного РМП, а цистэктомию выполняют лишь при опухолях мочевого пузыря, резистентных к лучевой терапии. В нашей стране лучевая терапия при РМП применяется как самостоятельно, так и в сочетании с хирургическим и/или химиотерапевтическим лечением. Облучение может осуществляться как на аппаратах для дистанционной, так и контактной лучевой терапии. Причем оптимальная методика лучевой терапии выбирается в зависимости от локализации опухолевого процесса в мочевом пузыре и степени его внепузырного распространения. Так, при прорастании опухолью мышечной стенки или наличии метастатического поражения зон регионарного лимфооттока, необходимо проведение послеоперационной лучевой терапии. При РМП можно применять и брахитерапию (внутриполостная и внутритканевая лучевая терапия). Однако из-за сложности проведения, и при этом необходимости вложения больших финансовых средств, для ее реализации, она применяется, в основном, в крупных специализированных центрах экономически развитых стран. При внутриполостном облучении разовая очаговая доза составляет, как правило, 3-5 Гр, а суммарная очаговая доза доводится до 45-50 Гр. При сочетаном облучении доза при внутриполостной лучевой терапии составляет, в среднем, 30-35 Гр.
До настоящего времени весьма сложной остается проблема лечения местно-распространенного РМП, при котором радикальным методом лечения является органоуносящая операция - цистэктомия. Вместе с тем, применение комбинированного лечения с использованием на 1-ом этапе лучевойтерапии в полной дозе, а затем, при частичной регрессии, выполнение органосохраняющих операций, позволяет решить задачу радикального лечения с сохранением "собственного" мочевого пузыря.
На основании собственного клинического опыта мы считаем, что при лечении опухолей мочевого пузыря можно ограничиться одной лишь ТУР органа только при наличии поверхностного (неинвазивного) высокодифференцированного рака. Во всех других случаях за ТУР должна следовать цистэктомия или лучевая терапия по радикальной программе. При этом, суммарная очаговая доза на слизистую оболочку мочевого пузыря и пути регионарного метастазирования при опухолях Т1-2 составляет при мелком фракционировании дозы 44-46 Гр, а при Т3 - доза на слизистую оболочку доводится до 65-70 Гр.
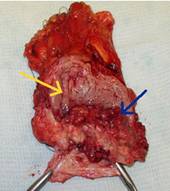
Мышечно-инвазивный рак мочевого пузыря (нормальная
слизистая - желтая стрелка, опухоль - синяя стрелка)
Список используемой литературы
1. Урология (Н.А. Лопаткин, 2006 г. Стр. 313-335)
. http://medbe.ru/materials/urologicheskie-zabolevaniya/etiologiya-i-patogenez-opukholey-mochevogo-puzyrya/
3. http://www.diagnos-online.ru/zabol/zabol-323.html
. http://formen.narod.ru/opuholi_mochpuz.htm
. http://www.uroportal.ru/zabolevaniya/0/13
. http://www.bladdercancer.ru/klasifikacija/index.html