Материал: Производство технической глюкозы
Производство технической глюкозы
Алматинский Технологический Университет
Кафедра
"Технология хлебопродуктов и перерабатывающих производств"
На
тему: Производство технической глюкозы
Выполнила: Ршимова Айгерим
Группа: ТХ-12-2
Проверила:
Рустемова А. Ж.
Алматы
2014
План
1. Глюкоза
. Получение глюкозы
. Физико-химические свойства глюкозы
. Характеристика продуктов глюкозного производства
. Производство технической глюкозы
. Получение глюкозно-фруктозного сиропа из крахмала
Список литературы
1.
Глюкоза
Глюкоза (декстроза) - крахмалопродукт, углевод, наиболее распространенный в природе, моносахарид.
Глюкоза может существовать в виде циклов (α
и
β
глюкозы).
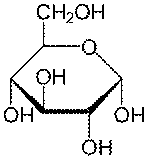
α-глюкоза
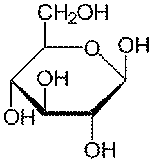
β-глюкоза
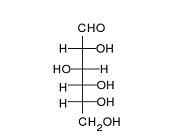
В пищевой промышленности глюкозой называют D-глюкозу, полученную гидролизом крахмала с последующей очисткой, кристаллизацией, центрифугированием и сушкой (ГОСТ Р 51953-2002 Крахмал и крахмалопродукты. Термины и определения).
Виды глюкозы
• фармакопейная, удовлетворяющая требованиям фармакопеи;
• гранулированная, полученная высушиванием и гранулированием глюкозного утфеля;
• влажная, получаемая при центрифугировании глюкозного утфеля;
• желтая - влажная глюкоза, получаемая при центрифугировании глюкозного утфеля по двухпродуктовой схеме производства.
Свойства глюкозы
Для производства продуктов питания используется способность D-глюкозы
• регулировать сладость и улучшать вкус изделий;
• увеличивать устойчивость при хранении;
• ускорять ферментацию и брожение.
Применяется также в качестве наполнителя и структурообразователя.
Применение глюкозы
Декстроза используется для производства широкого спектра продуктов питания:
• кондитерских изделий;
• десертов и мороженого;
• алкогольных и безалкогольных напитков;
• детского питания;
• консервов.
Глюкозу считают основным источником энергии для млекопитающих и человека, обеспечивает процессы метаболизма. Она необходима для нормального функционирования всех систем организма, для полного сгорания жиров. При ряде заболеваний необходимо ограничение употребления глюкозы в пищу.
Глюкоза - простейший природный сахар. Она
довольно широко распространена в природе. Свободная глюкоза содержится в
плодах, ягодах, входит в состав меда. Особенно часто глюкоза встречается в
природе в виде сложных высокомолекулярных соединений. таких, как крахмал,
клетчатка и др. Все виды углеводов, поступающих с пищей в организм человека,
превращаются в глюкозу. Глюкоза имеет важное значение для углеводного обмена
живого организма и служит источником питания всех его клеток.
. Получение глюкозы
В промышленных масштабах глюкозу получают в основном из крахмала и крахмалсодержащего сырья. В зависимости от технологии переработки сырья производство глюкозы подразделяется на получение следующих продуктов: кристаллической гидрат-ной глюкозы, медицинской гидратной и ангидридной, пищевой кусковой, брикетированной, гранулированной и порошкообразной глюкозы, технической глюкозы и глюкозно-фруктозных сиропов.
Производство глюкозы условно можно разделить на две стадии: приготовление высоко доброкачественных глюкозных сиропов и получение из них глюкозы и глюкозо содержащих продуктов.
Первая стадия складывается из следующих технологических операций: подготовки крахмальной суспензии, гидролиза (кислотного или ферментативного), нейтрализации кислоты или инактивации фермента, очистки (диатомитом, активным углем или нонообменниками), уваривания и охлаждения глюкозного сиропа. Технологические операции первой стадии осуществляются почти так же, как и в паточном производстве, и с использованием аналогичной аппаратуры. Указанные операции, теоретические основы кислотного н ферментативного гидролиза крахмала, а также физико-химическая сущность ионообменной очистки сиропов подробно освещены в предыдущих разделах, поэтому ниже остановимся только на особенностях, характерных для глюкозного производства.
Дальнейшая обработка глюкозного сиропа (вторая стадия) связана с особенностями готовой продукции и заключается в осуществлении следующих операций: если кристаллизация производится с отделением межкристального раствора, то за ней следуют центрифугирование, сушка и просеивание, если кристаллизация идет без отделения межкристального раствора, то она осуществляется в распылительной сушилке с досушиванием продукта или затвердеванием утфеля в формах с последующим измельчением и просеиванием или брикетированием.
При получении фруктозо содержащих продуктов
включается операция по изомеризации глюкозы в сиропах.
. Физико-химические свойства глюкозы
Глюкоза принадлежит к наиболее простому классу углеводов - моносахаридам и является природным органическим соединением, состоящим из трех элементов: углерода, водорода и кислорода. По классификации моносахарид глюкоза относится к гексозам.
Моносахариды, содержащие в оксикарбонильной форме альдегидную группу С, называются альдозами. В альдозах карбонильная группа находится на конце цепи молекулы.
Углеродные атомы в молекуле принято нумеровать, начиная с того конца цепи, на котором находится или к которому ближе карбонильная группа.
Наличие в глюкозе четырех асимметрических атомов углерод обусловливает существование 16 стереоизомеров В- и Ь-ряда. Изомеры с гидроксилом, расположенным справа у наиболее отдаленного от карбонильной группы асимметрического углеродного атома, относятся к Б-ряду, слева-к Ь- глюкоза растительного происхождения - к О-ряду.
Оксикарбонильная форма хорошо объясняет реакционную способность глюкозы. Но в водном растворе большинство молекул находится в циклической форме. Карбонильная группа взаимодействует со спиртовой группой пятого или четвертого углеродного атома. При этом двойная связь карбонильной группы разрывается, водород от спиртового гидроксила переходит к карбонильному кислороду, образуя так называемый полуацетальный или гликозидный гидроксил, а кислород спиртового гидроксила соединяется с первым углеродным атомом и образуется шести- или пятичленное кольцо. Отсюда название: глюкопираноза и глюкофураноза. Пиранозные формы глюкозы более устойчивы, чем фуранозные. Поэтому кристаллическая глюкоза находится в пиранозной "форме. Фуранозы встречаются только в растворах. Образованный при полуацетальном углеродном атоме гликозидный гидроксил отличается от остальных ОН-групп большой реакционной способностью и обусловливает редуцирующую способность глюкозы.
Если в молекуле моносахарида гидроксильные группы при первом и втором асимметрических углеродных атомах направлены в одну сторону плоскости кольца, стереоизомер называют а-формой, а если в разные стороны - р-формой.
Природная глюкоза существует в пиранозной форме в виде "-О-глюкопиранозы. При растворении в воде она таутомерно превращается в четыре циклические полуацетальные формы Б-ряда.
Между этими формами в растворе устанавливается динамическое равновесие, сопровождающееся оптическим эффектом, поскольку глюкоза является оптически активным соединением. Б-глюкоза отклоняет плоскость поляризации вправо и называется правовращающим изомером.
Мерой оптической активности вещества служит его удельное вращение плоскости поляризации. Удельное вращение раствора глюкозы изменяется со временем, пока не достигнет некоторого постоянного значения. Это явление получило название мутаротация. Мутаротация связана с взаимным превращением таутомерных форм глюкозы и устанавливанием равновесия между ними. Свежеприготовленные растворы а- и р-Б-глюкозы имеют вращение +110,1° и -{-19,3° соответственно. С течением времени удельное вращение первого падает, а второго возрастает, в обоих случаях достигая постоянного значения 4-52,5°. Если исходить из равновесного взаимопревращения пяти таутомерных форм, то скорость мутаротации должна выражаться весьма сложным уравнением. Однако для Б-глюкозы скорость мутаротации подчиняется уравнению обратной реакции первого порядка, что соответствует равновесию только между двумя таутомерными формами: а- и р-изомерами пиранозной формы, поскольку они преобладают в растворе. Прочие таутомеры присутствуют в очень низких концентрациях.
Глюкоза легкорастворима в воде, обладает сладким вкусом и проявляет слабые кислотные свойства. Константа электролитической диссоциации при 18° С у глюкозы равна 3,6-10,3. Увеличение рН насыщенных растворов вызывает повышение степени ионизации глюкозы как кислоты, а следовательно и ее растворимости.
Из водных пересыщенных растворов при температуре 0,5- 50° С глюкоза выкристаллизовывается в моногидратной форме.
СбН^Об-НгО. Тонкие гемиморфные пластинки гидратной глюкозы относятся к кристаллам моноклинической системы. Имеют относительную плотность 1,5714, молекулярную массу 198, точка плавления их находится между 86-90° С. Во время кристаллизации 1 г-моль гидратной глюкозы выделяет 19,76 кДж тепла.
Кроме кристаллизационной воды гидратная глюкоза способна удерживать еще некоторое количество влаги, так называемой гигроскопической. Количество присоединенной гигроскопической влаги зависит от влажности окружающей среды.
При температуре 50-90° С из пересыщенных растворов выкристаллизовывается ангидридная глюкоза С6Н^Ое, кристаллы которой относятся к ромбической системе и представляют собой удлиненные призмы с концевыми гемигедральными поверхностями. Ангидридная глюкоза имеет относительную плотность 1,5384, молекулярную массу 180, температуру плавления 146-147° С, при кристаллизации I г-моль ее выделяет 9,89 кДж тепла.
Глюкоза является сильным восстановителем и легко окисляется. В качестве окислителя в аналитической практике чаще всего применяют оксид меди в виде щелочного раствора. При окислении глюкозы происходит восстановление меди с выделением красного осадка закиси. По количеству выпавшего осадка редуцированной меди с помощью таблиц находят концентрацию глюкозы в растворе.
В производственных условиях глюкоза подвергается интенсивному воздействию высокой температуры, кислот, оснований и различных несахаров, в результате чего часть ее разрушается, обусловливая безвозвратные потери. Так, процесс кислотного гидролиза крахмала при получении глюкозы протекает при низком значении рН и высокой температуре.
Эти условия благоприятны как для реакции разложения глюкозы, так и для процесса ее реверсии. Эти две реакции приводят к так называемым "химическим" потерям глюкозы. В кислой среде глюкоза относительно устойчива к нагреванию, при постоянном рН скорость разложения глюкозы увеличивается пропорционально повышению температуры. Скорость кислотного разложения глюкозы при температуре 100° С в 0,1 н. растворе соляной кислоты примерно в 300 раз меньше скорости гидролиза крахмала Однако особое влияние на разложение глюкозы оказывает продолжительность нагрева.
Зоной максимальной устойчивости глюкозы является интервал рН 2,0-4,2. При рН -3,5 распад глюкозы минимальный. В среде с рН >4,2 под влиянием гидроксильных ионов происходит увеличение содержания глюкозы в карбонильной форме, что способствует ускорению реакции разложения (с увеличением рН на единицу константа скорости реакции разложения увеличивается в 5,83 раза). В среде с рН <2,0 разложение ускоряется в результате более быстрой и глубокой дегидратации молекул (с уменьшением рН на единицу константа скорости реакции "увеличивается в 5,3 раза). Дегидратация молекул глюкозы происходит с отнятием трех молекул воды и образованием малоустойчивого соединения - оксиметил фурфурол а, которое легко разлагается на муравьиную и левулиновую кислоты. Оксиметилфурфурол обладает высокой реакционной способностью и является источником образования продуктов распада глюкозы, в том числе красящих веществ.
В условиях кислотного гидролиза крахмала глюкоза склонна подвергаться частичной полимеризации с образованием продуктов. реверсии, обладающих большей молекулярной массой. Реверсия глюкозы происходит двумя путями- конденсацией двух или более молекул глюкозы с образованием ди- и трисахаридов и присоединением молекул глюкозы к имеющимся в растворе молекулам гидроксиметилфурфурола и олигосахаридов. В процессе реверсии получаются преимущественно углеводы с 1-6-глюкозидными связями. В заводских гидролизатах реакция реверсии идет активнее,, чем в растворах чистой глюкозы, что подтверждает участие олигосахаридов в процессе реверсии. При постоянной концентрации и температуре количество ревертоз уменьшается с увеличением рН и достигает минимума при рН 5, при рН 6 реверсия вновь-увеличивается.
Образование оксиметил фурфурола не является единственной и главной причиной потемнения глюкозных сиропов. Со временем оксиметилфурфурол разрушается и при высоких температурах, происходит потемнение сиропов от светло-желтого до коричневого цвета.
Интенсивность коричневой окраски вызывается присутствием в сиропе плохо отмытых от крахмала азотистых веществ. При сильном нагреве белки расщепляются и растворяются. Почти все-аминокислоты активно участвуют с глюкозой в реакции образования красящих веществ. Степень окрашивания пропорциональна количеству аминного азота. Чем выше изоэлектрическая точка аминокислоты, тем сильнее побурение. Красящие вещества можно разделить на три группы:
· продукты распада глюкозы;
· меланоидины - продукты взаимодействия редуцирующих веществ с азотсодержащими веществами;
· продукты карамелизации, возникающие при термическом разрушении Сахаров.
Процесс образования красящих веществ происходит сложно,, через ряд промежуточных стадий, причем одновременно протекает несколько реакций. Например, в меланоидиновой реакции наряду с взаимодействием моносахаридов с азотсодержащими веществами, независимо от него происходят реакции глюкозы и аминокислот. Реакция образования меланоидинов идет весьма интенсивно при взаимодействии глюкозы с ди- и трипептидами и усиливается по мере повышения щелочности раствора.
Минимальное количество красящих веществ образуется при рН 3. Одной из важнейших черт красящих веществ является кислотный характер. Значительное каталитическое действие на реакцию образования красящих веществ оказывают окислы железа, мели и некоторых других тяжелых металлов. Красящие вещества склонны к образованию стойких комплексов с различными катионами металлов. Это увеличивает интенсивность цветности растворов. Образующиеся красящие вещества нельзя считать конечными продуктами, процесс их формирования протекает непрерывно. В ходе реакции происходит укрупнение частиц красящих веществ, что увеличивает оптическую плотность растворов.
Дисперсионный анализ характеризует неоднородность размеров частиц. Около 70% частиц имеет радиус от 0,75 до 4,21 им, остальные выше 4,21 нм. Эти данные объясняют затруднения, возникающие при адсорбционной очистке сиропов, и причины повышенной цветности кристаллов глюкозы.
В сильнощелочной среде устойчивость глюкозы резко снижается, прекращается мутаротация и образуются щелочные глюкоза-ты. При длительном воздействии щелочи на холоде или при слабом нагревании происходят эпимеризация глюкозы, превращение ее в другие моносахариды, родственные по строению, такие, как фруктоза, манноза, пентоза и др.
При определенных условиях глюкоза вступает в
реакцию с некоторыми солями. Так, с хлористым натрием глюкоза образует легко
кристаллизующееся двойное соединение.
. Характеристика продуктов глюкозного
производства
Кристаллическую гидратную глюкозу получают глубоким гидролизом крахмала кислотой или ферментным препаратом с последующим сгущением очищенного сиропа, кристаллизацией и центрифугированием утфеля (смеси кристаллов и межкристального раствора). Гидратная глюкоза должна представлять собой кристаллический порошок белого цвета со сладким вкусом (без постороннего привкуса) я свойственным ей запахом. Цветность раствора (в единицах оптической плотности) должна быть не более 0,09 для ФЭК-М, 0,16 для ФЭК-56 и 0,18 для ФЭК-56М. прозрачность (светопропускаемость) - не менее 69% для ФЭК-М, 65% для ФЭК-56 и 65% для ФЭК-56М; удельное вращение [а]о° 52.5-53,0%, содержание золы - не более 0,07%, влаги не более 9,0, железа - не более 0,003%. Не допускается содержание свободных минеральных кислот и остатка при просеивании на металлическом сите с отверстиями размером 1,5 мм (ГОСТ 975-75).