Материал: Производство серной кислоты при повышенном давлении
Производство серной кислоты при повышенном давлении
Кафедра общей химической технологии
Курсовая расчетная работа
по теме: «Производство серной кислоты при
повышенном давлении»
Москва 2014
Оглавление
Задание на курсовую работу
Введение
. Теоретическая часть
.1 Производство серной кислоты
.2 Технологическая схема производства серной кислоты. Описание технологического процесса, функциональная и операторная схема
.3 Основные этапы сернокислого производства
. Расчетная часть
.1 Материальный баланс процесса
.2 Материальный баланс для печи сжигания серы
.3 Расчет сушильной башни
.4 Расчет олуемного абсорбера (ОА)
.5 Расчет моногидратного абсорбера (МА)
.6 Расчет технологических показателей
Библиографический список
Задание на курсовую работу
Вариант №18.
· Схема функционирует под общим давлением 0,6 МПа.
· Воздух после сушильной башни поступает в контактный аппарат 4 с температурой 30ºС. Степень сгорания серы принята равной 100%.
· Степень превращения диоксида серы в контактных аппаратах 4 и 5 по заданию составляет 0,95 и 0,98 соответственно.
· В абсорберах 6 и 7 происходит полное поглощение серного ангидрида.
· Производительность 100%-ой серной кислоты: 1000 т/сутки.
· Массовое соотношение серная кислота: олеум = 5:1
· Содержание свободного SO3 в олеуме: 6%.
· Парциальное давление водяных паров в воздухе 4,8 КПа.
· Концентрация диоксида серы на выходе из печи 13,3% об.
· Концентрация орошающей кислоты в сушильной башне 93,0% масс.
· Концентрация орошающей кислоты в моногидратном абсорбере 98,4% масс.
Задание:
) исходя из технологической схемы производства серной кислоты, составить ее операторную схему;
) найти аналитическое выражение для расчета общей степени превращения диоксида серы по ее значениям для 1-ой и 2-ой степеней контактирования;
) рассчитать материальный баланс ХТС производства серной кислоты в целом;
) составить материальные балансы для 1-ой и 2-ой ступеней контактирования, для этого определить:
· объем и состав газовой смеси перед 1-ой ступенью;
· объем и состав газовой смеси на выходе из нее;
· количество и состав газа после 2-ой ступени;
) составить материальный баланс сушильной башни, определить:
· количество паров воды в воздухе, поступающем на сушку;
· потоки олеума и кислоты, поступающие из абсорберов 6 и 7 в сборник сушильной башни;
· количество воды, направляемой в сборник кислоты сушильной башни для разбавления кислоты до заданной концентрации;
· потоки кислоты, поступающей в сборники абсорберов из сборника сушильной башни;
) составить материальный баланс абсорбционного отделения. Для этого определить:
· количество серного ангидрида, поглощаемого в абсорберах;
· потоки олеума и кислоты, поступающие из сборников абсорберов в сборник сушильной башни и из сборника сушильной башни в сборники абсорберов;
) рассчитать объем и состав выхлопных
газов.
Введение
Среди многих сотен тысяч органических соединений, известных в настоящее время, серной кислоте принадлежит особая роль.
Широкий спектр применения серной кислоты, прежде всего, обусловлен ее физическими и химическими свойствами. Серная кислота - бесцветная едкая тяжелая маслообразная жидкость без запаха, смешивается с водой в любых соотношениях. Эта кислота гигроскопична, то есть способна поглощать влагу из воздуха.
При обычной температуре она не летуча и не имеет запаха. Серная кислота взаимодействует почти со всеми металлами. Скорость этого взаимодействия зависит от природы металла, концентрации кислоты и температуры [1].
На поглощении воды серной кислотой основана осушка газов. Серную кислоту выпускают нескольких сортов, в зависимости от того, для производства какого продукта она требуется. Например, для производства медицинских препаратов, особо чистых реактивов, для заливки аккумуляторов требуется чистая кислота.
В других случаях для производства подойдет менее чистая серная кислота, так называемое купоросное масло. Сернокислотная промышленность выпускает олеум, используемый при производстве некоторых органических препаратов и взрывчатых веществ. Олеум представляет собой раствор серного ангидрида в серной кислоте.
В современном мире многие отрасли промышленности такие как, металлургия, нефтяная промышленность, производство удобрений, микроэлектронное производство, тонкие химические технологии - немыслимы без применения серной кислоты.
Например, большое количество серной кислоты используется для получения фосфорных и азотных удобрений. В металлургии серную кислоту применяют для обнаружения микротрещин в готовой продукции, а также серную кислоту используют в цехах гальванопокрытий. Также серная кислота необходима для переработки различных руд и ископаемых. Большое количество серной кислоты требуется нефтеперерабатывающей промышленности для очистки нефти и ее различных фракций. В органическом синтезе концентрированная серная кислота - необходимый компонент при получении многих красителей и лекарств.
серный кислота окисление абсорбер
1. Теоретическая часть
.1 Производство серной кислоты
Сырьевая база производства серной кислоты - это серосодержащие соединения, из которых с помощью обжига можно получить диоксид серы. В промышленности около 80% серной кислоты получают из природной серы и железного колчедана.
Иногда в качестве сырья используют отходящие газы цветной металлургии, получаемые при обжиге сульфидов цветных металлов и содержащие диоксид серы, а в некоторых производствах применяют сероводород, образуемый при сероочистке в нефтепереработке.
При получении серной кислоты из отходящих газов стадия обжига входит в состав другого производства.
Химическая схема производства серной кислоты из
серы включает следующие стадии:
S + O2 => SO2
+ Qр
(1)2+ 1/2 O2 <=> SOз
+ Qр(2)з
+ H2O
<=>H2SO4
+ Qр(3)
Минеральное сырье содержит примеси, поэтому функциональная схема включает еще стадию очистки газа после его обжига. Сера - легкоплавкое вещество с температурой плавления 386 К. Перед сжиганием ее расплавляют, используя пар, получаемый при утилизации теплоты горения.
Расплавленная сера отстаивается и фильтруется для удаления имеющихся в природном сырье примесей, затем насосом подается в печь сжигания.
При горении серы по реакции 1 часть кислорода эквимолярно переходит в диоксид серы, поэтому суммарная концентрация О2 и SO2 постоянна и равна концентрации кислорода Со в исходном газе (а+b = Со), так что при сжигании серы в воздухе:
b = 0,21 - a.
1.2 Технологическая схема производства серной кислоты при повышенном давлении. Описание технологического процесса, функциональная и операторная схемы
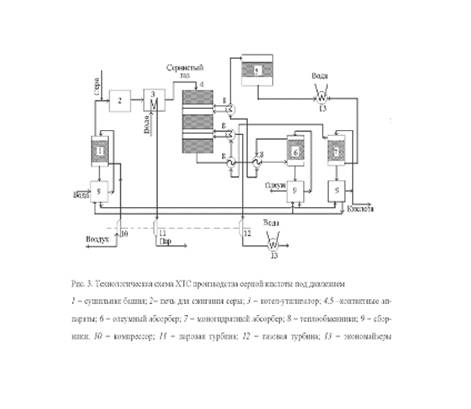
Расправленная сера подается с потоком воздуха в печь 2 , где сжигается до диоксида серы.
Сернистый газ охлаждается в котле- утилизаторе 3 и направляется в контактный аппарат 4, где на катализаторе осуществляется процесс окисления SO2 в SO3 методом двойного контактирования с промежуточной абсорбцией SO3 в абсорбере 6.
Трехслойный контактный аппарат 4 составляет первую ступень контактирования. Нагретый за счет химической реакции газ после прохождения каждого из трех слоев катализатора охлаждается в теплообменнике 8.
Газ после первой ступени освобождается от SO3 в абсорбере 6.
Контактный аппарат 5 представляет собой вторую ступень контактирования - в ней происходит доокисление непрореагировавшего SO2.
После доокисления газовая смесь охлаждается в экономайзере 13 и поступает в моногидратный абсорбер 7.
Сушка атмосферного воздуха нагнетаемого компрессором 10 производится в сушильной башне 1 орошаемой концентрированной серной кислотой.
После абсорбера 7 газ подогревается в теплообменнике 8, после чего отправляется на газовую турбину 12 и затем в экономайзер 13.
Продукция в виде олеума и моногидрата отбирается
из абсорберов 6 и 7.
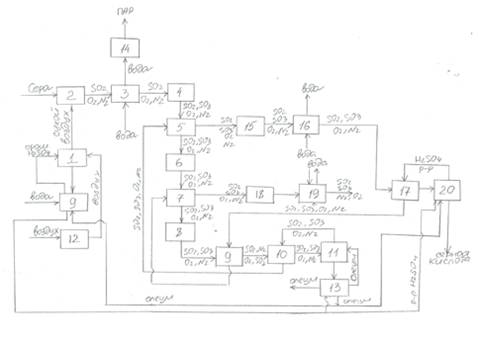
Структурная схема производства серной кислоты
при повышенном давлении
1 - сушильная башня; 2 - печь для сжигания серы;
3- котел-утилизатор; 4,6,8,15 - контактный аппарат; 5,7,9,10 - теплообменники;
11 - олеумный абсорбер; 12 - компрессор; 9,13,20 - сборники; 14 - паровая
турбина; 16,19 - экономайзеры; 17 - моногидратный абсорбер; 18 - газовая
турбина.
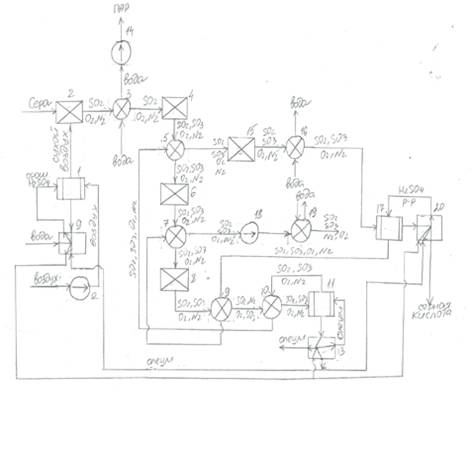
Операторная схема
производства серной кислоты при атмосферном давлении:
- сушильная башня; 2 - печь для сжигания серы;
3- котел-утилизатор; 4,6,8,15 - контактный аппарат; 5,7,9,10 - теплообменники;
11 - олеумный абсорбер; 12 - компрессор; 9,13,20 - сборники; 14 - паровая
турбина; 16,19 - экономайзеры; 17 - моногидратный абсорбер; 18 - газовая
турбина.
1.3 Основные этапы сернокислого
производства
Процесс производства серной кислоты из элементарной серы состоит из следующих основных этапов:
. Подготовка сырья: очистка и плавление серы; очистка, сушка и дозировка воздуха;
. Сжигание серы:
S + O2
= SO2
(1).
Процесс ведут с избытком воздуха. Выделяется очень большое количество теплоты ΔН = -362,4 кДж/моль
. Контактное окисление SO2
в
SO3:
SO2+
0,5O2
= SO3
(2).
на ванадиевом катализаторе при температуре 420-550˚C, тепловой эффект реакции при 500˚C составляет 94,23 кДж/моль;
4. Абсорбция SO3:
3
+ H2O = H2SO4 (3).
Абсорбционная колонна орошается 98,4% H2SO4.
Перед отправкой на склад кислота разбавляется до ~ 93%
2. Расчетная часть
2.1 Материальный
баланс процесса
Расчет производительности серной кислоты (кмоль/ч).
Производительность
по 100% серной кислоте - 1000 т/сутки.
П(т/сутки)=П * 1 000/(кол-во часов в сутки)=П(кг/ч)
П (с.к.) (кмоль/ч)
=( П (с.к.) кг / ч ) / (М (с.к.) кг / кмоль)
П (с.к.) = 1 000 * 1 000 / 24 = 41 666,667 кг/ч
М (с.к.) = 2*1,008 + 32,065 + 4*15,999 = 98,077 кг / кмоль
П (с.к.) = 41 666,667 / 98,077 = 424,836 кмоль /ч
![]()
Рассчитаем
количество получившегося олеума:
![]()
где n - массовое соотношение кислоты и олеума
![]()
На основании этих данных, а также зная степени
превращения и абсорбции, мы можем рассчитать количество серы, необходимое для
получения продуктов. Примем, что вся сера сгорает полностью:
![]()
По реакциям, проходящим, видим, что
стехиометрические соотношения одинаковы и равны единице:
S + O2 = SO2
SO2
+ ![]()
![]() O2 = SO3
O2 = SO3
SO3 + H2O = H2SO4
Составим уравнение, где x - это кол-во серы (сернистого газа, так как окисление серы до диоксида происходит 100%).:
После 1ой ступени окисления поток:
![]()
После абсорбции в олеумном абсорбере:
![]()
После 2ой ступени окисления:
![]()
После абсорбции в моногидратном абсорбере:
![]()
Общее аналитическое выражение для расчета общей степени превращения сернистого газа:
![]()
Найдём количество серы, затраченное на образование олеума и серной кислоты. Олеум состоит из SO3 и серной кислоты. Содержание SO3 в олеуме 6%:
![]()
![]()
![]()
![]()
Количество серы, затраченное на образование товарной кислоты:
![]()
Общее количество серы, затраченное на образование товарных продуктов:
![]()
![]()
![]()
Доля серы, потерянная в отходящих газах:
![]()
![]()
![]()
Зная количество серы, рассчитаем
количество воздуха, необходимое для её сжигания. По уравнению реакции окисления
найдём количество затраченного кислорода:
S + O2 = SO2
![]()
![]()
Концентрацию кислорода в сернистом газе можно найти по уравнению:
![]()
Количество кислорода, оставшегося после реакции:
![]()
![]()
![]()
![]()
Определим поток сухого воздуха.
Для этого составим пропорцию: ![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
Определим количество воды в воздухе до осушки.
![]()
Количество влажного воздуха:
![]()